DIABETES MELLITUS IN DOGS: A CASE OF INSULIN RESISTANCE
REGISTRO DOI: 10.69849/revistaft/ch10202511300517
Livia Saab Muraro1
Audrey de Cássia Lirio da Silveira Ramos2
Sofia de Souza Pereira Gomes3
Rogério M. Soila4
Daniele Silvano Gonçalves5
Resumo
Diabetes mellitus (DM) é a endocrinopatia mais comum em cães, caracterizada por hiperglicemia e frequentemente classificada como insulino-deficiente. Em contraste, a resistência insulínica, embora menos comum como forma primária, é influenciada por múltiplos fatores, incluindo condições endócrinas, obesidade e uso de glicocorticóides. O presente trabalho tem como objetivo relatar um caso de diabetes mellitus em um cão macho castrado, Bido Antônio, que apresentou resistência à insulina devido a comorbidades associadas e a um fator exógeno: a absorção de estrogênio tópico proveniente do gel de reposição hormonal utilizado pela tutora. O paciente, um Lhasa Apso, 7 anos, castrado, apresentava obesidade, hipertensão, alterações ultrassonográficas (compatíveis com pancreatopatia crônica e adrenomegalia) e necessidade de doses crescentes de insulina. A dosagem de estradiol no paciente (71,45 pg/mL, acima do valor de referência para machos castrados) revelou-se um fator complicador. Após a orientação de mudança no local de aplicação do gel pela tutora, a dosagem de estrogênio no cão diminuiu (59,80 pg/mL) e o controle glicêmico melhorou, permitindo a manutenção da glicemia apenas com insulina basal. O caso demonstra a complexidade da resistência insulínica na DM e sublinha a importância de uma anamnese detalhada, incluindo a investigação de exposição a hormônios exógenos no ambiente domiciliar.
Palavras-chave: Diabetes mellitus; Insulina; Fatores de Resistência Insulínica; Canino.
1. INTRODUÇÃO
Diabetes mellitus (DM) é uma doença crônica e sistêmica, apontada como o distúrbio mais comum do pâncreas endócrino. Caracteriza-se por síndrome de hiperglicemia (ADA, 2010), resultante de uma deficiência absoluta ou relativa de insulina devido à secreção inadequada pelas células beta, sendo semelhante ao diabetes mellitus tipo 1 em humanos e, por isso, classificada como insulino dependente (NELSON, 2015). As causas e à classificação da DM têm sido amplamente discutidas na literatura (AHLGREN et al., 2014, NELSON, REUSCH, 2014, GILOR et al., 2016). Atualmente, o projeto ALIVE (Agreeing Language in Veterinary Endocrinology) a define como um grupo de doenças com múltiplas etiologias (NIESSEN et al., 2022).
A doença pode ser classificada com base no modelo utilizado em humanos (tipo 1 – juvenil e tipo 2 – senil) (HOENIG, 2002) e outros autores descrevem-na como DM dependente de insulina, quando há necessidade de terapia insulínica, e não dependente de insulina, utilizando dietas, fármacos hipoglicemiantes e atividade física para o controle glicêmico (GUPTILL, GLICKMAN, GLICKMAN, 2003).
Essa classificação insulino-deficiente e insulino-resistente é a proposta da ALIVE. A DM insulino-deficiente caracteriza-se por disfunção progressiva ou destruição das células β pancreáticas, culminando em secreção insuficiente de insulina endógena e consequente dependência de terapia insulínica exógena para manutenção da normoglicemia. Em contraste, a DM insulino-resistente resulta de redução da sensibilidade periférica à ação da insulina, apesar de níveis adequados ou elevados do hormônio, estando frequentemente associada a adiposidade aumentada, inflamação metabólica e desregulação endócrina (NIESSEN et al., 2022).
A etiopatogênese do DM insulino deficiente em cães envolve fatores como predisposição genética, a disfunção da célula beta ou a destruição por respostas imunomediadas associada a doença pancreática exócrina, pancreatite, neoplasia ou idiopática, toxicidade medicamentosa, glicotoxicidade, lipotoxicidade, infecção, aplasia/hipoplasia de células beta (NELSON, 2015, NIESSEN et al., 2022), diferente de humanos é um achado raro em cães jovens, sendo a média de idade de ocorrência em torno de 9 anos, com semelhança da DM autoimune latente do adulto em humano (LADA – latente autoimmune diabetes of the adult) (CATCHPOLE et al., 2005, DAVISON et al., 2008).
A DM insulino resistente é influenciada por fatores endócrinos como o GH (origem hipofisária, mamária ou exógeno), esteróides como os glicocorticóides (exógeno ou endógeno) e progestágenos (diestro, gestacional ou exógeno) e outros hormônios como catecolaminas (exógeno e endógeno), hipertireoidismo além da obesidade, mediadores inflamatórios e desordens nos receptores e sinalização intracelular (NELSON, 2015, NIESSEN et al., 2022). Esses fatores geralmente podem estar associados a DM tipo 1 em cães (HOENIG, 2002), exercem influência no controle glicêmico com a terapia insulínica, um efeito patológico aos efeitos da insulina (BEHREND et al., 2022).
A resistência insulínica em cães pode decorrer de uma combinação de processos inflamatórios crônicos, alterações hormonais e uso de fármacos, tornando o controle glicêmico particularmente desafiador. Embora esses fatores sejam conhecidos, ainda são limitados os relatos clínicos que abordam casos complexos envolvendo múltiplos elementos simultaneamente.
Em vista dos múltiplos fatores que contribuem para a resistência insulínica e a dificuldade no controle glicêmico, o presente trabalho objetiva relatar caso de diabetes mellitus em um cão que apresenta à resistência insulínica multifatorial, como processos inflamatórios (dermatite, otite, uveíte, doença periodontal), além do uso de glicocorticóides e contato com estrógeno exógeno, discutindo os possíveis mecanismos envolvidos e suas implicações terapêuticas.
2. REVISÃO DA LITERATURA
A diabetes mellitus (DM) considerada uma das endocrinopatias mais comuns em cães (CATCHPOLE et al., 2005), bastante frequente nas rotinas clínicas, doença grave que pode comprometer o bem-estar dos cães (HEELEY et al., 2020).
Doença complexa, de evolução crônica, que resulta em hiperglicemia persistente (ADA, 2010), devido a disfunção insulínica, seja por problemas relacionados à secreção, por deficiência absoluta ou relativa de insulina, interação com receptores específicos, ou em ambos (WHO, 2019; BEHREND et al., 2022, NIESSEN et al., 2022).
As concentrações séricas persistentes de glicose acima de 180-220mg/dl são suficientes responsáveis por sinais clínicos que são frequentemente reportados como polidipsia persistente, poliúria, polifagia com perda de peso, desenvolvimento de catarata e uveíte induzida por cristalino que levam o animal à cegueira transitória e permanente (BEAM, CORREA, DAVIDSON, 1999; RICHTER, GUSCETTI, SPIESS, 2002, BEHREND et al., 2022; SAMSON, RAND, FORD, 2023).
Eventualmente, se não tratada ou inadequadamente controlada o aumento da mobilização de gordura leva à lipidose hepática, hepatomegalia, hipercolesterolemia, hipertrigliceridemia e aumento do catabolismo, que resultam cetonemia, a cetonúria e a cetoacidose com comprometimento progressivo da saúde do paciente (BEHREND et al., 2022).
Historicamente, a classificação da diabetes mellitus em cães se apoiou em modelos provenientes da medicina humana, especialmente na distinção entre diabetes tipo 1 e tipo 2. Entretanto, com o acúmulo de evidências clínicas e epidemiológicas específicas da espécie, observou-se que tais categorias não refletiam adequadamente a diversidade de mecanismos envolvidos na doença canina, marcada por forte influência de fatores hormonais, reprodutivos, imunológicos e pancreáticos. Esse avanço no conhecimento reforçou a necessidade de desenvolver sistemas classificatórios próprios da medicina veterinária, mais coerentes com a fisiopatologia observada em cães (CATCHPOLE et al., 2005; NELSON, REUSCH, 2014; GILOR, 2016). Esse desenvolvimento abre caminho para a compreensão dos modelos atualmente empregados.
Atualmente, não existe uma classificação diagnóstica universalmente aceita, mas formas insulino dependentes e insulino resistentes de DM canina foram descritas (CATCHPOLE et al., 2005), evoluindo para a publicação e sistema de classificação mais recentes sobre este tópico pelo Projeto ALIVE (Agreeing Language in Veterinary Endocrinology) (NIESSEN et al., 2022).
Nesse cenário de evolução conceitual e necessidade de padronização, o Projeto ALIVE surge como um marco científico relevante para a endocrinologia veterinária, ao propor uma linguagem unificada e critérios classificatórios mais coerentes com a biologia da DM canina e felina. Essa iniciativa internacional sistematiza definições e terminologias, permitindo distinguir de maneira mais precisa as formas insulino-deficientes e insulino-resistentes, além de reconhecer a coexistência de mecanismos mistos em muitos pacientes. O ALIVE representa, portanto, um avanço importante para a comunicação científica, para o ensino e para a prática clínica, fornecendo um fundamento teórico atualizado e amplamente aplicável (NIESSEN et al., 2022).
A diabetes mellitus é classificada em humanos em dois tipos: o Tipo 1, caracterizado pela produção insuficiente de insulina, e o Tipo 2, marcado pela resistência à insulina nos tecidos (HOENIG, 2002).
No projeto ALIVE a diabetes mellitus é classificada pela etiologia em duas formas principais: insulino-deficiente e insulino-resistente sumarizada no trabalho de Niessen et al. (2022) e descritas a seguir, ainda ressaltam que ambas as formas de diabetes podem ser observadas em cães e gatos, e os animais podem apresentar características de ambos os mecanismos de forma simultânea, ou seja, uma combinação de deficiência e resistência à insulina.
A DM insulino-deficiente pode ocorrer quando a secreção da insulina é reduzida ou defeituosa e os fatores que levam a secreção reduzida são: células beta do pâncreas falham na produção de insulina; destruição das células pelas seguintes causas por mecanismos imunomediados e/ou associados a doenças no pâncreas exócrino, como pancreatite, neoplasia e causas idiopáticas; toxicidade ao diazoxido; infecção; morte celular (apoptose) das células beta por glicotoxicidade, lipotoxicidade e também causas idiopáticas; aplasia, atrofia, hipoplasia das células beta (NIESSEN et al., 2022).
A DM insulino resistente está relacionada: Influência endócrina: a) GH exógeno ou endógeno pela hipófise ou glândula mamaria; b) esteróides como a hipersecreção dos glicocorticóides endógenos ou a administração de glicocorticóides exógenos, progestágenos endógenos em fase lútea (gestação ou diestro) ou progestágenos exógenos.; c) catecolaminas; d) hormônios tireoidianos em hipertireoidismo; Obesidade; Drogas: diuréticos tiazídicos, agonista beta adrenérgicos; Mediadores inflamatórios; Desordens do receptor ou sinalização intracelular (NIESSEN et al., 2022).
Da mesma forma, entende-se a complexidade causada por várias combinações de fatores genéticos e ambientais (GILOR et al., 2016, DENYER, CATCHPOLE, DAVISON, 2021a, O’KELL, DAVISON, 2023). Portanto, a DM canina é uma doença altamente heterogênea (GILOR et al., 2016) e esclarecimento científico é necessário para melhorar a classificação e facilitar o manejo personalizado dos pacientes (DENYER et al., 2025).
À medida que as diferentes etiologias se tornam mais bem compreendidas, o tratamento pode ser mais especificamente adaptado ao paciente individual. O tratamento mais específico para a etiologia subjacente presumivelmente levará a um melhor controle dos sinais clínicos de DM e possivelmente aumentará as taxas de remissão (BEHREND et al., 2022).
A maioria dos pacientes diabéticos caninos depende de injeções externas de insulina (DAVISON, HERRTAGE, CATCHPOLE, 2005) e o número reduzido de células beta observado no pâncreas de cães diabéticos (SHIELDS et al., 2015) sugere que a DM canina resulta da perda de células beta e/ou falha na regeneração. Em alguns cães, a deficiência de insulina pode ser precedida por resistência à insulina, que pode ser devida aos efeitos de drogas ou hormônios na ação da insulina (NIEESSEN et al. 2022).
Ademais, a DM é a endocrinopatia mais frequente em cães (CATCHPOLE et al., 2005, O’KELL et al., 2017), como demostrado em estudo de prevalência de DM canino nos EUA em que passou de 19 casos para 64 por 10.000 entre 1970 e 1999 (GUPTILL, GLICKMAN, GLICKMAN, 2003), na Suécia em que a incidência foi de 13 casos para 10.000 cães entre 1995 a 2004 (FALL et al., 2007).
Pöppl e González (2005) observaram o aumento nos casos de DM canina na região sul do Brasil, com a prevalência de 0,11% (1 caso de DM para 865 consultas) no período de janeiro de 2000 a outubro de 2004. Acrescentam as características dessa população, os quais 95% dos cães eram fêmeas e 69% destas desenvolveram a doença durante a fase do diestro, com a idade variou de 2 a 15 anos (média 10,45 ± 3,16 anos) com pico de prevalência aos 10 anos.
De forma semelhante no Reino Unido (DAVISON, HERRTAGE, CATCHPOLE, 2005) e nos EUA (GUPTILL, GLICKMAN, GLICKMAN, 2003) a DM normalmente se desenvolve entre 5 e 12 anos de idade, casos raros em cães com menos de 12 meses de idade (CATCHPOLE et al., 2013).
Alguns estudos relatam uma predominância em fêmeas, no Reino Unido cerca de 53% fêmeas (DAVISON, HERRTAGE, CATCHPOLE, 2005), como no caso na Suécia em 72% da população eram fêmeas (FALL et al., 2007). Em concordância, referem que fêmeas tem risco aumentado de desenvolver DM em comparação aos machos (GUPTILL, GLICKMAN, GLICKMAN, 2003).
Enquanto outros levantamentos não demonstraram uma predileção por sexo (HESS et al., 2000; HUME, DROBATZ, HESS, 2006) e complementam que machos castrados apresentam risco aumentado em comparação aos machos não castrados (GUPTILL, GLICKMAN, GLICKMAN, 2003; MATTIN et al., 2014).
No entanto, não está claro se o sexo sozinho está associado à DM (MATTIN et al., 2014; CATHPOLE et al., 2013; USUI, YASUDA, KOKETSU, 2015). Essa discordância, pode ser explicada pela diferença nas características da população estuda nas diferentes localidades, já que cães na Europa têm maior probabilidade de permanecer sexualmente intactos (e em risco de desenvolver diabetes do diestro) do que cães nos EUA, onde recomenda-se a castração (O’KELL et al., 2017).
O principal fator da suscetibilidade maior nas fêmeas em relação aos machos está relacionado as flutuações hormonais ocasionadas pela fase no ciclo estral. Por exemplo, o efeito da progesterona, secretada pelo corpo lúteo na fase do diestro, que é também o principal hormônio gestacional (CONCANNON, 2011), em que pode levar o aumento da liberação do hormônio do crescimento (GH) pelo tecido mamário. O GH estimula a proliferação e diferenciação da glândula mamária e do endométrio uterino, predispondo a neoplasias mamaria e hiperplasia endometrial cística e até a ocorrência de piometra, além de levar a acromegalia causar resistência insulínica. A progesterona interfere na ligação da insulina ao receptor e diminuindo o transporte de glicose nos tecidos alvos, adicionado ao efeito do GH, atuando também nas vias sinalização intracelular da insulina (DOMINICI et al., 2005; PÖPPL et al., 2021).
Alguns fatores do ciclo estral que interfere na sensibilidade / resistência insulínica ainda não poucos estudos na medicina veterinária, como por exemplo o efeito do estrogênio, o que se observa que cadelas com DM em insulinoterapia apresentam mal controle durante o proestro (PÖPPL et al., 2024), fase do ciclo em que aumentam devido a atividade folicular (CONCANNON, 2011).
Ademais Barros et al. (2006) demonstram em experimentos com ratos o papel inibitório dos estrógenos sobre os transportadores de glicose dependentes de insulina (GLUT-4). Porém ainda há contradição, pois apesar observar quadros de resistência à insulina em mulheres, como no final da gravidez ou na síndrome dos ovários policísticos, alegam-se que os estrogênios têm efeitos protetores sequenciais em tecidos-alvo da insulina e em outros órgãos na pós-menopausa (PAOLI, ZAKHARIA, WERSTUCK, 2021; TAO, CHENG, 2023).
Diferentes estudos destacam o papel protetor dos estrogênios na saúde metabólica das mulheres, especificamente em relação à distribuição da massa de gordura corporal, mobilização de ácidos graxos, bem como a resposta à glicose pelos vários tecidos e órgãos sensíveis à glicose (ADEYANJU et al., 2018), as reduções no estrogênio podem impactar significativamente o metabolismo energético e a homeostase metabólica geral (PAOLI, ZAKHARIA, WERSTUCK, 2021). Há muitas evidências de que o estrogênio modula a sensibilidade à insulina e está envolvido na homeostase da glicose (GODSLAND, 2005).
Dentro da população canina diabética, algumas raças são muito mais representadas do que outras, embora as predisposições de raça relatadas variem entre os países. Raças como o Terrier Australiano, o Samoieda, o Schnauzer Miniatura (FALL et al., 2007; HEELEY et al., 2020; YOON et al., 2020), Yorkshire (CATHPOLE et al.,2019) apresentam risco aumentado em múltiplos estudos; enquanto o Boxer, o Golden Retriever e o Pastor Alemão são consistentemente relatados como tendo menor risco (DAVISON, HERRTAGE, CATCHPOLE, 2005; CATHPOLE et al., 2013; MATTIN et al., 2014; YOON et al., 2020). Essas aparentes predisposições raciais podem sugerir o componente genético na etiologia da DM canina, atuando em combinação com fatores ambientais (DENYER et al., 2025).
Heeley et al. (2020) realizou estudo de os fatores associados ao risco de cães desenvolverem DM. Neste trabalhou compararam 409 cães de clínicas de atendimento primário do Reino Unido diagnosticados com DM em 2016, com 818 cães sem DM. Os cães com maior probabilidade de serem diagnosticados com DM incluíam aqueles com mais de 8 anos, fêmeas não castradas, machos castrados, Border Terriers, West Highland White Terriers, aqueles que já haviam feito uso de glicocorticoides (esteroides) e aqueles com outras condições de saúde, como obesidade, pancreatite ou hiperadrenocorticismo. Por outro lado, Staffordshire Bull Terriers, Shih-tzus e Pastores Alemães apresentaram menor probabilidade de desenvolver DM.
Assim como a obesidade tem sido associada tanto ao diabetes mellitus tipo 2 (DM2) em humanos quanto ao diabetes em felinos (NELSON, REUSCH, 2014), mas em caninos há evidências limitadas sobre o papel da obesidade no desenvolvimento de DM (HOENIG, 2014, GILOR et al., 2016). Em cães a ocorrência tem sido relacionado a comorbidades como hipercortisolismo, infecções do trato urinário (ITU), dermatite, otite, pancreatite e hipotireoidismo (HESS, KASS, WARD, 2000; DAVISON, HERRTAGE, CATCHPOLE, 2005; HUME, DROBATZ, HESS, 2006; MATTIN et al., 2014).
No caso, o hipercortisolismo é uma das endocrinopatias mais comumente associada ao DM (HESS, KASS, WARD, 2000; BLOIS et al., 2011; MICELI, PIGNATARO, CASTILLO, 2017) e foi identificado como um fator de risco (FALL et al., 2007; MATTIN et al., 2014), que provavelmente está relacionado ao antagonismo do cortisol à insulina.
Diante dos fatores supracitados, espera-se que o paciente diabético, seguindo as recomendações do Guideline, deva ser avaliado a saúde geral do animal (histórico, incluindo dieta e medicamentos em uso, e um exame físico completo), além de investigar quaisquer complicações que possam estar associadas à doença (por exemplo, catarata em cães, neuropatia periférica em gatos), outros problemas concomitantes frequentemente associados à doença (por exemplo, infecções do trato urinário, pancreatite), e quaisquer condições que possam interferir na resposta do paciente ao tratamento (por exemplo, hipertireoidismo, doença renal, hiperadrenocorticismo) e por fim avaliar os fatores de risco como obesidade, pancreatite, doença resistente à insulina, medicamentos diabetogênicos e diestro em cadelas (BEHREND et al., 2022; NIESSEN et al., 2022).
Conforme mencionado anterior o tratamento da DM consiste na insulinoterapia, a demais com ajustes na dieta, com intuito de manter a glicemia abaixo do limiar renal o máximo de tempo possível em 24 horas, com melhoria dos sinais clínicos e evitar a hipoglicemia clinicamente significativa (BEHREND et al., 2022).
3. METODOLOGIA
Realizou-se um relato de caso de um paciente canino diagnosticado com Diabetes Mellitus, atendido em um serviço especializado de endocrinologia no município de Mogi das Cruzes – SP. O atendimento foi conduzido pela Médica Veterinária Audrey de Cássia Lirio da Silveira Ramos, especialista em Endocrinologia e Metabologia de Cães e Gatos, no Núcleo de Endocrinologia e Especialidades Veterinárias.
4. RESULTADOS E DISCUSSÕES
Um canino, Lhasa apso, macho, castrado, 7 anos (na data do diagnóstico), nascido em 10/05/2015, denominado de Bido Antonio, com diagnóstico de DM desde agosto 2022, sendo acompanhado pela a Médica Veterinária Audrey a partir de fevereiro/2023.
A idade ao diagnóstico do paciente está na faixa etária mencionada por alguns autores da prevalência entre 7 e 9 anos (GRECO, 2001a) e entre 10 e 15 anos (GUPTILL, GLICKMAN, GLICKMAN, 2003), pico de 10 anos (PÖPPL, GONZALEZ, 2005). Ainda os estudos revelam também um maior risco de diabetes em cães castrados, quando comparados com cães inteiros (MATTIN et al., 2014, YOON et al, 2020).
O paciente, na primeira avaliação, realizada em 06/02/23, com peso de 11,8 kg, apresentava queixa de hipertensão em tratamento, além de catarata, ao diagnóstico apresentava poliúria, polidipsia, polifagia e fazia uso de alimentação natural monitorada por profissionais (nutrólogo) em virtude do apetite seletivo.
Os sinais clínicos de DM apresentado pelo paciente concordam com os citados por outros autores, referem a polidipsia em 96% dos casos, poliúria em 77%, e polifagia em 19% dos casos (GRECO, 2001b). No trabalho de avaliação dos aspectos epidemiológicos e clínicos-laboratoriais encontrou a poliúria como sinal clínico mais frequente, porém a catarata também aparece como sinal que levou o responsável à procura do veterinário em 21% dos casos (PÖPPL, GONZALEZ, 2005).
No exame físico observou Escore de Condição Corporal (ECC) em torno de 7 (na escala de 0 a 9) e sem perda de massa muscular, a pressão arterial de 150 mmHg e glicemia no momento da consulta de 96 mg/dL. A conduta clínica foi manter a prescrição do tratamento para a hipertensão (Enalapril 0,4 mg/kg a cada 12 horas) e manter a dose da insulina glargina já utilizada: 12 U (1,01 UI/kg) de 6:30 hs e 10 UI (0,85 UI/kg) as 18:30 e adicionado ômega 3 (1000 mg) 2 cápsula ao dia, mantido a alimentação com acompanhamento do nutrólogo para adequações e ajustes necessários na dieta para pacientes diabéticos.
O ECC é baseado na inspeção e palpação do paciente, o qual emprega escalas de um à nove, para diminuir a subjetividade (LAFLAMME, 1997). Segundo LAFLAMME (2006) na classificação do ECC, cada ponto equivale aproximadamente ao aumento de 10% a 15% do peso corporal, ou seja, um cão com ECC 7 encontra-se de 20% a 30% mais pesado em relação ao seu peso ideal. O ECC também possibilita estimar a porcentagem de gordura (%GC), ECC 5= 17 % em machos e 20 % com fêmeas, ECC 6= 22 % em machos e 26 % com fêmeas, ECC 7= 26 % em machos e 31 % com fêmeas, ECC 8= 31 % em machos e 37 % com fêmeas, e ECC 9= 35 % em machos e 43 % com fêmeas.
Há trabalhos em humanos que apontam a resistência insulínica está intimamente associada á obesidade e hipertensão (LIANG, KOYA, 2010; LAAKSO, KUUSITO, 2014), fatores esses em que o paciente apresenta sobrepeso com 20% a 30% acima do peso ideal e em terapia para hipertensão arterial.
Ainda no atendimento, foram solicitados a realização de exames laboratoriais, como hemograma, dosagem bioquímica, eletrolítica, TSH e T4 livre, urinálise, exames ultrassonográficos da região cervical, com os resultados demonstrados a seguir. Justifica-se essa investigação, pois em conformidade ao consenso de DM, o paciente com DM deve ter a saúde geral avaliada (histórico, incluindo dieta e medicamentos em uso, e um exame físico completo), além de investigar quaisquer complicações que possam estar associadas à doença (por exemplo, catarata em cães, neuropatia periférica em gatos), outros problemas concomitantes frequentemente associados à doença (por exemplo, infecções do trato urinário, pancreatite), e quaisquer condições que possam interferir na resposta do paciente ao tratamento (por exemplo, hipertireoidismo, doença renal, hiperadrenocorticismo) e por fim avaliar os fatores de risco como obesidade, pancreatite, doença resistente à insulina, medicamentos diabetogênicos (BEHREND et al., 2022; NIESSEN et al., 2022).
O hemograma com os valores na normalidade esperada pela espécie conforme mostra na figura 1) em acordo com Nelson (2015), assim como a creatinina (0,52 mg/dL, com valores de referência 0,6 a 1,8 mg/dL), ureia (39 mg/dL, com valores de referência 10 a 54 mg/dL), colesterol total (269 mg/dL, com valores de referência 108 a 270 mg/dL), triglicérides (74 mg/dL, com valores de referência 20 a 112 mg/dL), ALT (36 mg/dL, com valores de referência 10 a 88 mg/dL), fósforo (4,26 mg/dL, com valores de referência 2,4 a 6,2 mg/dL) nos valores de normalidade, albumina aumentada (4,12 g/dL com valores de referência de 2,1 a 3,8), fosfatase alcalina elevada (429 UI/L com valores de referência de 10 a 156 UI/L).
A prevalência e a gravidade das anormalidades identificadas no painel bioquímico sérico dependem da duração do diabetes não tratado e da presença de doenças concomitantes, (HESS et al., 2000). O painel bioquímico sérico geralmente não apresenta alterações significativas em cães diabéticos sem doenças concomitantes importantes, além de hiperglicemia e hipercolesterolemia. As concentrações de ureia no sangue (BUN) e creatinina sérica geralmente são normais em diabéticos sem complicações. As anormalidades mais comuns são o aumento da atividade da alanina aminotransferase e da fosfatase alcalina séricas e a hipercolesterolemia. Níveis séricos de fosfatase alcalina superiores a 800 U/L devem levantar suspeita de hipercortisolismo concomitante (NELSON, 2015)
Os eletrólitos também dentro da normalidade, cálcio iônico (1,16 mmol/L com valores de referência 1,12 – 1,4 mmol/L), sódio (146,9 mmol/L com valores de referência 139 – 150 mmol/L), potássio (4,5 mmol/L com valores de referência 3,5 – 5,4 mmol/L), cloreto (115,1 mmol/L com valores de referência 108,0 – 120,0 mmol/L). Na urinálise densidade urinária de 1,047 (1,035 a 1,045), sem outras alterações, incluindo ausência de glicosúria.
As principais alterações laboratoriais associadas ao diabetes canino manifestam-se na urina e na composição química do sangue. O aumento do volume urinário é uma consequência da diurese osmótica induzida pela hiperglicemia (NICHOLS, 2001). A densidade urinária em cães diabéticos frequentemente excede 1.025, um achado atribuível à glicosúria e proteinúria (NELSON, 2015). Além disso, a ausência persistente de glicosúria em pacientes sob terapia insulínica pode sinalizar um risco iminente de hipoglicemia (WHITLEY, DROBATZ, PANCIERA, 1997).
A avaliação dos hormônios tireoidianos encontrou valores dentro da normalidade, descartando, nesse momento, hipotireodismo associado ao DM, T4 livre por diálise com valor de 1,83 (Valores de referência de 0,82 a 3,65 ng/dL, metodologia radioimunoensaio) e o TSH 0,09 (0,1 a 0,6 ng/mL, pela metodologia quimioluminescência). Quanto a avaliação da tireóide é importante no paciente diabético pois está descrito que tanto o hipotiroidismo como o hipertiroidismo podem causar uma significativa insulinorresistência (BEHREND et al., 2022; NIESSEN et al., 2022).
A ultrassonografia da região cervical foi realizada com o objetivo de avaliar principalmente a glândula tireoide quanto ao aspecto, volume e estruturas, apresentaram sem alterações evidentes, com os lobos da tireoide com aspecto fusiforme e contornos definidos, predominantemente homogêneo, com medidas no lobo esquerdo 2,32cm X 0,47cm X 0,51cm / Volume:0,291cm ³, e lobo direito 1,78/2,08cm X 0,41cm X 0,46cm / Volume: 0,175cm ³ Volume glandular total:0,466cm ³. Paratireóides em suas topografias habituais, sendo duas externas do lado direito, formatos ovaladas, hipoecogênicas e homogêneos, medindo cerca de 0,43cm x 0,21cm e 0,22cm x 0,21cm de dimensões do lado direito e 0,26cm x 0,19cm e 0,22cm x 0,18cm de dimensões do lado esquerdo. Artérias carótidas comuns: Esquerda: medindo em torno de 0,29cm x 0,26cm de diâmetro, paredes e lúmen preservados. Direita: medindo em torno de 0,27cm x 0,25cm de diâmetro, paredes e lúmen preservados. Proporção área tireoide/ área ACC:- Direita: 14,85mm²/ 5,31mm² =2,79- Esquerda: 18,84mm²/ 5,93mm² =3,17 Razão tireoide/ACC:2,98 (Normal >1,12).
Figura 1. Hemograma do paciente Bido Antônio realizado no dia 08.02.23

Em abril/23 o paciente foi submetido a cirurgia de catarata, sendo uma consequência que possa estar associados ao paciente com DM (BEHREND et al., 2022; NIESSEN et al., 2022). Como demonstra o estudo retrospectivo de cataratas em 132 cães diabéticos, reportou a presença das de 14% dos animais apresentavam catarata no momento do diagnóstico de DM; cerca de 50% dos animais desenvolveram catarata diabética 170 dias após o diagnóstico e 80% dos animais, 470 dias após o diagnóstico (BEAM, CORREA, DAVIDSON, 1999).
O desenvolvimento de cataratas diabéticas deve-se as alteração nas relações osmóticas do cristalino induzida pela acumulação intracelular de sorbitol. Em condições de hiperglicemia, a enzima aldose redutase converte o excesso de glicose em sorbitol, um álcool de açúcar que não atravessa facilmente as membranas celulares, o acúmulo no cristalino dessa substância aumenta a osmolaridade intracelular, causando um influxo de água para o cristalino, levando a um edema e rutura das fibras, desenvolvendo-se assim as cataratas (RICHTER, GUSCETTI, SPIESS, 2002; THORNE et al., 2024).
Após o procedimento cirúrgico, tornou-se necessário ajustar a dose da insulina glargina em razão do pós-operatório e do uso de glicocorticoide oral, fazendo uso de 13 UI BID (peso 11,9 kg) e com a glicemia acima de 350 fazer uso de 2 UI insulina regular, com média de 2 a 3 aplicações ao longo do dia, com recuperação em maio/23 mantido 12 UI de insulina glargina e suspenso a regular, com peso 11,8 kg, também foi solicitado avaliação ultrassonográfica abdominal.
O uso de corticoides é indicado em algumas situações clínicas; contudo, trata-se de substâncias contrarreguladoras da ação da insulina, sendo consideradas medicamentos diabetogênico (BEHREND et al., 2022; NIESSEN et al., 2022), está relacionado ao antagonismo do cortisol à insulina. Outrossim a utilização desse medicamento aumenta duas vezes a probabilidade de o cão desenvolver DM em animais não diabéticos (CAMPBEL, LATIMER, 1984).
Em maio/23 realizou-se a avaliação ultrassonográfica, com as descrições a seguir.
O fígado apresentava dimensões preservadas, contornos regulares, bordos afilados, ecogenicidade normal e ecotextura homogênea, exceto por uma área ovalada, bem delimitada e ecogênica e homogênea medindo cerca de 0,50cm x 0,32cm em topografia de lobo quadrado. Conforme a literatura as principais alterações ultrassonográficas descritas são o aumento da ecogenicidade hepática (muitas vezes acompanhada de hiperatenuação, a hepatopatia vacuolar é uma das afecções que provoca esta hiperecogenicidade hepática encontrada em situações de HAC ou outra endocrinopatia. A hepatomegalia é comum em situações de doença metabólica como HAC, hipotiroidismo e DM (MATTON, NYLAND, 2015), em contraste o paciente não apresentava aumento do fígado, apenas com áreas ovaladas (pode estar relacionada com área de fibrose e/ou hiperplasia).
A vesícula biliar repleta por conteúdo anecogênico e ecogênico amorfo em suspensão e depositado, não formador de sombreamento acústico posterior, com paredes finas e lisas sugerindo lama biliar tipo 4. Em concordância aos sinais ultrassonográficos mais frequentemente descritos na literatura foram distensão ligeira a moderada (31%) e presença de sedimento ligeiro a moderado (41,4%) (COELHO, 2023). Foi prescrito ácido ursodesoxicólico 150 mg SID por 3 meses, para tratamento da lama biliar.
Pâncreas com dimensões preservadas em ramo esquerdo, porém pouco aumentadas em corpo e ramo direito, medindo cerca de 1,03cm em ramo direito, 0,87-1,10cm em corpo e 0,84cm em ramo direito de espessura, ecotextura grosseira e ecogenicidade elevada em corpo e ecogenicidade mista em ramo direito e ramo esquerdo, nota-se ao menos uma área ovalada, bem delimitada, hipoecogênica e homogênea em região de transição entre corpo e ramo direito medindo cerca de 0,79cm x 0,45cm (comprimento x altura), sugerindo hiperplasia nodular e pancreatopatia crônica/ lesão antiga e/ou infiltrado fibroadiposo.
Devido à pancreatite muitas vezes associada a diabetes, alterações ultrassonográficas em pâncreas são também comuns. No entanto, a pancreatite nem sempre provoca suficientes alterações pancreáticas que permitam a sua deteção através da ultrassonografia (MATTON, NYLAND, 2015). Quanto ao pâncreas, os sinais ultrassonográficos mais frequentemente visualizados foram aumento do tamanho do órgão (34,5%) e parênquima difusamente heterogêneo em estrutura e/ou ecogenicidade (24,1%) (COELHO 2023).
Rins simétricos, em topografia habitual, contornos regulares e dimensões normais. Em estudo dos sinais ultrassonográficos em cães diabetéticos os sinais mais vezes descritos foram hiperecogenicidade difusa, perda de diferenciação corticomedular, pielectasia e presença de estruturas mineralizadas (COELHO 2023).
As adrenais simétricas com dimensões pouco aumentadas em polo caudal de adrenal esquerda (AE: 1,92cm x 0,58cm e AD: 2,29cm x 0,48cm – comprimento x polo caudal), em polo caudal de adrenal esquerda onde observa-se uma área parcialmente definida, tendendo a ovalada, ecogenicidade pouco elevada e ecotextura homogênea medindo cerca de 0,61cm x 0,37cm (comprimento x altura). Ademais, a diabetes pode estar associada a afeções como síndrome de cushing, sinais ultrassonográficos como adrenomegalia bilateral ou unilateral, lesões císticas ou nodulares e massas nas adrenais podem também estar presentes (MATTON, NYLAND, 2015).
Adicionalmente, da mesma forma, além do uso os corticosteroides exógenos e o paciente apresenta aumento da glândula adrenal esquerda, por isso a importância na investigação do aumento da produção de corticóides endógenos, pois tanto o corticoide exógeno quanto o endógeno antagonizam a ação da insulina (NIESSEN et al., 2022), considerado o hipercortisolismo um fator de risco potencial para o desenvolvimento de DM (MATTIN et al., 2014), aumenta a gliconeogênese e pode causar resistência à insulina (GILOR e GRAVES 2011).
Em julho/23 paciente apresentou lambedura e prurido nas patas, tratado por médico veterinário especializado em dermatologia que solicitou análise citológica da pele, com discreta quantidade de queratina e poucas estruturas leveduriformes compatíveis com Malassezia sp., não foram observadas bactérias ou células inflamatórias, prescrito cytopoint e apoquel, e mantido a prescrição da insulina de 12 UI BID.
Em outubro/23 fez reavaliação da ultrassonografia após 3 meses do uso do ácido ursodesoxicólico, com melhoria do nódulos no fígado, e a vesícula biliar preenchida com discreta quantidade de conteúdo ecogênico depositado, as adrenais simétricas, tópicas apresentando formato bilobado, contornos regulares, ecogenicidade pouco aumentada, ecotextura preservada, no parênquima e dimensões preservadas (AE: 1,87cm x 0,65cm x 0,29cm; AD: 1,99cm x 0,37cm x 0,34cm – comprimento x polo caudal x polo cranial).
Em janeiro e março/24 reavaliação e na ocasião foi mantido a prescrição da insulina glargina de 12 UI BID (peso de 11,9 kg), e nesse período fez uso de corticoide oral prednisona 2,5 mg SID por 4 dias para auxílio no controle da alergia nas patas, refez exame de urinálise em fev/24, apresentando densidade urinaria maior que 1,050 (Valores de referência 1,015 a 1,045) e glicosúria 3 cruzes e na cultura bacteriana, não apresentando crescimento, solicitado também avaliação laboratoriais.
Em março/24 fez avaliação ultrassonográfica abdominal apresentando vesícula biliar moderadamente repleta por conteúdo anecogênico e por moderada quantidade de conteúdo ecogênico em suspensão, baço com presença de estrutura de limites pouco definidos, hipoecogênica e pouco grosseira em face parietal de corpo esplênico, medindo cerca de 0,87cm x 0,83cm – Pode estar relacionado com hiperplasia nodular. Em relação ao baço, as alterações ultrassonográficas descritas foram esporádicas, sendo que o sinal mais frequentemente foi o aumento do tamanho do órgão (17,2%) (COELHO 2023).
As adrenais simétricas parênquima grosseiro, com presença de estrutura amorfa, ecogênica e homogênea, medindo cerca de 1,03cm x 0,72cm entre polo cranial e caudal de adrenal esquerda, dimensões aumentadas em adrenal esquerda (AE: 2,05cm x 0,70cm x 0,48cm; AD: 1,96cm x 0,33cm x 0,33cm – comprimento x polo caudal x polo cranial). Pâncreas parcialmente caracterizado, apresentando dimensões habituais (até 0,82cm em ramo esquerdo/ até 0,87cm em corpo/ até 0,93cm em ramo direito), contornos regulares, ecogenicidade elevada e ecotextura pouco grosseira.
Em abril/24 o exame de hemograma apresentava uma discreta linfopenia (918 valores de ref. 1.000 a 6.400), conforme demonstra na figura 2. Os valores da avaliação bioquímica na normalidade esperada pela espécie, como proteína total (7,09 g/dL com valores de referência de 5,7 a 7,1 g/dL), albumina (3,47 g/dL com valores de referência de 2,1 a 3,8 g/dL), globulina (3,62 g/dL com valores de referência de 2,7 a 4,4 g/dL), bilirrubina total (0,44 mg/dL com valores de referência de 0,10 a 0,70 mg/dL), bilirrubina direta (0,36 mg/dL com valores de referência de 0,06 a 0,30 mg/dL), bilirrubina indireta (0,08 mg/dL com valores de referência de 0,01 a 0,50 mg/dL), a creatinina (0,63 mg/dL, com valores de referência 0,5 a 1,6 mg/dL), ureia (43,13 mg/dL, com valores de referência 10 a 54 mg/dL), fósforo (3,68 mg/dL, com valores de referência 2,4 a 6,2 mg/dL) GGT (5 UI/L com valores de referência de 1 a 10 UI/L), AST (28 UI/L com valores de referência de 10 a 88 UI/L), ALT (41 mg/dL, com valores de referência 10 a 88 mg/dL), triglicérides (80,8 mg/dL, com valores de referência 20 a 112 mg/dL). Com valores aumentados colesterol total (300 mg/dL, com valores de referência 108 a 270 mg/dL), fosfatase alcalina elevada (903 UI/L com valores de referência de 10 a 156 UI/L).
A concentração sérica de colesterol e triglicérides está normalmente aumentada em animais diagnosticados com DM. A insulina é um agente inibidor da lipólise e da oxidação dos ácidos graxos livres. Deste modo, ao haver deficiência em insulina: i) a atividade da lipoproteína lipase está reduzida; ii) a lipase sensível está ativada; iii) a produção hepática de triglicéridos de lipoproteína de muito baixa densidade (VLDL, do inglês very-low-density lipoprotein) está aumentada; e iv) a depuração de VLDL está diminuída. O aumento das concentrações de colesterol intrahepático suprime os receptores das lipoproteínas de baixa densidade (LDL, do inglês lowdensity lipoprotein) nos hepatócitos, reduzindo consequentemente a depuração das partículas de LDL e de lipoproteínas de alta densidade (HDL, do inglês high-density lipoprotein) em circulação, provocando, por fim, hipercolesterolemia (NELSON, 2015)
Figura 2. Hemograma do paciente Bido Antônio realizado no dia 01.04.24

Em novembro/24 realizado os exames hemograma apresentava uma discreta linfopenia (747 valores de ref. 800 a 4.100), conforme demonstra na figura 3.
Os valores da avaliação bioquímica na normalidade esperada pela espécie, a creatinina (0,87 mg/dL, com valores de referência 0,5 a 1,6 mg/dL), ureia (55,31 mg/dL, com valores de referência 10 a 54 mg/dL), ALT (48,26 mg/dL, com valores de referência 10 a 88 mg/dL), fósforo (2,43 mg/dL, com valores de referência 1,9 a 7,9 mg/dL), cálcio total (10,82 mg/dL, com valores de referência 8,8 a 11,9 mg/dL), cálcio iônico (1,28 mmol/L, com valores de referência 1,12 a 1,40 mmol/L) triglicérides (59,42 mg/dL, com valores de referência 20 a 160 mg/dL). Com valores aumentados colesterol total (306,56 mg/dL, com valores de referência 116 a 300 mg/dL), fosfatase alcalina elevada (1318,18 UI/L com valores de referência de 10 a 156 UI/L), albumina (4,07 g/dL com valores de referência de 2,3 a 3,8 g/dL).
Figura 3. Hemograma do paciente Bido Antonio realizado no dia 27.11.24

A ultrassonografia realizada em novembro/24 mostrou fígado com dimensões pouco aumentadas, bordos arredondados e pequenas estruturas nodulares ecogênicas e homogêneas, uma delas medindo aproximadamente 0,60 cm × 0,46 cm. A vesícula biliar encontrava-se moderadamente repleta por conteúdo anecogênico e acentuada quantidade de material ecogênico em suspensão (lama biliar tipo 4), com paredes finas e regulares. Baço de dimensões preservadas, presença de estrutura de limites pouco definidos, ecogênica e grosseira em face parietal de corpo esplênico, medindo cerca de 0,94cm x 1,21cm. As adrenais simétricas, tópicas apresentando formato bilobado, contornos regulares, ecogenicidade elevada em adrenal esquerda, parênquima grosseiro em adrenal esquerda e dimensões aumentadas em adrenal esquerda (AE: 2,19cm x 1,03cm x 0,60cm; AD: 1,51cm x 0,34cm x 0,29cm – comprimento x polo caudal x polo cranial). Pâncreas parcialmente caracterizado, apresentando dimensões habituais (até 0,78cm em ramo esquerdo/ até 0,92cm em ramo direito), com aparente estrutura arredondada, hipoecogênica e homogênea, medindo cerca de 0,96cm x 0,92cm em ramo direito.
Em dezembro/24, houve reajuste da dose da insulina glargina 15 UI pela manhã e 12 UI a noite (peso 12 kg) e a urinalise foi refeita e apresentou como resultado a densidade urinária de 1,044 (1,015 a 1,045) e glicosúria de 4 cruzes.
Em Abril/25 intenso prurido nas pastas, prescrito prelone (3mg/mL – 2 ml), com histórico das glicemias de 383mm/dL em 27/4 às 12 h e 417 28/4 as 14:30, aferidos em glicosímetro free style optium neo, Lantus 17 manha e 15 U a noite, insulina regular 1U se a glicemia maior que 350.
Em maio/25 teve melhora do prurido das patas e realizou profilaxia dentária e remoção neoformações no plano nasal, nos membros posteriores esquerdo e direito e na lateral do tórax, fez uso de corticóide devido ao procedimento cirúrgico de retirada das neoformações, com uso de 3 UI insulina regular 3 ao vezes ao dia, com reajuste da lantus 17 UI de BID, com não medição pelo sensor (marcado HI), figura 4 e 5 demonstra as médias diárias das glicemias aferidas pelo sensor no mês maio/25
Figura 4: Curva glicêmica dos dias 24 e 26 de maio/2025.
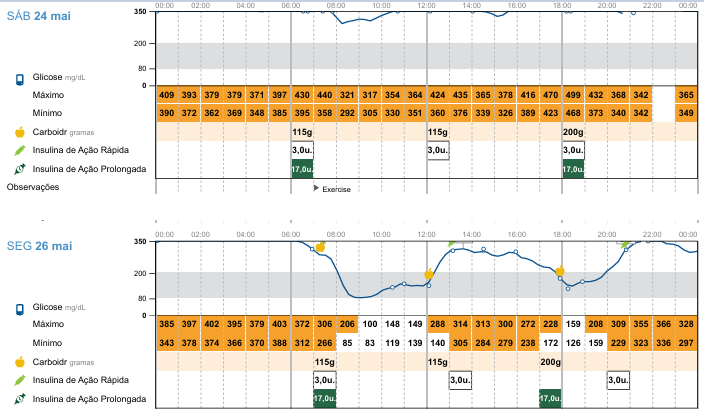
Figura 5. Resumo mensal das médias diárias de glicemias no período de 01 a 31 de maio/25.

Em Junho/25 no inicio do mês, optou-se pela troca da insulina glargina para a Insulina Caninsulin® 40 UI/ml, com 42 UI BID e 4 UI de insulina regular 3 vezes ao dia quando glicemia superior a 350 mg/dL (período da manhã, tarde e à noite), com glicemia no momento da consulta de 307 mg/dL, com ajuste de dose no final de junho para 48 UI BID de insulina Caninsulin® e 4UI de regular a cada 2 horas se a glicemia maior que 350, figura 6 demonstra as médias diárias das glicemias aferidas pelo sensor no mês junho/25.
Behrend et al. (2018) a escolha da insulina apropriada deve considerar a duração de ação, incluindo insulinas de ação rápida, intermediária e prolongada, adequando-se às necessidades metabólicas de cada paciente. Diante da ação do não controle glicêmico optou-se pela troca da insulina glargina pela Caninsulin® para o paciente.
Figura 6: Resumo mensal das médias diárias de glicemias no período de 01 a 30 de junho/25.

Em Julho/25, foi realizado ajuste de dose para 50 UI BID de Caninsulin®, além de 5UI de insulina regular caso a glicemia estivesse acima de 350, e solicitado teste de estimulação e avaliação de tireoide. A dosagem do T4 total pelo método radioimunoensaio 2,07 (valores de referência 1,25 a 3,90 µg/dL) e TSH pelo método quimioluminescência de 0,14 (0,10 a 0,60 ng/mL). A dosagem de cortisol basal metodologia Radioimunoensaio de 2,06 (ref 1,0 a 4,6 µg/dL) e o cortisol pós ACTH de 15,43 (ref 5,0 a 17,0 µg/dL).
Os demais exames aumentados de GGT (9,22 UI/L, com valores de referência 1,2 a 6,4 UI/L) e Fosfatase alcalina (1616,4 UI/L, com valores de referência 15,0 a 80 UI/L), e dos demais dentro da normalidade como o colesterol total (261,05 mg/dL, com valores de referência 135 a 270 mg/dL), triglicérides (54,0 mg/dL, com valores de referência 32 a 125 mg/dL), bilirrubina total (0,30 mg/dL com valores de referência de 0,10 a 0,60 mg/dL), bilirrubina direta (0,14 mg/dL com valores de referência de 0,10 a 0,30 mg/dL), bilirrubina indireta (0,16 mg/dL com valores de referência de 0,01 a 0,30 mg/dL). Os eletrólitos dentro da normalidade para os valores de referência utilizados pelo laboratório, potássio (4,22 mmol/L com valores de referência 4,1 – 5,4 mmol/L), sódio (149,09 mmol/L com valores de referência 143 – 150 mmol/L).
Em agosto/25 foi trocado a insulina Caninsulin® para a Tresiba, com 20 UI BID e 3 UI de insulina regular se a glicemia maior que 350, com ajuste de dose para 22 UI BID. Durante a consulta foi mencionado que a tutora faz reposição hormonal tópica de estrogênio desde abril/25, motivando a solicitação da dosagem do estradiol no paciente e orientado a tutora a mudar o local de aplicação do gel no antebraço para a parte de traz das costas, a dosagem do estrogênio, pelo método radioimunoensaio, com 71,45 (referência para macho castrado é de 23,10 a 65,1 pg/mL).
Em setembro/25, após a mudança da utilização da reposição hormonal tópica da responsável, a glicemia do paciente melhorou apenas com insulina Tresiba 23 UI BID, sem a necessidade da associação com a insulina regular.
Esse conjunto de fatores justifica a dificuldade de controle na glicemia, pois os estudos apontam que incidência de DM é maior em fêmeas, cerca de 70% (FLEEMAN, RAND, 2001), e 95% (CATCHPOLE et al., 2005, PÖPPL, GONZÁLEZ, 2005) do que em machos, pois a flutuação hormonal (COUSINS, 1991) interfere: na sinalização da insulina ao receptor (RYAN, ENNS, 1988, RAND et al., 2004), no transporte de glicose e na captação pelo tecido adiposo (RYAN, ENNS, 1988). Explica-se que os fatores do ciclo estral possam ter impacto, como o estradiol, que é o principal marcador hormonal na fase estrogênica, principalmente no pró-estro e reduz durante o estro (HOFFMANN, RIESENBECK, KLEIN, 1996, OLIVEIRA, MARQUES JUNIOR, NEVES, 2003, RODRIGUES, RODRIGUES, 2002). Em experimentos em ratos demonstrou o papel inibitório dos estrógenos sobre os transportadores de glicose dependentes de insulina (GLUT-4) (GODSLAND, 2005, BARROS et al., 2006).
Em humanos o efeito mais consistente dos contraceptivos orais e da terapia de reposição hormonal com estrogênio é a redução da glicemia de jejum e o agravamento da tolerância à glicose (ZHANG et al., 2002; MARGOLIS et al., 2004), ou seja, a deficiência de estrogênio está associada a uma deterioração relativamente pequena na tolerância à glicose e a um aumento da resistência à insulina (GODSLAND, 1996). Em contraste, o excesso de estrogênio está associado à deterioração da tolerância à glicose e à resistência à insulina (GONZALEZ et al., 2002).
No entanto, algumas cadelas diabéticas em tratamento com insulina podem apresentar diabetes mal controlada durante o proestro. Nessa fase, há um efeito predominante do estrogênio. Os níveis basais de estrogênio do anestro (5-15 pg/mL) aumentam progressivamente durante o proestro devido à atividade folicular e podem atingir níveis de platô acima de 60-70 pg/mL dias antes do estro (CONCANNON, 2011).
Em outubro passou por tratamento de otite com corticoide, e apresentou glicemia de 400 mg/dL, e com queixa de diarreia (prescrito o tratamento com probiótico up flora e metronidazol 125 mg BID por 10 dias).
Em outubro/25 teve quadro de ceratite e úlcera no olho esquerdo que evoluindo para a necessidade de enucleação, com glicemia na consulta de 236 mg/dl, fazendo uso da insulina tresiba 23 UI BID, e solicitado novamente a dosagem do estrogênio, pelo método radioimunoensaio, com 59,80 (referência para macho castrado é de 23,10 a 65,1 pg/mL), diminuindo quando comparado com a primeira avaliação (71,45 pg/mL).
5. CONCLUSÃO/CONSIDERAÇÕES FINAIS
A análise deste caso permitiu alcançar o objetivo de identificar os fatores que dificultaram o controle glicêmico do paciente, evidenciando que múltiplos elementos contribuíram para a resistência insulínica, incluindo condições inflamatórias, uso de corticosteroides e a suspeita inicial de endocrinopatia não confirmada pelos exames hormonais.
O caso de Bido Antonio ilustra a complexidade do manejo da DM canina com resistência à insulina, a qual envolve múltiplos fatores. O relato destaca a importância da anamnese minuciosa, que deve incluir a investigação de exposição a fatores ambientais, como hormônios exógenos utilizados pelos tutores, para um manejo personalizado e eficaz da doença.
O achado mais relevante foi a interferência inesperada da reposição hormonal tópica utilizada pela tutora, que impactou diretamente a estabilidade glicêmica do animal, aspecto pouco descrito na literatura e que amplia a compreensão clínica sobre fatores externos capazes de alterar a resposta à insulina. Embora o estudo se limite a um único caso, reforça a importância de atenção a variáveis ambientais no manejo do diabetes e sugere a necessidade de pesquisas futuras que explorem de forma mais aprofundada o efeito da exposição inadvertida a hormônios tópicos em cães diabéticos.
REFERÊNCIAS
ADA (AMERICAN DIABETES ASSOCIATION). Diagnosis and classification of diabetes mellitus. Diabetes Care. v. 33, n. 1, p.62–69, 2010.
ADEYANJU, O. A. et al. Oral hormonal therapy with ethinylestradiol-levonorgestrel improves insulin resistance, obesity, and glycogen synthase kinase-3 independent of circulating mineralocorticoid in estrogen-deficient rats. Canadian Journal of Physiology and Pharmacology. v. 96, p. 577 – 586, 2018.
AHLGREN, K. M. et al. Lack of evidence for a role of islet autoimmunity in the ae tiology of canine diabetes mellitus. PLoS One. v. 9, n. 8, p.105473, 2014.
BARROS, R. P. A. et al. Muscle GLUT4 regulation by estrogen receptors Erβ and Erα. PNAS. v. 31, p.1605-1608, 2006.
BEAM, S., CORREA, M. T., DAVIDSON, M. G. A retrospective-cohort study on the development of cataracts in dogs with diabetes mellitus: 200 cases. Veterinary Ophthalmology. v. 2, n. 3, p. 169–172. 1999.
BEHREND, E. et al. AAHA Diabetes Management Guidelines for Dogs and Cats 2018. Journal of the American Animal Hospital Association. v. 54, n. 1, p. 1-21, 2022.
BLOIS, S. L. et al. Multiple endocrine diseases in dogs: 35 cases (1996-2009). Journal of the American Veterinary Medical Association. v. 238, n.12, p. 1616–21, 2011.
CAMPBELL, K. L., LATIMER, K. S. Transient diabetes mellitus associated with prednisone therapy in a dog. Journal of the American Veterinary Medical Association. v. 185, n. 3, p. 299–301, 1984.
CATCHPOLE, B. Canine diabetes mellitus: can old dogs teach us new tricks? Diabetologia. v.48, p. 1948 – 1956, 2005.
CATCHPOLE, B. et al. Canine diabetes mellitus: from phenotype to genotype. Journal Small Animal Practice. p. 4-10, 2019.
CATCHPOLE, B. et al. Genetics of canine diabetes mellitus: are the diabetes susceptibility genes identified in humans involved in breed susceptibility to diabetes mellitus in dogs? Veterinary Journal. v. 195, n. 2, p.139-47, 2013.
COELHO, C, C.P. Sinais ecográficos associados a diagnóstico de Diabetes mellitus em 29 cães, 2023. Mestrado Integrado em Medicina Veterinária. Universidade de Évora – Escola de Ciências e Tecnologia, Evora, 121 f.
CONCANNON, P. W. Reproductive cycles of the domestic bitch. Animal Reproduction Science. v. 124, p. 200 – 210, 2011.
COUSINS, L. Insulin sensitivity in pregnancy. Diabetes. v.40, p.39-43, 1991.
DAVISON, L. J. et al. Autoantibodies to GAD65 and IA-2 in canine diabetes mellitus. Autoantibodies to GAD65 and IA-2 in canine diabetes mellitus. Veterinary Immnulogu and Immunopathology. v.126, p.83-90, 2008.
DAVISON, L. J., HERRTAGE, M. E., CATCHPOLE, B. Study of 253 dogs in the United Kingdom with diabetes mellitus. Veterinary Record. v. 156, p. 467 – 471, 2005;156.
DENYER, A. L. et al. Epidemiology and clinical management of 1072 dogs with diabetes mellitus in a UK diabetes register. Companion Animal Health and Genetics. v. 12, n. 7, p. 1-16, 2025.
DENYER, A. L., CATCHPOLE, B., DAVISON, L. J. Genetics of canine diabetes mellitus part 1: phenotypes of disease. Veterinary Journal. v.270, p. 105611, 2021.
DOMINICI, F. P. et al. Influence of the crosstalk between growth hormone and insulin signaling on the modulation of insulin sensitivity. Growth Hormone & IGF Research. v. 15, p.324-336, 2005.
FALL, T. et al. Diabetes mellitus in a population of 180,000 insured dogs: incidence, survival, and breed distribution. Journal of Veterinary Internal Medicine. v. 21, p. 1209-1216, 2007.
FLEEMAN, L. M., RAND, J. S. Managament of canine diabetes. Veterinary Clinics of North America: Small Animal Practice. v.31, n.5, p.855-879, 2001.
GILOR, C. et al. What’s in a name? Classification of diabetes mellitus in veterinary medicine and why it matters. Journal of Veterinary Internal Medicine. v. 30, p. 927–940, 2016.
GILOR, C., GRAVES, T. K. Interpretation of laboratory tests for canine Cushing’s syndrome. Topics in Companion Animal Medicine. v. 26, p. 98–108, 2011.
GODSLAND, I. F. Oestrogens and insulin secretion. Diabetologia. v. 48, p. 2213–2220 2005.
GODSLAND, I. F. The influence of female sex steroids on Glucose metabolism and insulin action. Journal of Internal Medicine. v. 240, p. 1–65, 1996.
GONZALEZ, C. et al. Role of 17 beta-estradiol administration on insulin sensitivity in the rat: implications for the insulin receptor. Steroids. v. 67, p. 993–1005, 2002.
GRECO, D. S. Diagnosis and treatment of juvenile endócrine disorders in puppies and kittens. Veterinary Clinics of North America: Small Animal Practice. v. 31, p. 401-407, 2001a.
GRECO, D. S. Diagnosis of diabetes mellitus in dogs. Veterinary Clinics of North America: Small Animal Practice. v. 31, p. 844-853, 2001b.
GUPTILL, L., GLICKMAN, L., GLICKMAN, N. Time trends and risk factors for diabetes mellitus in dogs: analysis of veterinary medical data base records. The Veterinary Journal. v.165, p.240-247, 2003.
HEELEY, A. M. et al. Diabetes mellitus in dogs attending UK primary-care practices: frequency, risk, factors and survival. Canine Medicine and Genetics. v. 7, n. 6, p. 1-19. 2020.
HESS, R. S. et al. Concurrent disorders in dogs with diabetes mellitus: 221 cases (1993-1998). Journal of the American Veterinary Medical Association. v. 217, p. 1166- 1173, 2000.
HESS, R. S., KASS, P. H., WARD, C. R. Breed distribution of dogs with diabetes mellitus admitted to a tertiary care facility. Journal of the American Veterinary Medical Association. v. 216, n. 9, p.1414 – 7, 2000.
HOENIG, M. Comparative aspects of diabetes mellitus in dogs and cats. Molecular and Cellular endocrinology. v. 197, p. 221-229, 2002.
HOENIG, M. Comparative aspects of human, canine, and feline obesity and factors predicting progression to diabetes. Veterinary Sciences. v. 1, n. 2, p.121- 135, 2014.
HOFFMANN, B., RIESENBECK, A., KLEIN, R. Reproductive endocrinology of bitches. Animal Reproduction Science. v. 42, p.275-288, 1996.
HUME, D. Z., DROBATZ, K. J., HESS, R. S. Outcome of dogs with diabetic ketoacidosis: 127 dogs (1993-2003). Journal of Veterinary Internal Medicine. v. 20, p. 547–555, 2006.
LAAKSO, M., KUUSISTO, J. “Insulin resistance and hyperglycaemia in cardiovascular disease development” Nature Reviews Endocrinology. v. 10, n. 5, p. 293–302, 2014.
LAFLAMME, D. P. Development and validation of a body condition score system for dogs: a clinical tool. Canine Practice. v. 22, n. 3, p. 10- 15, 1997.
LAFLAMME, D. P. Understanding and managing obesity in dogs and cats. Veterinary Clinics Small Animal Practice. v. 36, p. 1283-1295, 2006.
LIANG, F. X., Koya, D. “Acupuncture: is it effective for treat ment of Insulin resistance?” Diabetes, Obesity and Metabolism. v. 12, n. 7, p. 555–569, 2010.
MARGOLIS, K. L. et al. Effect of oestrogen plus progestin on the incidence of diabetes in postmenopausal women: results from the Women’s Health Initiative Hormone Trial. Diabetologia. v. 47, p. 1175–1187, 2004.
MATTIN, M. J. et al. An epidemiological study of diabetes mellitus in dogs attending first opinion practice in the UK. Veterinary Record. v.174, p. 349–349, 2014.
MATTOON, J. S., NYLAND, T. G. Small Animal Diagnostic Ultrasound. 3. ed. St. Louis, Missouri : Elsevier Saunders, 2015.
MICELI, D. D., PIGNATARO, O. P., CASTILLO, V. A. Concurrent hyperadrenocorticism and diabetes mellitus in dogs. Research in Veterinary Science. v. 115, p. 425–31, 2017.
NELSON, R. W. The endocrine pancreas. In: FELDMAN, E.C. et al. Canine and feline endrocrinology. 4 ed. Missouri: Elsevier Saunders, cap.6, p.213-257, 2015.
NELSON, R. W., REUSCH, C. E. Animal models of disease: classification and etiology of diabetes in dogs and cats. Journal of Endocrinology. v. 222, n. 3, p. 1–9, 2014.
NICHOLS, R. Polyuria and polydipsia. Veterinary Clinics of North America: Small Animal Practice. v. 31, p. 833-843, 2001.
NIESSEN, S. J. M. et al. Agreeing Language in Veterinary Endocrinology (ALIVE): diabetes mellitus – a modified Delphi-method-based system to create consensus disease definitions. The Veterinary Journal. v. 289, 2022, p. 105910.
O’KELL, A. L. et al. Comparative pathogenesis of autoimmune diabetes in humans, NOD mice, and canines: has a valuable animal model of type 1 diabetes been overlooked? Diabetes. v. 66, p.1443 – 1452, 2017.
O’Kell, A. L., DAVISON, L. J. Etiology and pathophysiology of diabetes mellitus in dogs. Veterinary Clinics of North America: Small Animal Practice. v. 53, n. 3, p. 493 – 510, 2023.
OLIVEIRA, E. R. S, MARQUES JUNIOR, A. P., NEVES, M. M. Endocrinologia reprodutiva da fertilidade da cadela – revisão. Archives of Veterinary Science. v.8, n.1, p.1-12, 2003.
PAOLI, M.; ZAKHARIA, A.; WERSTUCK, G. H. The role of estrogen in insulin resistance: A review of clinical and preclinical data. The American Journal of Pathology. v. 191, n. 9, p. 1490-1498, 2021.
PÖPPL, A. G. et al. Estrus cycle, pyometra, and insulin resistant diabetes in the bitch: What is know and why it is relevant? Preprints.org. v. 1, 2024.
PÖPPL, A. G. et al. Pyometra-associated insulin resistance assessment by insulin binding assay and tyrosine kinase activity evaluation in canine muscle tissue. Domestic Animal Endocrinology. v. 76, p. 106626, 2021.
PÖPPL, A. G., GONZALEZ, F. H. D. Aspectos epidemiológicos e clínico – laboratoriais da diabetes mellitus em cães. Acta Scientiae Veterinarinariae. v.33, n.1, p.33-40, 2005.
RAND, J. S. et al. Canine and feline diabetes mellitus: nature ou nuture? The Journal of Nutrition. v.134, p.2072-2080, 2004.
RICHTER, M., GUSCETTI, F., SPIESS, B. Aldose reductase activity and glucose-related opacities in incubated lenses from dogs and cats. American Journal of Veterinary Research. v. 63, n. 11, p. 1591–1597. 2002.
RODRIGUES, B. A., ROGRIGUES, J. L. Endrocrinologia reprodutiva na cadela. Clínica Veterinária. v. 40, p.50-58, 2002.
RYAN, E. A., ENNS, L. Role of gestacional hormones in the induction of insulin resistance. Journal of Clinical Endocrinology and Metabolism. v. 67, p.341, 1988.
SAMSON, A. R. H., RAND, J., FORD, S. L. Detemir improves diabetic regulation in poorly controlled diabetic dogs with concurrent diseases. Journal of the American Veterinary Medical Association. v. 261, n. 3, 2023.
SHIELDS, E. J. et al. Extreme Beta-Cell deficiency in pancreata of dogs with canine diabetes. PLoS ONE. v. 10, p.0129809–0129809, 2015.
TAO, Z., CHENG, Z. Hormonal regulation of metabolism – recent lessons learned from insulin and estrogen. Clinical Science. v.137, p. 415 – 434, 2023.
THORNE, C. A. et al. The synergistic effects of polyol pathway-induced oxidative and osmotic stress in the aetiology of diabetic cataracts. International Journal of Molecular Sciences. v. 25, n. 16, p. 9042, 2024.
USUI, S., YASUDA, H., KOKETSU, Y. Characteristics of dogs having diabetes mellitus; analysis of data from private Japanese veterinary clinics. Veterinary Medicine and Animal Science. v. 3, n. 1, 2015.
WHITLEY, N. T., DROBATZ, K. J., PANCIERA D. L. Insulin overdose in dogs and cats: 28 cases (1986-1993). Journal of American Veterinary Medical Association. v. 211, p. 326-330, 1997.
WHO. Classification of Diabetes Mellitus. World Health Organization, Geneva. 2019.
YOON, S. et al. Epidemiological study of dogs with diabetes mellitus attending primary care veterinary clinics in Australia. Veterinary Record. v. 187, n. 3, 2020.
ZHANG, Y. et al. The effect of estrogen use on levels of glucose and insulin and the risk of type 2 diabetes in American Indian postmenopausal women: the Strong Heart Study. Diabetes Care. v. 25, p. 500–504, 2002.
1Discente do Curso de Especialização em Endocrinologia e Metabologia de Cães e Gatos Anclivepa, São Paulo, SP, Brasil. Médica Veterinária do Centro de Diagnóstico Veterinário, Pesquisa e Desenvolvimento do Vet Vida, Cuiabá, MT, Brasil. e-mail: liviatcho@hotmail.com;
2Médica Veterinária Especializada em Endocrinologia e Metabologia de Cães e Gatos Anclivepa SP, responsável pelo Núcleo de Endocrinologia e Especialidades Veterinária em Mogi das Cruzes-SP;
3Médica Veterinária, mestrando do Programa de Pós-Graduação em Ciências Veterinárias, Faculdade de Medicina Veterinária, Universidade Federal do Mato Grosso, Cuiabá, MT, Brasil;
4Médico Veterinário, Especializado em Patologia Clínica pela Anclivepa. Patologia clínico Provet Medicina Veterinária Diagnóstica e Coordenador técnico e gerente do laboratório de dosagens hormonais no Provet Medicina Veterinária Diagnóstica, São Paulo, SP, Brasil;
5Orientadora, Médica Veterinária, doutora em Patologia Clínica Veterinária pela UNESP Botucatu, SP, Brasil. DS consultoria Laboratorial Veterinária, Criciúma, SC, Brasil. E-mail:contato@danisilvano.com.br
