EFFICACY OF PROTON PUMP INHIBITORS AND THEIR ADVERSE EFFECTS IN THE TREATMENT OF GASTROESOPHAGEAL REFLUX DISEASE AND PEPTIC ULCER DISEASES: A LITERATURE REVIEW
REGISTRO DOI: 10.69849/revistaft/cl10202510181210
Ana Carolina Abati1
Bruno Luís Almeida Aranha Camargo2
Eduarda de Angelis Rubira3
Prof. Especialista Rogelio Rocha Barros4
Resumo
O presente estudo aborda a eficácia dos inibidores da bomba de prótons e seus efeitos adversos no tratamento da Doença do Refluxo Gastroesofágico e da Doença Ulcerosa Péptica. Objetivou-se revisar a literatura recente acerca das principais indicações, mecanismos de ação, benefícios, riscos e atualizações terapêuticas dos IBPs, oferecendo subsídios para a prática clínica baseada em evidências. Realizou-se uma revisão sistemática de literatura nos últimos seis anos (2020–2025), utilizando bases de dados internacionais como PubMed, Scielo e Google Acadêmico. Foram incluídos estudos completos relacionados ao tema, enquanto trabalhos duplicados ou com informações insuficientes foram excluídos. Os artigos selecionados foram avaliados quanto a autores, ano de publicação, objetivos, resultados e conclusões e dados extraídos de forma qualitativa. Os IBPs demonstraram elevada eficácia no manejo da DRGE e da DUP, promovendo supressão ácida sustentada, cicatrização mucosa, alívio sintomático e redução de complicações, incluindo hemorragias digestivas e recidivas ulcerosas. Para DRGE, alcançam cicatrização mucosa entre 75% e 95% em oito semanas, com melhora sintomática em 60–85% dos casos. Na DUP, a terapia com IBPs combinada à erradicação do Helicobacter pylori reduz significativamente recidivas e necessidade de intervenções cirúrgicas. Entre os efeitos adversos observados, destacam-se deficiência de vitamina B12, redução da absorção de cálcio, aumento do risco de fraturas, infecções gastrointestinais e possíveis eventos cardiovasculares, principalmente em uso prolongado. Novas terapias, como fexuprazano e alginatos, apresentam eficácia superior em DRGE refratária e refluxo noturno. Os IBPs continuam sendo a primeira linha no tratamento da DRGE e DUP, com comprovada eficácia clínica. Entretanto, a atenção aos efeitos adversos e à necessidade de terapias complementares é fundamental. Alternativas terapêuticas recentes podem otimizar o manejo de pacientes refratários ou com sintomas noturnos persistentes.
Palavras-chave: Inibidor da Bomba de Prótons. Doença do Refluxo Gastroesofágico. Doença Ulcerosa Péptica. Benefícios. IBPs.
1. INTRODUÇÃO
Dentre as doenças que acometem o trato gastroesofágico, destacam-se a Doença do Refluxo Gastroesofágico (DRGE) e Doença Ulcerosa Péptica (DUP), as quais apresentam prevalência mundial de 13%1 e 10%2, aproximadamente.
A doença do refluxo gastroesofágico é uma condição bastante prevalente e muitas vezes incômoda, sobretudo quando os sintomas se manifestam durante a noite. Esse distúrbio ocorre devido ao retorno do conteúdo ácido do estômago para o esôfago, provocando manifestações desconfortáveis como queimação (azia) e regurgitação.3
A úlcera péptica, que inclui tanto as úlceras gástricas quanto as duodenais, resulta de um desequilíbrio entre mecanismos de defesa e agentes agressivos que comprometem a mucosa do trato gastrointestinal.4 Entre os principais fatores envolvidos estão a infecção pela bactéria Helicobacter pylori, o uso de anti-inflamatórios não esteroides (AINEs) e a ação do ácido gástrico.5
Além disso, aspectos relacionados ao estilo de vida, como tabagismo, consumo de bebidas alcoólicas e estresse, também contribuem para seu desenvolvimento. A H. pylori, uma bactéria gram-negativa que coloniza a mucosa gástrica, está presente em cerca de 30% a 40% da população dos Estados Unidos e em quase metade da população mundial.4
Os inibidores da bomba de prótons (IBPs) constituem uma classe de fármacos amplamente utilizada no manejo de diversas condições associadas ao excesso de ácido gástrico.6 Eles derivam da estrutura química do benzimidazol heterocíclico e são amplamente utilizados como primeira escolha pelos gastroenterologistas no tratamento de diversas condições, incluindo: Esofagite; Doença do refluxo não erosiva; Úlcera péptica; Profilaxia de úlceras associadas ao uso de anti-inflamatórios não esteroides (AINEs); Síndrome de Zollinger-Ellison; Parte do esquema de terapia tripla para erradicação da infecção por Helicobacter pylori.6
O omeprazol, representante dessa classe terapêutica, figura entre os dez fármacos mais prescritos nos Estados Unidos. Até 2015, o FDA havia aprovado os seguintes medicamentos desta classe: omeprazol, esomeprazol, lansoprazol, dexlansoprazol, pantoprazol e rabeprazol.6
O presente estudo aborda as principais indicações, mecanismos de ação e contraindicações dos IBPs, ressaltando sua importância no tratamento dos distúrbios relacionados à acidez estomacal, como a Doença do Refluxo Gastroesofágico e a Doença Ulcerosa Péptica.
Também serão discutidos aspectos fundamentais como possíveis efeitos adversos, usos off-label, posologia, farmacodinâmica, farmacocinética, estratégias de monitoramento e interações medicamentosas relevantes, fornecendo subsídios para a atuação da equipe interprofissional no cuidado desses pacientes.
2. REVISÃO DA LITERATURA
Os medicamentos antissecretórios, como os antagonistas dos receptores H2 (H2RAs) e os inibidores da bomba de prótons (IBPs), continuam sendo a base do tratamento clínico da DRGE. Sua ação ocorre de forma indireta, reduzindo a quantidade e a acidez do suco gástrico disponível para o refluxo, o que diminui a agressividade do material que retorna ao esôfago.7 Além disso, os IBPs reduzem o volume da chamada “bolsa ácida” e elevam o pH de seu conteúdo, passando de cerca de 1 para 4.8
Essa vantagem decorre do fato de os IBPs bloquearem a etapa final da produção de ácido gástrico, independentemente do estímulo que desencadeia a secreção. Outro ponto importante é que sua ação é mais eficaz durante o dia do que à noite, o que garante um melhor controle dos episódios de refluxo após as refeições, consolidando-os como o padrão atual de tratamento.8
3. METODOLOGIA
Foram considerados os artigos publicados nos últimos 6 anos, ou seja, publicados no período decorrente entre os anos de 2020 a 2025. Os estudos incompletos ou com fuga do tema a ser revisado, que não oferecem as informações necessárias para o desenvolvimento do tema proposto no trabalho serão excluídos. Dentre estes critérios de exclusão, também se inclui a repetição de estudos em diferentes bases de dados.
Este é um trabalho construído através de uma revisão sistemática de várias literaturas, realizada por meio de várias plataformas científicas de busca online de caráter internacional, como: Public Medical Literature Analysis and Retrieval System Online (PubMed), Medscape, Scientific Eletronic Library Online (Scielo), Google Acadêmico, entre outros.
A partir das buscas com as combinações de tópicos e descritores propostos, será realizada a leitura exploratória dos resumos desses materiais bibliográficos. E posteriormente a leitura completa do texto desses estudos. Portanto, após esse procedimento, serão selecionados trabalhos científicos para constituir a presente revisão.
Para a seleção dos artigos a serem revisados, foram utilizados os seguintes descritores: “Inibidor da Bomba de Prótons”, “Doença do Refluxo Gastroesofágico”, “Doença Ulcerosa Péptica”, “Benefícios” e “IBPs”. Estes descritores também foram procurados em inglês: “Proton Pump Inhibitor”, “Gastroesophageal Reflux Disease”, “Peptic Ulcer Disease”, “Benefits” e “PPIs”, no intuito da promoção de uma base literária mais rica e abrangente quanto ao conteúdo.
Inicialmente os artigos foram classificados por data de publicação e passaram por análise avaliativa de acordo com instrumentos de coleta de dados composto com as questões: autores; ano de publicação; objetivo(s); resultados e discussão; e conclusão da revisão dos trabalhos. Após essa fase de levantamento e análise de conteúdo, este será analisado e utilizado para o desenvolvimento do estudo.
Por se tratar de uma revisão bibliográfica, o presente estudo não necessita de aprovação em Comitê de Ética em Pesquisa – CEP, atendendo as normas estabelecidas na resolução nº 466, de 12 de dezembro de 2012 e a resolução nº 510/2016.
Figura 1 – Fluxograma de Análise Metodológica
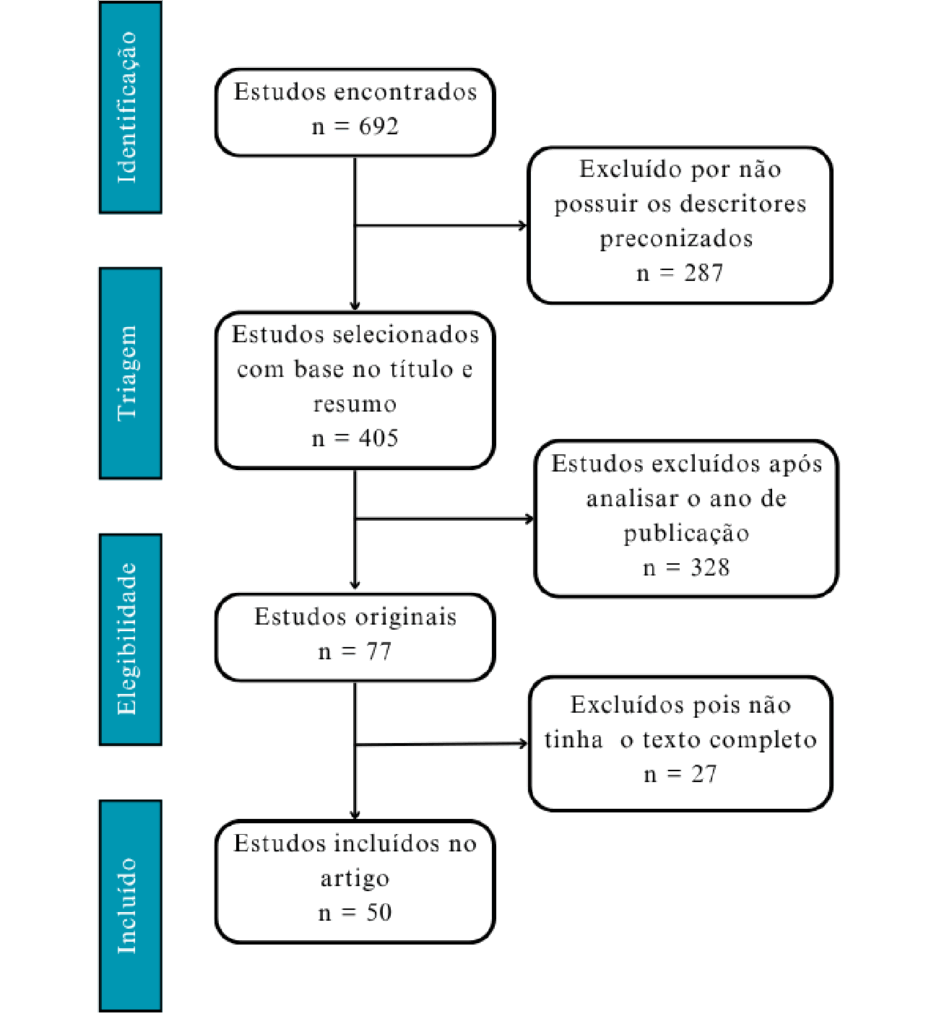
Fonte: Autoria própria.
4. RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
Os inibidores da bomba de prótons (IBPs) constituem o tratamento mais utilizado para a doença do refluxo gastroesofágico (DRGE), considerada um dos transtornos gastrointestinais mais frequentemente diagnosticados nos Estados Unidos, com prevalência estimada em cerca de 20% da população.9 A DRGE é caracterizada pelo retorno anômalo do conteúdo gástrico para o esôfago ou mesmo para regiões acima, incluindo a cavidade oral.9
Além da DRGE, os IBPs também são empregados no manejo da esofagite, da doença do refluxo não erosiva e da úlcera péptica, assim como na prevenção de úlceras associadas ao uso de anti-inflamatórios não esteroides, no tratamento da síndrome de Zollinger-Ellison e como parte dos esquemas terapêuticos para erradicação do Helicobacter pylori.6
4.1 IBP’s e a DRGE
4.1.1 Indicações da Terapia com IBP’s
As indicações para o uso de IBPs variam conforme a condição clínica, o tempo de tratamento e os objetivos terapêuticos. Na prática, muitos distúrbios relacionados à acidez gástrica são inicialmente conduzidos com um ciclo limitado de IBPs, conhecido como fase de tratamento, seguido por uma reavaliação da resposta,10 como descrito na Tabela 1.
Tabela 1 – Indicações de uso dos IBP’s
| Tipo de Indicação | IBP de longo prazo (> 8 semanas) | IBP de curto prazo (< 8 semanas) | ||
| Definido | Condicional | Definido | Condicional | |
| Terapêutico | DRGE com esofagite erosiva (LA C+D); Estenose péptica; – Esofagite eosinofílica com resposta histológica; Esôfago de Barret; Síndrome de Zollinger-Ellison. | – DRGE com resposta incompleta ao IBP de curto prazo; – DRGE com recorrência de sintomas na cessação do IBP; – Esofagite eosinofílica (manutenção); – Tosse crônica idiopática (confirmada por DRGE). | DRGE; Erradicação de H. pylori (terapia combinada); – DRGE não erosivo (Alívio dos sintomas); Doença da úlcera péptica; Inflamação péptica leve. | Dispepsia funcional (ensaio); Refluxo laringofaríngeo (LPR) (teste e revisão); Gastrite leve. |
| Profilático | Uso crônico de AINEs/aspirina + alto risco de GI; – Terapia antiplaquetária úlcera pós sangramento; Esclerose sistêmica com refluxo. | – Corticosteróides de longo prazo + fatores de risco GI. | Uso de AINE/aspirina (curso curto + fatores de risco); – Terapia pós endoscópica com úlcera; Profilaxia de úlcera de estresse (somente UTI). | Pós-cirurgia bariátrica (curto prazo); Pós-escleroterapia e ligadura; – Para cobrir a prescrição de corticosteróides/alta dose de AINE de curto prazo. |
Fonte: Adaptado de Andrawes et al. (2025).
DRGE – Doença do Refluxo Gastroesofágico; IBP – Inibidor da Bomba de Prótons; GI – Gastrointestinal; UTI – Unidade de Terapia Intensiva; AINE – Anti-inflamatório Não Esteroidal; LA C+D – Classificação de Los Angeles, Graus C e D.
Em casos como a DRGE não complicada ou a úlcera péptica, geralmente se prescreve um esquema de 4 a 8 semanas, visando a cicatrização da mucosa e o alívio dos sintomas.11 Após esse período, cabe ao médico decidir sobre a continuidade ou não do tratamento. Quando ocorre melhora clínica e não há fatores de risco relevantes, a terapia pode ser reduzida, interrompida ou utilizada apenas sob demanda.11
Já a chamada terapia de manutenção corresponde ao uso prolongado dos IBPs, com o intuito de prevenir recorrências ou complicações, devendo ser sempre empregada na menor dose eficaz ou, quando possível, em regime intermitente.12 O tratamento contínuo é indicado para pacientes com condições graves ou de risco elevado, como esofagite erosiva avançada (graus C/D de Los Angeles), esôfago de Barrett, úlcera péptica com sangramento ativo, doença ulcerosa recorrente ou síndrome de Zollinger-Ellison.12
Por outro lado, há situações nas quais o uso prolongado de IBPs deve ser evitado (Tabela 2), a fim de minimizar potenciais efeitos adversos, conforme as recomendações da American Gastroenterology Association (AGA),10 as quais as condições estão descritas em diretrizes específicas.
Tabela 2 – Condições em que os IBP’s devem ser evitados
| Condições | Uso de Curto Prazo | Uso a Longo Prazo |
| Terapêutico | – Sintomas isolados de garganta; – Sintomas agudos indiferenciados do GI superior (por exemplo, dor, náusea, vômito) não parecem ser devidos a DRGE ou DUP; – Sintomas isolados do TGI inferior. | – Refluxo não erosivo ou dispepsia funcional sem resposta à terapia de IBP em altas doses; – DUP, incluindo erosões gástricas ou duodenais |
| Profilático | — | – Terapia com esteróides na ausência de terapia concomitante com AINE/antiplaquetária; – Prevenção de sangramento GI recorrente por outras razões que não a úlcera péptica. |
Fonte: Adaptado de Andrawes et al. (2025)
DRGE – Doença do Refluxo Gastroesofágico; IBP – Inibidor da Bomba de Prótons; GI – Gastrointestinal; TGI – Trato GI; AINE – Anti-inflamatório Não Esteroidal; DUP – Doença Ulcerosa Péptica.
4.1.2 Benefícios da Terapia com IBP’s
Os IBPs permanecem como a terapêutica mais eficaz para a DRGE, alcançando índices de cicatrização mucosa entre 75% e 95% após aproximadamente oito semanas de tratamento, por mais que a taxa de resolução sintomática seja inferior, variando de 60% a 85%.13 Entre as diferentes moléculas disponíveis, o esomeprazol apresenta desempenho discretamente superior em termos de cicatrização esofágica quando comparado aos demais IBPs.13
A terapêutica com inibidores da bomba de prótons (IBPs) demonstra ampla eficácia clínica, englobando benefícios que vão desde a supressão ácida sustentada até a promoção de cicatrização mucosa e alívio sintomático em doenças ácido-relacionadas. Diversos estudos randomizados e revisões sistemáticas evidenciam que o uso de IBPs está associado a múltiplos benefícios terapêuticos, como demonstrado na Tabela 3.
Tabela 3 – Benefícios da Terapia Farmacológica com IBPs
| Benefício Clínico / Efeito Esperado | Descrição Curta | Referência |
| Supressão efetiva da secreção ácido gástrica | – Redução potente e prolongada da secreção gástrica de HCl por inibição covalente da H⁺/K⁺-ATPase das células parietais; – Base para controlar sintomas e promover cicatrização mucosa. | Abe, et al., (2025) Tian, et al. (2024) Ito, et al. (2024) |
| Cicatrização da esofagite e cura endoscópica | – Taxas elevadas de cicatrização mucosa em DRGE erosiva (tipicamente ~75–95% em 8 semanas); – Melhora objetiva na mucosa e redução de lesões. | Targownik, et al. (2022) Dharmarajan (2021) |
| Alívio sintomático e melhora na qualidade de vida | – Diminuição significativa da pirose e regurgitação em grande parte dos pacientes; – Melhora em medidas de qualidade de vida relacionadas a refluxo. | Shanika, et al. (2023) Fernández-González, et al. (2024) |
| Terapêutica adjuvante para erradicação de H. pylori | – IBPs aumentam pH gástrico e melhoram eficácia de regimes antibióticos usados para erradicação (são parte de esquemas padrão combinados). | Tanimaru, et al. (2024) Tai, et al. (2025) |
| Cicatrização e prevenção de úlcera péptica / controle de | – Promovem cicatrização de úlceras pépticas e reduzem risco de recidiva; – Usados também na terapia e prevenção de úlceras | Garegnani, et al. (2025) Shanika, et al. (2023) |
| sangramento | associadas a AINE/antiagregantes. | |
| Indicação em síndromes hipersecretoras (ex.: Zollinger–Ellison) | – Controle efetivo da hipersecreção ácida em doenças que provocam secreção ácida excessiva, permitindo manejo clínico prolongado. | Alexander, et al. (2025) Ito, et al. (2024) |
| Redução de hemorragia péptica e profilaxia em pacientes críticos | – Em contextos selecionados (ex.: sangramento péptico ativo, profilaxia de sangramento de stress), redução de eventos hemorrágicos quando adequadamente indicada. | Karuppasamy, et al. (2024) Sutton, et al. (2025) |
| Uso bem estabelecido e perfil de segurança aceitável a curto prazo | – Uso generalizado e eficácia comprovada em curto/curto-médio prazo; – Efeitos adversos sérios são raros, embora exista debate sobre riscos longos. | Franciosi, et al. (2022) Ji, et al. (2024) |
Fonte: Autoria própria.
4.1.3 Desvantagens e Efeitos Adversos da Terapia com IBP’s
Apesar de os inibidores da bomba de prótons (IBPs) serem amplamente aceitos como terapia de primeira escolha para a DRGE, muitos pacientes continuam apresentando sintomas, sobretudo durante o período noturno.28 Isso evidencia uma necessidade ainda não suprida no manejo da doença com esses fármacos. Estima-se que até 40% dos indivíduos relatem alívio insuficiente dos sintomas mesmo em uso de IBPs.29
Essa resposta limitada tem sido atribuída a fatores como ativação dependente da ingestão de alimentos, presença de polimorfismos genéticos e curta meia-vida das medicações. Entre os principais desafios, a inibição inadequada da acidez noturna permanece como uma preocupação relevante, frequentemente exigindo a associação de terapias complementares.30
Os IBPs representam a terapia de primeira escolha no manejo da DRGE. Entretanto, entre 30% e 40% dos pacientes continuam apresentando sintomas de refluxo que não são controlados de forma adequada mesmo após o uso de uma dose padrão do IBP por pelo menos oito semanas.31 Além disso, alguns pacientes exibem esofagite de refluxo (ER) que não cicatriza adequadamente ou que apresenta recorrência após a suspensão do medicamento. Esse quadro é classificado como DRGE refratária ao IBP.32
As razões que explicam a refratariedade podem incluir: supressão ácida incompleta, refluxo não ácido ou fracamente ácido, exposição persistente ao ácido durante a noite, hipersensibilidade do esôfago, alterações na motilidade esofágica, além de fatores psicológicos e psiquiátricos.33
Nos últimos anos, diversos estudos têm investigado os possíveis efeitos adversos associados ao uso prolongado de inibidores da bomba de prótons (IBPs). Entre eles, destaca-se a deficiência de vitamina B12, especialmente em pacientes idosos e em indivíduos com alterações nutricionais, nos quais o risco de desenvolver essa carência pode ser significativamente maior.33
Outro efeito observado é a redução na absorção de cálcio, já que o aumento do pH gástrico dificulta sua passagem para a corrente sanguínea, fazendo com que permaneça no trato gastrointestinal até ser eliminado. A insuficiência de cálcio compromete a atividade de osteoclastos e osteoblastos, prejudicando o processo normal de remodelação óssea.34, 35
Evidências também sugerem que o uso crônico de IBPs pode estar relacionado a maior risco de fraturas, embora essa associação ainda precise ser melhor esclarecida. Além disso, há registros de maior suscetibilidade a infecções, como supercrescimento bacteriano no intestino delgado, infecções por salmonela, campylobacter, Clostridium difficile e pneumonia.35
Outros efeitos adversos relatados incluem o aumento do risco de eventos cardiovasculares graves, como infarto agudo do miocárdio e acidente vascular cerebral, principalmente quando utilizados em altas doses ou por tempo prolongado. Embora menos comuns, também foram descritos casos de comprometimento renal, incluindo nefrite intersticial aguda, além de associação com quadros de demência.34
De forma geral, os principais efeitos relacionados ao uso de IBPs, tanto em curto quanto em longo prazo, costumam ser resumidos em tabelas comparativas para melhor compreensão clínica. Um estudo realizado por Jun Oh e seu grupo (2025), foram realizados 4 semanas de tratamento com Fexuprazano e Esomeprazol em 2 grupos diferentes.36
4.1.4 Atualizações na terapêutica com IBP’s
O fexuprazano tem se mostrado altamente eficaz no controle dos sintomas da doença do refluxo gastroesofágico (DRGE), especialmente no refluxo noturno. Em comparação ao esomeprazol, demonstrou maior capacidade de reduzir a intensidade dos sintomas, com benefícios mais expressivos em pacientes com manifestações graves.36 Além disso, indivíduos que migraram do esomeprazol para o fexuprazano apresentaram melhora superior àqueles que fizeram a transição inversa.37
Seu diferencial clínico está relacionado à meia-vida prolongada, característica dos bloqueadores competitivos de ácido (P-CABs), permitindo supressão ácida mais duradoura durante a noite. Esse efeito sustentado favorece não apenas o alívio sintomático, mas também a melhora da qualidade do sono, da produtividade e da qualidade de vida dos pacientes.37
Comparado a outros P-CABs, como tegoprazan e vonoprazan, o fexuprazano apresenta uma meia-vida ainda mais longa, o que potencializa seu efeito farmacológico e contribui para resultados superiores.38 Assim, representa uma alternativa promissora aos inibidores da bomba de prótons, sobretudo em casos de DRGE com sintomas persistentes ou noturnos intensos, em que os IBPs convencionais apresentam limitações.
Os fármacos à base de alginato representam uma alternativa terapêutica diferenciada, especialmente útil em pacientes com doença do refluxo gastroesofágico (DRGE) que não respondem adequadamente ao tratamento com inibidores da bomba de prótons (IBPs).39 O efeito clínico desses agentes decorre de uma interação específica com o meio ácido gástrico. Ao entrar em contato com o pH ácido do estômago, o alginato de sódio — geralmente obtido de algas marrons — sofre precipitação e origina um gel viscoso e de baixa densidade, descrito como uma “jangada” flutuante.39, 40
Essa barreira mecânica torna-se particularmente relevante na DRGE refratária aos IBPs, uma vez que, embora esses últimos reduzam de forma eficaz a secreção ácida, eles não impedem o refluxo de componentes gástricos não ácidos ou fracamente ácidos, como pepsina e sais biliares.39, 40
Além disso, os IBPs não neutralizam integralmente o chamado “bolso ácido” pós prandial, caracterizado pelo acúmulo de ácido livre próximo à junção gastroesofágica após as refeições. A formação da jangada de alginato atua diretamente sobre essa região, funcionando como uma barreira protetora contra diferentes constituintes do refluxo, e contribuindo para o alívio dos sintomas persistentes mesmo diante de supressão ácida adequada.39, 40
4.2 IBP’s e a DUP
De acordo com as recomendações aprovadas pela FDA (Food and Drug Administration – EUA) e pelas principais diretrizes clínicas, o tratamento da DUP com IBPs deve ser limitado, em geral, a um período máximo de oito semanas.41 Esse tempo é suficiente para alcançar cicatrização da mucosa e alívio sintomático na maioria dos pacientes, refletindo a elevada eficácia desses fármacos no controle da secreção ácida e na promoção da reparação tecidual.42
No entanto, quando se trata da profilaxia de sangramento gastrointestinal, as orientações médicas disponíveis apresentam considerável variabilidade. Em análises posteriores, considerou-se que o uso prolongado de IBPs estava justificado sempre que atendesse a critérios estabelecidos por diretrizes de gastroproteção.42 Nesses casos, a prescrição é interpretada como clinicamente apropriada e alinhada à prática baseada em evidências.
Assim, embora a duração padrão do tratamento da DUP seja restrita, a eficácia dos IBPs no controle da acidez gástrica e na prevenção de complicações, como sangramento digestivo, sustenta sua indicação tanto em regimes de curta duração quanto em contextos de uso prolongado, quando respaldados por recomendações específicas.42
4.2.1 Considerações sobre a Terapia com IBP’s sobre a DUP
A terapia com inibidores da bomba de prótons (IBPs) representa a intervenção farmacológica mais eficaz no manejo da doença ulcerosa péptica (DUP), promovendo supressão ácida sustentada, favorecendo a cicatrização da mucosa gástrica e duodenal, reduzindo a sintomatologia e diminuindo a taxa de recorrência, especialmente quando associada à erradicação do Helicobacter pylori.
Diversos estudos clínicos e revisões sistemáticas demonstram que os IBPs oferecem múltiplos benefícios terapêuticos na DUP, incluindo maior taxa de cicatrização em comparação aos antagonistas dos receptores H₂, prevenção de complicações hemorrágicas, alívio sintomático e contribuição significativa para a redução da necessidade de intervenção cirúrgica, como demonstrado na Tabela 4.
Tabela 4 – Considerações sobre a Terapia com IBPs perante a DUP
| Benefício sobre a DUP | Evidência clínica | Referência |
| Cicatrização de úlceras (gástricas e duodenais) | IBPs elevam persistentemente o pH intragástrico ao inibir a H⁺/K⁺-ATPase, favorecendo a reparação da mucosa ulcerada e alcançando altas taxas de cicatrização em semanas (regimes de 4–8 semanas costumam ser suficientes na maioria dos casos simples). | Ladeira, et al. (2024) |
| Alívio dos sintomas (dor epigástrica, queimação) | Ao reduzir a acidez e a ação proteolítica do pepsinogênio ativado, os IBPs diminuem a dor e desconforto epigástrico associados à DUP, melhorando relatos de sintomas e qualidade de vida. | Wang, et al. (2024) Ladeira, et al. (2024) |
| Redução da recorrência quando associado à erradicação de H. pylori | Esquemas que combinam IBP + antibióticos para erradicação do H. pylori reduzem significativamente as recidivas de úlcera versus terapia sem erradicação bacteriana. | Lima, et al. (2024) Dong, et al. (2024) |
| Prevenção e tratamento de sangramento péptico | Em úlceras sangrantes, a supressão ácida com IBP estabiliza coágulos, reduz re-hemorragia e facilita tratamento endoscópico — indicado no manejo agudo e para reduzir recidiva quando indicado. | Tanimaru, et al. (2024) Ladeira, et al. (2024) |
| Maior eficácia que antagonistas H₂ para cicatrização | Comparados aos bloqueadores H₂, os IBPs atingem supressão ácida mais profunda e duradoura, traduzindo-se em taxas de cicatrização superiores e menor fenômeno de tolerância. | Begg, et al. (2023) Park, et al. (2020) |
| Indicação em síndromes hipersecretoras e proteção mucosa | IBPs são a base terapêutica em síndromes de hipersecreção (Zollinger-Ellison) e em profilaxia quando há risco elevado de lesão péptica (ex.: uso contínuo de AINEs associado a fatores de risco). | Lima, et al. (2024) Alexander, et al. (2025) Ito, et al. (2024) |
| Melhora de desfechos clínicos com condução endoscópica menos frequente de cirurgia | A eficácia clínica e o avanço em terapêuticas endoscópicas diminuíram a necessidade de cirurgia para complicações; tratamento clínico bem conduzido (IBP + erradicação de H. pylori) reduz complicações graves. | Negash, et al. (2023) Ladeira, et al. (2024) |
| Flexibilidade de regimes (indução curta vs. manutenção) | Em DUP não complicada, curso de 4–8 semanas é padrão; manutenção com IBP é reservada a casos selecionados (úlcera recorrente, sangrante ou hipersecretor). Essa estratégia maximiza benefício e minimiza exposição prolongada. | Lima, et al. (2024) Wang, et al. (2024) Andrawes, et al. (2025) Targownik, et al. (2022) |
| Evidência de melhora objetiva em exames (endoscopia) e parâmetros laboratoriais | Estudos e revisões incluídos relatam melhoria endoscópica documentada e resolução de sinais inflamatórios locais quando o tratamento é aplicado adequadamente. | Shung e Laine (2024) Negash, et al. (2023) |
Fonte: Autoria própria.
5. CONCLUSÃO/CONSIDERAÇÕES FINAIS
Com base na revisão apresentada, é possível concluir que os inibidores da bomba de prótons (IBPs) constituem a base terapêutica mais eficaz no manejo da Doença do Refluxo Gastroesofágico (DRGE) e da Doença Ulcerosa Péptica (DUP). Sua capacidade de promover supressão ácida sustentada, cicatrização mucosa e alívio sintomático é bem estabelecida, sendo superior à oferecida por outras classes farmacológicas, como os antagonistas H₂. Além disso, os IBPs permitem a prevenção de complicações, incluindo sangramentos e recorrências, especialmente quando associados à erradicação do Helicobacter pylori, consolidando sua importância tanto em esquemas de indução quanto de manutenção terapêutica.
Os IBPs apresentam flexibilidade de uso, podendo ser administrados em cursos de curta duração para cicatrização e alívio sintomático, ou em regimes prolongados em pacientes de alto risco, como portadores de esofagite erosiva grave, esôfago de Barrett ou síndromes hipersecretoras. Essa abordagem permite otimizar o benefício clínico, minimizando a exposição prolongada a possíveis efeitos adversos. A individualização da terapia, aliada à reavaliação periódica, garante um equilíbrio entre eficácia e segurança, sendo fundamental para a condução adequada do paciente com DRGE ou DUP.
Apesar de sua eficácia comprovada, a utilização prolongada de IBPs não está isenta de efeitos adversos, incluindo alterações na absorção de micronutrientes, risco aumentado de infecções gastrointestinais, complicações renais e, possivelmente, eventos cardiovasculares. Tais achados reforçam a necessidade de monitoramento clínico, prescrição criteriosa e educação do paciente quanto ao uso correto do medicamento, destacando a importância de estratégias de profilaxia e condução de terapia sob demanda sempre que possível.
Por fim, novas opções terapêuticas, como os bloqueadores competitivos de ácido (PCABs) e os medicamentos à base de alginato, oferecem alternativas promissoras, especialmente para pacientes com DRGE refratária ou com sintomas noturnos persistentes. Esses avanços, aliados ao uso racional dos IBPs, contribuem para a melhoria da qualidade de vida, redução de complicações e otimização do manejo clínico dessas condições ácido relacionadas, reforçando o papel central dos IBPs e das estratégias combinadas no tratamento moderno da DRGE e da DUP.
REFERÊNCIAS
- Liu, Xinyang et al. “Sex-specific association of visceral and abdominal subcutaneous adipose tissue with gastroesophageal reflux disease: a large-scale prospective cohort study.” BMC gastroenterology vol. 25,1 635. 2 Sep. 2025, doi:10.1186/s12876-025-04218-x. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40898149/
- Wadewitz, Elisabeth et al. “Approaches for the treatment of perforated peptic ulcers: a network meta-analysis of randomized controlled trials.” Langenbeck’s archives of surgery vol. 410,1 266. 5 Sep. 2025, doi:10.1007/s00423-025-03848-9. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40911086/
- Maret-Ouda, John et al. “Gastroesophageal Reflux Disease: A Review.” JAMA vol. 324,24 (2020): 2536-2547. doi:10.1001/jama.2020.21360. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33351048/
- Fang, Yi-Jen et al. “Impact of anti-peptic ulcer disease medications on type 2 diabetes mellitus risk in patients with PUD: a population-based retrospective cohort study.” Therapeutic advances in endocrinology and metabolism vol. 16 20420188251323945. 19 Mar. 2025, doi:10.1177/20420188251323945. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40110098/
- Almadi, Majid A et al. “Peptic ulcer disease.” Lancet (London, England) vol. 404,10447 (2024): 68-81. doi:10.1016/S0140-6736(24)00155-7. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38885678
- Ahmed A, Clarke JO. Proton Pump Inhibitors (PPI) [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www-ncbi-nlm-nih-gov.translate.goog/books/NBK557385/?_x_tr_sl=en&_x_tr_tl=pt&_x_tr_hl=pt&_x_tr _pto=tc.
- Scarpignato, Carmelo et al. “Hyaluronic acid and chondroitin sulfate-based medical devices: formulations, esophageal mucosal protection, and their place in the management of GERD.” Therapeutic advances in gastroenterology vol. 18 17562848251337822. 11 Jun. 2025, doi:10.1177/17562848251337822. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40520453/
- Barberio, Brigida et al. “Comparison of acid-lowering drugs for endoscopy negative reflux disease: Systematic review and network Meta-Analysis.” Neurogastroenterology and motility vol. 35,1 (2023): e14469. doi:10.1111/nmo.14469. Disponível em: https://pubmed.ncbi.nlm.nih.gov/36153790/
- Wołowiec, Łukasz et al. “Pharmacodynamics, pharmacokinetics, interactions with other drugs, toxicity and clinical effectiveness of proton pump inhibitors.” Frontiers in pharmacology vol. 16 1507812. 23 Jul. 2025, doi:10.3389/fphar.2025.1507812. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40771914/
- Andrawes, Monica et al. “Proton Pump Inhibitors (PPIs)-An Evidence-Based Review of Indications, Efficacy, Harms, and Deprescribing.” Medicina (Kaunas, Lithuania) vol. 61,9 1569. 31 Aug. 2025, doi:10.3390/medicina61091569. Disponível em: https://pubmed.ncbi.nlm.nih.gov/41010960/
- Peyton-Navarrete, Anna et al. “Prescribing responsibly: navigating the tides of deprescribing in proton pump inhibitor stewardship.” Pharmacoepidemiology 4.3 (2025): 15. Doi: https://doi.org/10.3390/pharma4030015. Disponível em: https://www.mdpi.com/2813-0618/4/3/15
- Targownik, Laura et al. “AGA clinical practice update on de-prescribing of proton pump inhibitors: expert review.” Gastroenterology 162.4 (2022): 1334-1342. Doi: https://doi.org/10.1053/j.gastro.2021.12.247. Disponível em: https://pubmed.ncbi.nlm.nih.gov/35183361/
- Shibli, Fahmi et al. “Drug treatment strategies for erosive esophagitis in adults: a narrative review.” Translational gastroenterology and hepatology vol. 10 54. 23 Jul. 2025, doi:10.21037/tgh-24-168. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40755734/.
- Abe, Hiroko et al. “Effect of oral proton pump inhibitor administration on reducing the delayed bleeding risk in five upper gastrointestinal endoscopic treatments.” The American journal of gastroenterology, 10.14309/ajg.0000000000003746. 22 Aug. 2025, doi:10.14309/ajg.0000000000003746. Disponível https://pubmed.ncbi.nlm.nih.gov/40844513
- Tian, Lidi et al. “Efficacy and safety of vonoprazan versus proton pump inhibitors in the treatment of peptic ulcer disease: a systematic review and network meta-analysis for randomized controlled trails.” Frontiers in nutrition vol. 11 1436993. 5 Sep. 2024, doi:10.3389/fnut.2024.1436993. Disponível em: https://pubmed.ncbi.nlm.nih.gov/39301419/ .
- Ito, Tetsuhide et al. “Long-Term Proton Pump Inhibitor-Acid Suppressive Treatment Can Cause Vitamin B12 Deficiency in Zollinger-Ellison Syndrome (ZES) Patients.” International journal of molecular sciences vol. 25,13 7286. 2 Jul. 2024, doi:10.3390/ijms25137286. Disponível em: https://pubmed.ncbi.nlm.nih.gov/39000391/ .
- Dharmarajan, Thiruvinvamalai S. “The Use and Misuse of Proton Pump Inhibitors: An Opportunity for Deprescribing.” Journal of the American Medical Directors Association vol. 22,1 (2021): 15-22. doi:10.1016/j.jamda.2020.09.046. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33321078/
- Shanika, Lelwala Guruge Thushani et al. “Proton pump inhibitor use: systematic review of global trends and practices.” European journal of clinical pharmacology vol. 79,9 (2023): 1159-1172. doi:10.1007/s00228-023-03534-z. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC10427555/?utm_source=chatgpt.com
- Fernández-González, Sara María et al. “Proton Pump Inhibitors in Pediatric Gastroesophageal Reflux Disease: A Systematic Review of Randomized Controlled Trials.” Children (Basel, Switzerland) vol. 11,3 296. 1 Mar. 2024, doi:10.3390/children11030296. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38539331/
- Tanimaru, Aline Namie et al. “Inibidores da bomba de prótons e sua relação com a microbiota gastrointestinal: O benefício compensa o risco?.” Revista de Medicina 103.3 (2024). Doi: http://dx.doi.org/10.11606/issn.1679-9836.v103i3e-210046. Disponível em: https://revistas.usp.br/revistadc/article/view/210046
- Tai, Wei-Chen et al. “Comparative efficacy and safety of vonoprazan versus esomeprazole-based high-dose dual therapies for first-line Helicobacter pylorieradication: a randomized controlled trial.” Therapeutic advances in gastroenterology vol. 18 17562848251378066. 20 Sep. 2025, doi:10.1177/17562848251378066. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40984972/
- Garegnani, Luis et al. “Proton pump inhibitors for the prevention of non-steroidal anti-inflammatory drug-induced ulcers and dyspepsia.” The Cochrane database of systematic reviews vol. 5,5 CD014585. 8 May. 2025, doi:10.1002/14651858.CD014585.pub2. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40337979/
- Alexander, Ryan G et al. “Diarrhea, Weight Loss, and an Elevated Gastrin: A Case Report.” Case reports in gastroenterology vol. 19,1 428-433. 11 Jun. 2025, doi:10.1159/000545714. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40503451/
- Karuppasamy, Gowri et al. “Proton pump inhibitors in inpatients: Are we getting it right? A retrospective analysis.” Qatar medical journal vol. 2024,4 60. 11 Nov. 2024, doi:10.5339/qmj.2024.60. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC11568192/?utm_source=chatgpt.com
- Sutton, Michael M et al. “Overuse of Intravenous Proton-Pump Inhibitors in the Treatment of Low-Risk Upper Gastrointestinal Bleeding.” Journal of clinical gastroenterology, 10.1097/MCG.0000000000002211. 23 Jun. 2025, doi:10.1097/MCG.0000000000002211. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40549584/
- Franciosi, James P et al. “Proton Pump Inhibitor Therapy for Eosinophilic Esophagitis: History, Mechanisms, Efficacy, and Future Directions.” Journal of asthma and allergy vol. 15 281-302. 26 Feb. 2022, doi:10.2147/JAA.S274524. Disponível em: https://pubmed.ncbi.nlm.nih.gov/35250281/
- Ji, Jeong-Yeon et al. “The Impact of a Twice-daily Versus Once-daily Proton Pump Inhibitor Dosing Regimen on Laryngopharyngeal Reflux Symptoms: A Prospective Randomized Controlled Trial.” Journal of neurogastroenterology and motility vol. 30,4 (2024): 459-467. doi:10.5056/jnm23118. Disponível https://pubmed.ncbi.nlm.nih.gov/39139030/
- Jung, Hye-Kyung et al. “2020 Seoul Consensus on the Diagnosis and Management of Gastroesophageal Reflux Disease.” Journal of neurogastroenterology and motility vol. 27,4 (2021): 453-481. doi:10.5056/jnm21077. Disponível em: https://pubmed.ncbi.nlm.nih.gov/34642267/
- Katz, Philip O et al. “ACG Clinical Guideline for the Diagnosis and Management of Gastroesophageal Reflux Disease.” The American journal of gastroenterology vol. 117,1 (2022): 27-56. doi:10.14309/ajg.0000000000001538. Disponível em: https://pubmed.ncbi.nlm.nih.gov/34807007/
- Ramani, Azaan et al. “Review of the clinical development of fexuprazan for gastroesophageal reflux-related disease.” European journal of clinical pharmacology vol. 79,8 (2023): 1023-1029. doi:10.1007/s00228-023-03521-4. Disponível em: https://pubmed.ncbi.nlm.nih.gov/37344679/
- Lin, Si Hui et al. “Dynamic Relevance Between Reflux Events and Esophageal Motility in Patients With Proton Pump Inhibitor-Refractory Gastroesophageal Reflux Disease.” Journal of digestive diseases vol. 26,5-6 (2025): 221-229. doi:10.1111/1751-2980.70007. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40891132/
- Mizuno, Hideki et al. “Follow-up study of vonoprazan maintenance therapy for reflux esophagitis: A 96-week evaluation in patients with PPI-refractory disease.” Biomedical reports vol. 23,4 160. 30 Jul. 2025, doi:10.3892/br.2025.2038. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40777627/
- Yadlapati, Rena et al. “AGA Clinical Practice Update on the Personalized Approach to the Evaluation and Management of GERD: Expert Review.” Clinical gastroenterology and hepatology : the official clinical practice journal of the American Gastroenterological Association vol. 20,5 (2022): 984-994.e1. doi:10.1016/j.cgh.2022.01.025. Disponível em: https://pubmed.ncbi.nlm.nih.gov/35123084/
- Sharma, Priya, and Rena Yadlapati. “Pathophysiology and treatment options for gastroesophageal reflux disease: looking beyond acid.” Annals of the New York Academy of Sciences vol. 1486,1 (2021): 3-14. doi:10.1111/nyas.14501. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33015827/
- Aljahdli, Emad S et al. “Assessment of Awareness and Knowledge of Proton Pump Inhibitors Among the General Population in Saudi Arabia.” Cureus vol. 14,7 e27149. 22 Jul. 2022, doi:10.7759/cureus.27149. Disponível em: https://pubmed.ncbi.nlm.nih.gov/36017269/
- Jun Oh, Dong et al. “Comparison of Fexuprazan and Esomeprazole for the Control of Nocturnal Gastroesophageal Reflux Symptoms: A Randomized, Crossover Study.” Journal of neurogastroenterology and motility, 10.5056/jnm25119. 25 Aug. 2025, doi:10.5056/jnm25119. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40854583/
- Lee, Kang Nyeong et al. “Randomized controlled trial to evaluate the efficacy and safety of fexuprazan compared with esomeprazole in erosive esophagitis.” World journal of gastroenterology vol. 28,44 (2022): 6294-6309. doi:10.3748/wjg.v28.i44.6294. Disponível em: https://pubmed.ncbi.nlm.nih.gov/36504556/
- He, Jinjie et al. “Safety, Tolerability and Pharmacokinetics of Single Ascending and Multiple Oral Doses of Tegoprazan in Healthy Chinese Subjects.” Clinical drug investigation vol. 41,1 (2021): 89-97. doi:10.1007/s40261-020-00986-4. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33355910/
- Tangvoraphonkchai, Kawin et al. “Comparable efficacy of generic and original alginate for symptom control in PPI-refractory GERD.” Scientific reports vol. 15,1 28429. 4 Aug. 2025, doi:10.1038/s41598-025-13400-w. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40760009/
- Spada, Cristiano et al. “E-Gastryal® + Magnesium Alginate Plus PPI vs. PPI Alone in GERD: Results from the GENYAL® Randomized Controlled Trial.” Journal of clinical medicine vol. 14,13 4794. 7 Jul. 2025, doi:10.3390/jcm14134794. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40649167/
- Laine, Loren et al. “ACG Clinical Guideline: Upper Gastrointestinal and Ulcer Bleeding.” The American journal of gastroenterology vol. 116,5 (2021): 899-917. doi:10.14309/ajg.0000000000001245. Disponível https://pubmed.ncbi.nlm.nih.gov/33929377
- Villars, Jordan A et al. “Proton Pump Inhibitor Use Exceeding the U.S. Food and Drug Administration Approved Treatment Duration for Patients With Peptic Ulcer Disease: A Retrospective Cohort Study.” Pharmacoepidemiology and drug safety vol. 34,5 (2025): e70152. doi:10.1002/pds.70152. Disponível em: https://pubmed.ncbi.nlm.nih.gov/40296703/
- Ladeira, Larissa Melo, et al. “ÚLCERA PÉPTICA: ACOMPANHAMENTO CLÍNICO E TRATAMENTO CIRÚRGICO DE INTERCORRÊNCIAS.” Revista Ibero-Americana de Humanidades, Ciências e Educação 10.9 (2024): 829-839. Doi: doi.org/10.51891/rease.v10i9.15599. Disponível em: https://periodicorease.pro.br/rease/article/view/15599
- Wang, Wen-Xin et al. “Efficacy and Safety of Potassium-Competitive Acid Blockers vs Proton Pump Inhibitors for Peptic Ulcer Disease or Postprocedural Artificial Ulcers: A Systematic Review and Meta-analysis.” Clinical and translational gastroenterology vol. 15,9 e1. 1 Sep. 2024, doi:10.14309/ctg.0000000000000754. Disponível em: https://pubmed.ncbi.nlm.nih.gov/39072507/
- Lima, Victor Mayrink, et al. “TRATAMENTOS PARA GASTRITE E ÚLCERAS PÉPTICAS NÃO PERFURADAS, DESAFIOS, AVANÇOS TECNOLÓGICOS E PERSPECTIVAS.” Periódicos Brasil. Pesquisa Científica 3.2 (2024): 1958-1968. Doi: https://doi.org/10.36557/pbpc.v3i2.229. Disponível em: https://periodicosbrasil.emnuvens.com.br/revista/article/view/229
- Dong, Yongqi et al. “Comparative efficiency and safety of potassium competitive acid blockers versusLansoprazole in peptic ulcer: a systematic review and metaanalysis.” Frontiers in pharmacology vol. 14 1304552. 11 Jan. 2024, doi:10.3389/fphar.2023.1304552. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38273830/
- Begg, Maha et al. “Comparing the Safety and Efficacy of Proton Pump Inhibitors and Histamine-2 Receptor Antagonists in the Management of Patients With Peptic Ulcer Disease: A Systematic Review.” Cureusvol. 15,8 e44341. 29 Aug. 2023, doi:10.7759/cureus.44341. Disponível em: https://pubmed.ncbi.nlm.nih.gov/37779765/
- Park, Joo-Hyun et al. “Comparing proton pump inhibitors with histamin-2 receptor blockers regarding the risk of osteoporotic fractures: a nested case-control study of more than 350,000 Korean patients with GERD and peptic ulcer disease.” BMC geriatrics vol. 20,1 407. 15 Oct. 2020, doi:10.1186/s12877-020-01794-3. Disponível em: https://pubmed.ncbi.nlm.nih.gov/33059626/
- Negash, Samuel et al. “Gastric outlet obstruction due to peptic ulcer disease in a 5 years-old female child. Case report. June 23, 2022.” International journal of surgery case reports vol. 105 (2023): 108086. doi:10.1016/j.ijscr.2023.108086. Disponível em: https://pubmed.ncbi.nlm.nih.gov/37018952/
- Shung, Dennis L; Loren Laine. “Review article: Upper gastrointestinal bleeding – review of current evidence and implications for management.” Alimentary pharmacology & therapeutics vol. 59,9 (2024): 1062-1081. doi:10.1111/apt.17949. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38517201/
1Discente do Curso Superior de Medicina do Centro Universitário Aparício Carvalho (FIMCA) e-mail: carolinanabati@gmail.com
2Discente do Curso Superior de Medicina do Centro Universitário Aparício Carvalho (FIMCA) e-mail: brunoaranha07@gmail.com
3Discente do Curso Superior de Medicina do Centro Universitário Aparício Carvalho (FIMCA) e-mail: dudarubira@gmail.com
4Docente do Curso Superior de Medicina do Centro Universitário Aparício Carvalho (FIMCA). Especialista em Farmacologia Clínica (CRF-PR). e-mail: rogeliorochabarros@gmail.com
