REGISTRO DOI: 10.69849/revistaft/ra10202510071634
Rafael Ferreira Batista; Cadma da Silva Pereira; Eliane Gabriel de Lima Negraes; Denise Cristina Vargas Albuquerque; Daniela Falcão Nobre; Rafaela Rodrigues Gomes Alencar; Fernanda Kincheski de Almeida; Jessica Ribeiro Martins Lanis; Marcela Cristina Borges dos Santos; Kali Mundim Dias de Jesus
RESUMO
Parada cardiorrespiratória é a interrupção súbita e inesperada da circulação sanguínea e da respiração eficaz, resultando em ausência de pulso e colapso respiratório.
A ressuscitação cardiopulmonar (RCP) envolve um conjunto de medidas que incluem suporte circulatório e ventilatório, ou seja, compressão torácica e ventilação. A parada cardiorrespiratória (PCR) pediátrica apresenta uma epidemiologia e etiologia distintas da PCR em adultos, geralmente resultando de uma piora respiratória ou circulatória progressiva. Os ritmos cardíacos mais frequentes em pediatria que indicam a necessidade de RCP são a bradicardia com sinais de hipoperfusão, assistolia e atividade elétrica sem pulso (AESP). Arritmias ventriculares ocorrem em menos de 10% das vítimas pediátricas em PCR pré-hospitalar.
No cenário pré-hospitalar, a sobrevida da PCR pediátrica até a alta hospitalar chega a 11,4% e varia conforme a faixa etária (17,1% para adolescentes, 13,2% para crianças, 4,9% para lactentes). Já a PCR pediátrica hospitalar apresenta uma maior sobrevida, chegando a até 41,1%.
Apesar das dificuldades na avaliação do prognóstico neurológico, devido à grande variabilidade de faixa etária, diferenças nas métricas e momento de avaliação, os sobreviventes parecem apresentar um prognóstico favorável em até 47% dos casos. O prognóstico favorável da PCR pediátrica é multifatorial, com a ocorrência em ambiente hospitalar, a detecção de ritmos iniciais chocáveis [fibrilação ventricular (FV) ou taquicardia ventricular (TV)] e o início precoce do suporte básico de vida (SBV) sendo alguns dos fatores associados.
A cadeia de sobrevivência pediátrica da American Heart Association (AHA) foi subdividida em intra-hospitalar e pré-hospitalar, composta por seis elos. O SBV em Pediatria é representado pelos três elos iniciais, que correspondem à prevenção da PCR pediátrica, ao SBV precoce e ao acionamento do serviço médico de emergência concomitante (pré-hospitalar) ou da equipe de resposta rápida, se disponível (intra-hospitalar).
Já o suporte avançado de vida (SAV) em pediatria inclui a manutenção do SBV associada à avaliação do ritmo cardíaco, desfibrilação, obtenção de acesso vascular, tratamento medicamentoso e manejo de via aérea avançada. Os cuidados pós-PCR permitem a manutenção da perfusão e viabilidade de órgãos vitais e a prevenção de novas lesões, seguida pela fase de reabilitação do paciente.
As diretrizes de RCP são revisadas pelo Internacional Liaison Comitee on Resuscitation (ILCOR), composto pelos principais comitês de ressuscitação do mundo, com o objetivo de promover um fórum de discussões sobre aspectos relevantes da RCP, disseminar o treinamento e estimular a pesquisa em áreas controversas ou com evidências escassas. Este capítulo abordará a ciência da RCP com base no ILCOR.
Importante ainda, indicar aos nobres leitores as principais alterações científicas em 2020.
Algumas das principais alterações científicas de 2020 incluem:
A RCP de alta qualidade deve se concentrar na administração de compressões torácicas na profundidade e na frequência adequadas, minimizando as interrupções na RCP, permitindo o retorno total do tórax entre as compressões e evitando ventilação excessiva.
Busque uma frequência respiratória de 20 a 30 ventilações por minuto para bebês e crianças que estiverem recebendo RCP com uma via aérea avançada existente ou que estiverem recebendo ventilação de resgate e tiverem pulso.
Para pacientes com ritmos não chocáveis, quanto antes a epinefrina for administrada depois do início da RCP, mais probabilidade o paciente terá de sobreviver.
Usar um tubo endotraqueal com cuff reduz a necessidade de trocas do tubo endotraqueal.
O uso rotineiro de pressão cricoide não reduz o risco de regurgitação durante a ventilação com bolsa-máscara e pode impedir o sucesso da intubação.
Para PCR extra-hospitalar, a ventilação com bolsa-máscara é recomendada, se comparada com intervenções de via aérea avançada, como a intubação endotraqueal.
A ressuscitação não termina com o retorno da circulação espontânea (RCE). Um excelente atendimento pós-PCR é de importância vital para obter os melhores resultados possíveis para o paciente. Para crianças que não retomam a consciência depois do RCE, esse atendimento inclui controle direcionado da temperatura e monitoramento contínuo por eletrocardiograma.
Para todas as crianças, a prevenção e/ou o tratamento da hipotensão, da hiperóxia ou da hipóxia e da hipercapnia ou hipocapnia são importantes.
Além dos cuidados de SBV padrão, a naloxona é recomendada para todos os pacientes pediátricos com parada respiratória por suspeita de overdose de opioides. Para choque séptico, os profissionais podem administrar 10 mL/kg ou 20 mL/kg de fluidos, com reavaliação frequente da sobrecarga de fluidos. Para choque séptico refratário a fluidos, use infusões de epinefrina ou norepinefrina.
Palavras-chave: Parada cardiorrespiratória em crianças, PCR, RCP, Causas mais comum em crianças, RCE.
ABSTRACT
Cardiopulmonary arrest is the sudden and unexpected interruption of blood circulation and effective breathing, resulting in pulselessness and respiratory collapse. Cardiopulmonary resuscitation (CPR) involves a set of measures that include circulatory and ventilatory support, i.e., chest compressions and ventilation. Pediatric cardiopulmonary arrest (CPA) has a distinct epidemiology and etiology from adult CPA, usually resulting from progressive respiratory or circulatory deterioration. The most common cardiac rhythms in pediatrics that indicate the need for CPR are bradycardia with signs of hypoperfusion, asystole, and pulseless electrical activity (PEA). Ventricular arrhythmias occur in less than 10% of pediatric victims of prehospital CPA. In the pre-hospital setting, pediatric cardiac arrest survival to hospital discharge reaches 11.4% and varies by age group (17.1% for adolescents, 13.2% for children, and 4.9% for infants). In-hospital pediatric cardiac arrest, on the other hand, has a higher survival rate, reaching up to 41.1%. Despite the difficulties in assessing neurological prognosis due to the wide variability among age groups, differences in metrics, and timing of assessment, survivors appear to have a favorable prognosis in up to 47% of cases. The favorable prognosis for pediatric cardiac arrest is multifactorial, with occurrence in a hospital setting, detection of initial shockable rhythms (ventricular fibrillation (VF) or ventricular tachycardia (VT)), and early initiation of basic life support (BLS) being some of the associated factors. The American Heart Association (AHA) pediatric chain of survival has been subdivided into in-hospital and pre-hospital care, consisting of six links. Pediatric BLS is represented by the three initial steps: preventing pediatric cardiac arrest, early BLS, and activating the concomitant emergency medical service (pre-hospital) or the rapid response team, if available (in-hospital). Advanced life support (ALS) in pediatrics includes maintaining BLS combined with cardiac rhythm assessment, defibrillation, obtaining vascular access, drug therapy, and advanced airway management. Postcardiac arrest care maintains perfusion and viability of vital organs and prevents further injury, followed by the patient’s rehabilitation phase. CPR guidelines are reviewed by the International Liaison Committee on Resuscitation (ILCOR), composed of the world’s leading resuscitation committees, with the goal of providing a forum for discussion on relevant aspects of CPR, disseminating training, and stimulating research in areas of controversy or limited evidence. This chapter will address the science of CPR based on ILCOR. It is also important to inform our readers of the main scientific changes of 2020. Some of the main scientific changes of 2020 include: High-quality CPR should focus on delivering chest compressions at the appropriate depth and rate, minimizing interruptions in CPR, allowing full chest recoil between compressions, and avoiding excessive ventilation.
Aim for a respiratory rate of 20 to 30 breaths per minute for infants and children receiving CPR with an existing advanced airway or who are receiving rescue ventilation and have a pulse. For patients with non-shockable rhythms, the sooner epinephrine is administered after CPR begins, the more likely the patient will survive. Using a cuffed endotracheal tube reduces the need for endotracheal tube changes. Routine use of cricoid pressure does not reduce the risk of regurgitation during bagmask ventilation and may impede successful intubation. For out-of-hospital cardiac arrest, bag-mask ventilation is recommended compared to advanced airway interventions such as endotracheal intubation. Resuscitation does not end with the return of spontaneous circulation (ROSC). Excellent post-cardiac arrest care is vital to achieving the best possible patient outcomes. For children who do not regain consciousness after ROSC, this care includes targeted temperature control and continuous electrocardiogram monitoring. For all children, prevention and/or treatment of hypotension, hyperoxia or hypoxia, and hypercapnia or hypocapnia are important. In addition to standard BLS care, naloxone is recommended for all pediatric patients with respiratory arrest due to suspected opioid overdose. For septic shock, providers can administer 10 mL/kg or 20 mL/kg of fluids, with frequent reassessment of fluid overload. For fluid-refractory septic shock, use epinephrine or norepinephrine infusions.
Keywords: Cardiac arrest in children, cardiac arrest, CPR, Most common causes in children, ROSC.
INTRODUÇÃO
Avaliação inicial para identificar uma situação potencialmente fatal:
A análise do paciente pediátrico na emergência foi definido pela Academia Americana de Pediatria (AAP) a partir do Triângulo de Avaliação Pediátrica (TAP). Este método é composto pela observação da aparência, respiração e circulação da pele, permitindo avaliação geral da criança em 30 a 60 segundos afim de determinar a gravidade da doença e a intervenção. O cuidado precoce pode prevenir a progressão para PCR, insuficiência respiratória, choque ou agravamento de outros sintomas clínicos.
Figura 1: Triângulo de avaliação pediátrica
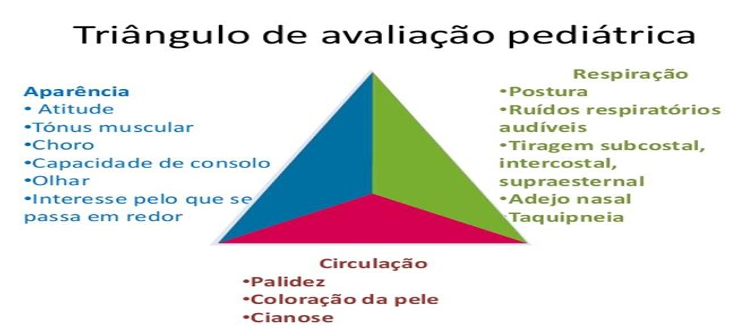
Fonte: Adaptado PALS, 2020.
Aparência: O Primeiro componente do Triângulo de Atendimento Pediátrico é a avaliação da aparência geral da criança. Isso inclui observar o nível de consciência, a resposta a estímulos e a interação com o ambiente. A aparência da criança pode fornecer pistas importantes sobre seu estado neurológico e geral. Mudanças no estado mental, como sonolência excessiva, confusão ou incapacidade de responder a estímulos, podem indicar problemas neurológicos significativos.
Respiração: A avaliação da respiração é o segundo ponto do Triângulo de atendimento pediátrico. A respiração é uma função vital que fornece oxigênio ao corpo e elimina dióxido de carbono. Os profissionais de saúde avaliam a presença de esforço respiratório, movimentos respiratórios, a profundidade da respiração e qualquer anormalidade na respiração, como estridor, gemidos, sibilos ou uso de músculos acessórios. Mudanças na frequência ou na qualidade da respiração podem indicar problemas respiratórios graves que requerem intervenção imediata.
Circulação: O terceiro componente é a avaliação da circulação. Isso envolve a observação da pele e mucosas: palidez, moteamento, rubor, petéquias, cianose periférica/central. A circulação adequada é crucial para fornecer oxigênio e nutrientes a todos os tecidos do corpo. Alterações na frequência cardíaca, como taquicardia ou bradicardia, e sinais de má perfusão, como extremidades frias ou palidez, podem indicar problemas circulatórios sérios, como choque.
O Triângulo de Atendimento Pediátrico, serve como uma ferramenta de triagem rápida, permitindo que os profissionais de saúde identifiquem de forma eficiente crianças em estado crítico que precisam de intervenção imediata. Após a avaliação desses três componentes, a abordagem se expande para a avaliação completa de vias aéreas, respiração, circulação, deficiências neurológicas e exposição (ABCDE),que guia as intervenções subsequentes e o tratamento adequado
Importante, os profissionais de saúde seguirem alguns passos e acrônimo essenciais para o atendimento na emergência pediátrica, exemplo abaixo do famoso TICOF, vejamos:
1.Tônus (tônus muscular).
2.Interatividade/nível de consciência com cuidador/examinador.
3.Consolação/Consolabilidade.
4.Olhar.
5.Fala ou choro.
Por sua vez, e não menos importante, devemos lançar um olhar minucioso na avaliação primária pediátrica.
A avaliação primária desempenha um papel importante na abordagem da criança em situações de emergência, oferecendo uma visão rápida e abrangente da condição de saúde do paciente. A avaliação primária segue uma abordagem sistemática para avaliar as vias aéreas, respiração, circulação, deficiências neurológicas e exposição (ABCDE).
Cada elemento desse processo é essencial para determinar a necessidade de intervenção imediata e para priorizar o tratamento. Vamos estudar cada componente em detalhes:
A – Airway/Vias Aéreas: A prioridade é assegurar vias aéreas permeáveis. Avalie se a criança está respirando espontaneamente ou se há obstrução das vias aéreas.
Utilize manobras apropriadas para manter as vias aéreas desobstruídas.
B- Breathing/Respiração: Avalie a frequência respiratória, a profundidade da respiração e a presença de anormalidades respiratórias. A bradipneia abaixo de 60 ou frequência respiratória irregular são sinais de parada iminente. Determine se a criança está em necessidade de suporte respiratório e, se necessário, inicie intervenções para melhorar a oxigenação e a ventilação.
C – Circulation/Circulação: Verifique o pulso e a frequência cardíaca para avaliar a circulação. Identifique sinais de choque, como taquicardia ou hipotensão, tempo de enchimento capilar e intervenha conforme necessário para estabilizar a circulação.
D – Disability/Deficiências Neurológicas: Avalie o estado neurológico da criança, incluindo o nível de consciência, a resposta a estímulos, resposta pupilares e outras alterações neurológicas. Essa avaliação ajuda a determinar a gravidade do comprometimento neurológico e orienta a intervenção.
E – Exposure/Exposição: Garanta que a criança esteja adequadamente exposta para permitir uma avaliação completa do corpo em busca de ferimentos ou condições médicas. Mantenha a criança aquecida para prevenir hipotermia.
A avaliação primária é projetada para ser conduzida de maneira rápida e eficaz, permitindo a identificação imediata de problemas críticos. Se durante essa avaliação surgirem achados anormais, a intervenção imediata é crucial para estabilizar a criança.
O PALS enfatiza a necessidade de intervenções rápidas e baseadas em evidências para melhorar as chances de sobrevivência e recuperação da criança.
Por sua vez, a avaliação secundária é um componente essencial da abordagem da criança em situações de emergência, conforme preconizado pelas diretrizes mais recentes. Após a conclusão da avaliação primária, que se concentra nas vias aéreas, respiração, circulação, deficiências neurológicas e exposição (ABCDE), a avaliação secundária visa a uma avaliação mais detalhada e completa do estado da criança.
A avaliação secundária é realizada após a estabilização das funções vitais imediatas e a implementação das intervenções necessárias identificadas durante a avaliação primária. Esta etapa oferece aos profissionais de saúde a oportunidade de coletar informações mais abrangentes e detalhadas sobre a condição da criança.
A avaliação secundária também fornece uma base sólida para tomada de decisões informadas e personalizadas, direcionando o tratamento e a gestão da situação de emergência.
A abordagem sistemática da avaliação secundária, conforme orientada pelas diretrizes do PALS, contribui para melhorar a qualidade dos cuidados prestados a crianças em situações críticas, visando uma abordagem abrangente e eficaz. Uma abordagem eficaz para a avaliação secundária é o uso do método SAMPLE, que ajuda a direcionar a coleta de informações clínicas relevantes. (Ludhmila Abrahão Hajjar, et al Emergências médicas).
Método SAMPLE (acrônimo):
S – Sintomas: Coleta de informações sobre os sintomas que a criança está apresentando, como dor, desconforto, falta de ar, náuseas.
A – Alergias: Identificação de alergias conhecidas da criança, especialmente aquelas que podem influenciar o tratamento ou causar reações adversas.
M – Medicamentos: Registro dos medicamentos que a criança está tomando regularmente, incluindo dosagens e horários. Também é importante perguntar sobre o uso recente de medicamentos.
P – Passado Médico: Obtenção de informações sobre o histórico médico da criança, incluindo condições médicas pré-existentes, cirurgias anteriores, hospitalizações, entre outros.
L – Última Ingestão Oral: Perguntar sobre a última vez que a criança comeu ou bebeu. Isso é importante para determinar se a criança pode estar em risco de aspiração ou se precisa ser preparada para procedimentos invasivos.
E – Eventos/Exposições: Coleta de informações sobre eventos que possam ter levado à emergência, como quedas, acidentes ou exposição a substâncias nocivas. Fonte: PALS –AHA 2020 – Adaptado.
A utilização do método SAMPLE durante a avaliação secundária permite que os profissionais de saúde coletem informações relevantes e valiosas para entender a história clínica da criança. Isso ajuda a direcionar o diagnóstico, a determinar a gravidade da situação e a planejar intervenções adequadas.
Ao seguir essa abordagem, os profissionais de saúde podem tomar decisões informadas e personalizadas, garantindo um cuidado mais completo e eficaz para a criança em situação de emergência. A avaliação secundária é conduzida em um ambiente mais calmo, permitindo a avaliação de áreas específicas do corpo e a obtenção de informações detalhadas sobre a história clínica.
Durante a avaliação secundária, vários elementos são considerados: Sinais Vitais: Aferir novamente os sinais vitais, incluindo frequência cardíaca, frequência respiratória, pressão arterial e temperatura. Essas medidas fornecem informações importantes sobre a estabilidade da criança e a eficácia das intervenções realizadas.
SUPORTE AVANÇADO DE VIDA PEDIÁTRICO
Os componentes de compõem o suporte avançado de vida pediátrico incluem o manejo da via aérea avançada, detecção de arritmias através de monitorização eletrocardiográfica, obtenção de um acesso vascular, tratamento medicamentoso e desfibrilação imediata se houver indicação, além de considerar e tratar as possíveis causas da PCR. (Ludhmila Abrahão Hajjar, et al Emergências médicas).
Abaixo segue o algoritmo da avaliação pediátrica inicial, vejamos:
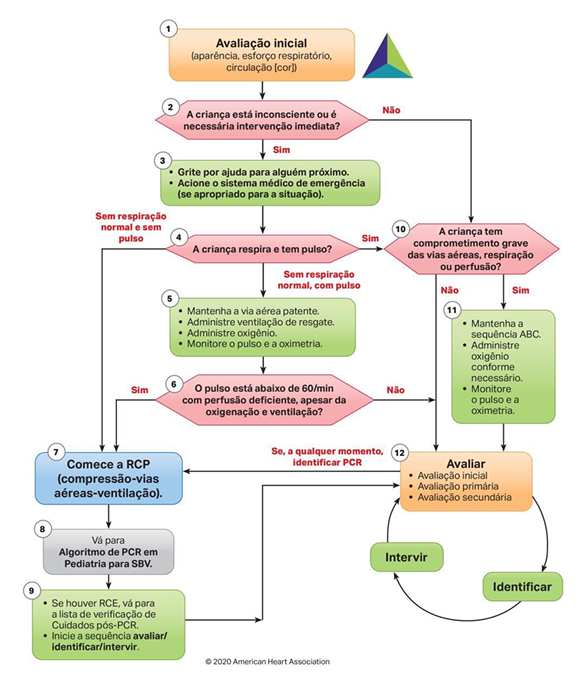
Suporte ventilatório
O suporte ventilatório deve incluir a permeabilização da via aérea, oferta de oxigênio e ventilação adequada. Após a abertura da via aérea, iniciar a ventilação com BVM, idealmente realizada com 2 socorristas treinados. Em PCR hospitalar, a ventilação através de BVM é satisfatória, pois apresentou desfecho semelhante aos casos com uso da via aérea avançada. A via aérea avançada através da intubação orotraqueal, preferencialmente com tubo com cuff (fórmula: idade/4 + 3,5), deve ser obtida com atenção para minimizar as interrupções das compressões.
A pressão cricoide não é recomendada de rotina, pois pode impedir o sucesso da intubação. Já a máscara laríngea pode ser uma alternativa para garantir a via aérea avançada na PCR.
Com a inserção da via aérea avançada, o uso da capnografia ou CO2 expirado (EtCO2) é fortemente recomendado durante a PCR, pois permite a avaliação da qualidade de compressão torácica durante a RCP e reconhece o retorno da circulação espontânea (RCE), ou seja, o reaparecimento do pulso. O RCE pode ser identificado através de elevações abruptas e sustentadas de EtCO2 com valores próximos ao normal.
Após a obtenção da via aérea avançada, não há necessidade de coordenar as compressões com as ventilações. Deste modo, um socorrista realiza as compressões de alta qualidade sem interrupções (100 a 120/minuto) e o outro realiza 1 ventilação a cada 2 a 3 segundos através do tubo traqueal (30 ventilações/minuto em lactentes e 25 ventilações/minuto em crianças). A cada 2 minutos de RCP, trocar as funções e checar o ritmo rapidamente para avaliar a necessidade de indicar o choque. (Hajjar, Ludhmila Abrahão, et al 2024, “Emergências médicas”)
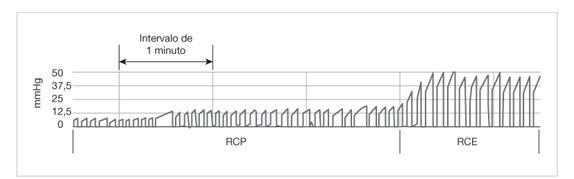
Capnografia durante a parada cardiorrespiratória.
EtCO2: CO2 exalado; RCE: retorno da circulação espontânea; RCP: ressuscitação cardiopulmonar.
Epinefrina
Em todos os ritmos da PCR, ou seja, nos casos de assistolia, AESP, FV e TV sem pulso, a epinefrina pode ser indicada pelo efeito alfa-adrenérgico, pois aumenta a pressão diastólica da aorta, permitindo melhora da perfusão coronariana. Quando associada às compressões torácicas, aumenta a oferta de oxigênio, promove melhora da contratilidade miocárdica, estimula a contração espontânea e aumenta o sucesso da desfibrilação.
A epinefrina deve ser administrada o mais precocemente possível nos ritmos não chocáveis (assistolia e AESP), idealmente até 5 minutos da PCR, pois o retardo pode estar associado a menor RCE, menor sobrevida em 24 horas e à alta hospitalar com bom prognóstico neurológico.
A dose recomendada de epinefrina é 0,01 mg/kg (0,1 mL/kg solução 1:10.000) via intravenosa e intraóssea ou, na ausência de acesso vascular, 0,1 mg/kg (0,1 mL/kg da solução 1:1000) por via traqueal. As doses subsequentes são recomendadas a cada 3 a 5 minutos. A via endotraqueal somente deve ser considerada na impossibilidade do acesso vascular, pois sua absorção é imprevisível.
Cálcio
Indicado no tratamento da hipocalcemia documentada, hipercalemia, hipermagnesemia e intoxicação por bloqueadores de canal de cálcio. Dose recomendada é 5-7 mg/kg de cálcio elementar. Cloreto de cálcio 10% é a preparação de escolha pela melhor biodisponibilidade que gluconato de cálcio. Dar preferência à infusão por via central devido ao risco de esclerose e infiltração.
Magnésio
Indicado no tratamento de hipomagnesemia documentada e na TV torsades de pointes (taquicardia ventricular polimórfica com QT longo).
Glicose
Devido aos depósitos reduzidos e às elevadas necessidades de glicose, as crianças podem desenvolver hipoglicemia. Assim, a glicose precisa ser monitorada durante a PCR e a hipoglicemia deve ser tratada prontamente com glicose a 25% na dose de 2 a 4 mL/kg (0,5 a 1,0 g/kg de glicose).
Bicarbonato de sódio
A administração de bicarbonato de sódio não está indicada de rotina na PCR. O seu uso pode ser considerado em algumas situações especiais como hipercalemia, acidose metabólica grave preexistente e algumas síndromes tóxicas.
Dose inicial é 1 mEq/kg (1 mL/kg da solução 8,4%) por via intravenosa ou intraóssea.
A administração excessiva do bicarbonato piora a oxigenação tecidual, além de causar hipocalemia, hipocalcemia, prejuízo da função cardíaca, hipernatremia e hiperosmolaridade. O bicarbonato leva à precipitação do cálcio e inativação de catecolaminas, de modo que deve-se evitar a mistura dessas soluções.
RESSUSCITAÇÃO CARDIOPULMONAR DE ACORDO COM O RITMO CARDÍACO
A maioria das crianças em PCR apresenta assistolia ou AESP. Somente cerca de 10% das PCR pediátricas ocorrem em ritmo chocável (FV ou TV sem pulso) associado a um desfecho favorável.
A meta inicial do tratamento da PCR é a obtenção do RCE através do SBV de alta qualidade, desfibrilação precoce nos ritmos chocáveis, ventilação e oxigenação apropriadas, além de administração precoce de epinefrina na assistolia e AESP.
Outro aspecto essencial durante a RCP é buscar e tratar ativamente as prováveis causas reversíveis de PCR. Recomenda-se o uso dos Hs e Ts
Ritmos não chocáveis: assistolia e atividade elétrica sem pulso
A assistolia e a AESP são os ritmos mais comuns na PCR pediátrica. A AESP corresponde a uma atividade elétrica organizada, caracterizada em geral por um ritmo lento, QRS alargado e sem pulso. As prioridades na abordagem dos ritmos não chocáveis devem ser o rápido início da RCP de alta qualidade, obtenção de acesso vascular para administração precoce de epinefrina, idealmente em até 5 minutos e repetida a cada 3 a 5 minutos.
Ritmos chocáveis: fibrilação ventricular e taquicardia ventricular sem pulso
A desfibrilação precoce é o tratamento definitivo da FV e TV sem pulso e apresenta sobrevida de 17% a 20%. As pás dos desfibriladores manuais podem ter dois tamanhos: adultos (indicado para maiores 1 ano ou 10 kg) e infantil (indicado para menores de 1 ano). A interface com uso do gel condutor permite a condução da energia elétrica. O posicionamento convencional das pás corresponde à posição anterolateral, ou seja, uma pá na região infraclavicular direita e a outra lateral ao mamilo esquerdo, não permitindo que as pás se toquem. Caso as pás estejam próximas, indica-se a posição anteroposterior das pás. (Hajjar, Ludhmila Abrahão, et al 2024, “Emergências médicas”).
A dose inicial de desfibrilação recomendada é de 2 J/kg. Caso a dose inicial seja refratária, estará indicada a dose de 4 J/kg e doses subsequentes de 4 a 10 J/kg. Após o primeiro choque (2 J/kg), reiniciar imediatamente as compressões de alta qualidade, obter acesso vascular para administração de medicações e alternar compressores. Caso o ritmo chocável persista após 2 minutos do choque inicial, indicar nova desfibrilação com carga de 4 J/kg seguida pela administração de epinefrina 1:10.000 por via endovenosa ou intraóssea durante as compressões, podendo ser repetida a cada 3 a 5 minutos. (Hajjar, Ludhmila Abrahão, et al 2024, “Emergências médicas”).
Checar o ritmo após 2 minutos do segundo choque (4 J/kg), alternar compressores, se ritmo chocável, selecionar a carga de 4 a 10 J/kg e preparar para administrar um antiarrítmico como amiodarona ou lidocaína.
Durante o atendimento, caso seja observado um ritmo não chocável e sem pulso, prosseguir através do algoritmo de assistolia e AESP. Se for observado um ritmo organizado ou uma elevação abrupta dos valores de capnografia, checar o pulso, pois pode sinalizar RCE.
Algoritmo de PCR pediátrica.
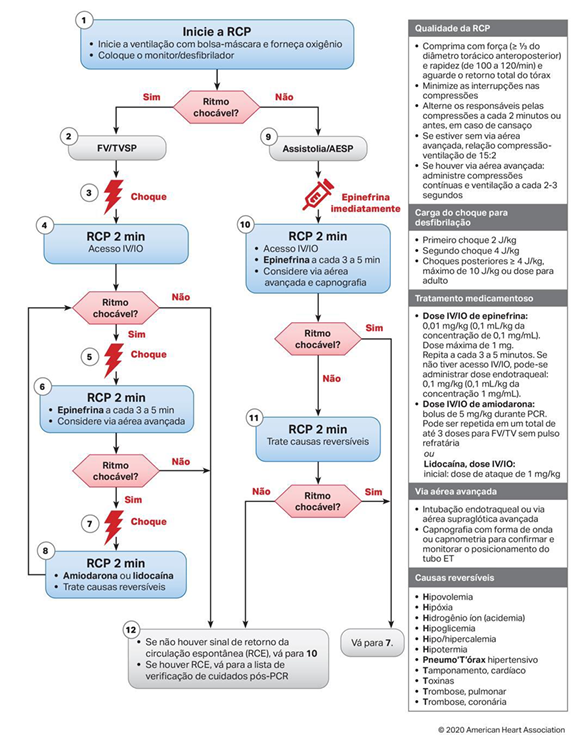
Fonte: Pals, 2020.
Algoritmo de bradicardia pediátrica.
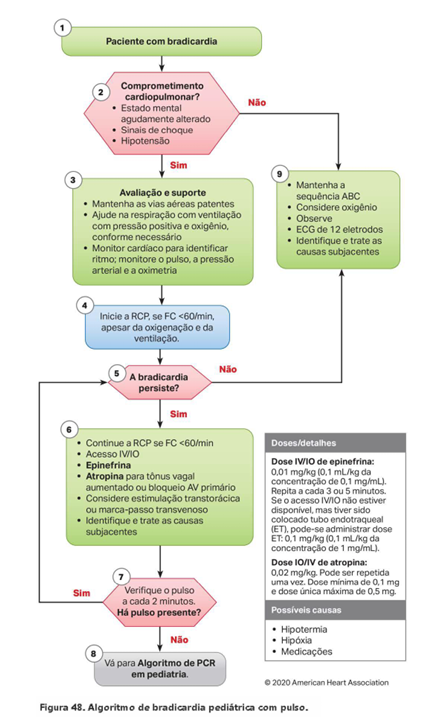
Fonte: PALS, 2020.
Se houver sinais de comprometimento cardiopulmonar, vá para a avaliação e suporte (Etapa 3):
Mantenha a via aérea patente. Ajude na respiração com ventilação com pressão positiva e oxigênio, conforme necessário.
Use um monitor cardíaco para identificar o ritmo. Monitore o pulso, a pressão arterial e a oximetria. Se não houver sinais de comprometimento cardiopulmonar (Etapa 9), mantenha os ABCs, conforme a necessidade.
Considere oxigênio.
Observe e realize reavaliações frequentes.
Obtenha um ECG de 12 derivações.
Identifique e trate as causas subjacentes 6H e 5T.
Iniciar a RCP, se a frequência cardíaca for menor que 60/min, apesar da oxigenação e da ventilação (Etapa 4).
Determine se a bradicardia persiste (Etapa 5).
Se os pulsos, a perfusão e as respirações estiverem adequadas, não será necessário tratamento de emergência. Monitore e continue a avaliação (Etapa 9). Se a bradicardia e o comprometimento cardiopulmonar persistirem (Etapa 6), Continue a RCP.
Estabeleça o acesso IV/10.
Administre epinefrina.
Administre atropina para tônus vagal aumentado ou bloqueio AV primário.
Considere estimulação transtorácica/lransvenosa.
Identifique e trate as causas subjacentes.
Se a bradicardia estiver associada a comprometimento cardiopulmonar e se a frequência cardíaca for inferior a 60/minuto, apesar de oxigenação e ventilação eficazes, continue a RCP.
Se a bradicardia persistir, passe ao tratamento medicamentoso e à possível estimulação com marca passo. Reavalie com frequência a resposta da criança a cada tratamento administrado.
Uma criança com bradicardia primária pode se beneficiar de avaliação por um cardiologista pediátrico. Porém, não atrase o início do tratamento de emergência, inclusive a RCP de alta qualidade, Se a vítima apresentar sintomas. Verifique o pulso e reavalie o ritmo (Etapa 7).
Verifique o pulso a cada 2 minutos. Se não houver pulso, vá para o algoritmo 11 da PCR pediátrica (Etapa 8) na Parte 5: identificação e tratamento de PCR.
Se houver insucesso, reavalie para determinar se a bradicardia e o comprometimento cardiopulmonar continuam, apesar da oxigenação, da ventilação da RCP (Etapa 5). Se a bradicardia e o comprometimento cardiopulmonar tiver melhorado, mantenha os ABCs conforme necessário, considere oxigênio, observe e realize reavaliações frequentes, faça um ECG de 12 derivações e identifique e trate as causas subjacentes. Se a criança ainda estiver bradicárdica com comprometimento cardiopulmonar, administre medicamentos, considere estimulação transtorácica/transvenosa e identifique e trate as causas subjacentes 6H e 5T.
CUIDADOS PÓS-RESSUSCITAÇÃO
Os objetivos nesta fase são a manutenção da perfusão dos órgãos vitais, prevenção de nova PCR e lesões secundárias. Deste modo, identificar as causas e adequar o tratamento é essencial. A terapêutica deve incluir normoxemia (saturação de oxigênio 94 a 99%) evitando a hipoxemia, PaCO2 apropriado à condição de base, ajustar fluidos e vasopressores/inotrópicos para manter pressão sistólica acima do percentil 5 para a idade, corrigir hipoglicemia e tratar agressivamente a hipertermia.
Em crianças que permanecem comatosas após PCR pré-hospitalar ou hospitalar, o uso de normotermia (36 a 37,5°C) ou hipotermia leve (32 a 34°C) demonstrou resultados semelhantes. Por outro lado, a hipertemia foi associada a pior prognóstico neurológico Pacientes que permanecem comatosos após RCE devem ter monitorização através do eletroencefalograma assim que disponível, pois a crise epiléptica é frequente no período pós anóxia, ocasionando aumento da demanda metabólica cerebral, além do potencial de amplificar a lesão secundária.
Avaliação clínica para predizer sobrevida com bom prognóstico neurológico foi um novo tópico revisado nas últimas diretrizes. A recomendação é que seja realizada de modo multimodal, sendo sugerida a avaliação do reflexo pupilar após 12 horas do RCE.
REABILITAÇÃO
O período de reabilitação foi acrescido à cadeia de sobrevivência AHA 2020, pois muitos pacientes necessitam de uma abordagem multiprofissional. É recomendado o seguimento neurológico desses pacientes sobreviventes por um período mínimo de 1 ano, pois pode haver melhora da função neurológica ou aparecimento de nova morbidade.
TÉRMINO DA RESSUSCITAÇÃO
Não há até o momento preditores que possam guiar e orientar o momento do término da RCP em crianças. Alguns indicadores como tempo de PCR, idade, local da PCR (pré-hospitalar ou hospitalar), ritmo inicial, número de doses de epinefrina e PCR presenciada podem estar associados ao prognóstico da PCR.
TRATAMENTO DAS TAQUIARRITMIAS
A criança tem pulso (ou sinais de circulação)?
Se não tiver pulso, inicie o Algoritmo da PCR pediátrica e tratamento de PCR.
Como a verificação do pulso é pouco precisa, identificar uma PCR pode exigir que se reconheça a ausência de sinais de circulação (ou seja, a criança não responde, não respira ou só apresenta gasping). Com a monitorização invasiva da pressão arterial, observa-se ausência de forma de onda arterial.
Se tiver pulso, prossiga com o algoritmo para taquicardia.
Prioridades do tratamento inicial
Assim que identificar uma taquiarritmia em um bebê ou criança, avalie se há sinais de hipotensão, alteração do estado mental, choque (ou seja, perfusão deficiente) ou instabilidade hemodinâmica potencialmente fatal. As prioridades do tratamento inicial compreendem:
• Manter a via aérea patente; auxiliar a ventilação, conforme a necessidade.
• Usar um monitor cardíaco para identificar o ritmo e monitorar o pulso, a pressão arterial e a oximetria.
• Estabelecer o acesso IV/10.
• Fazer um ECG de 12 derivações (mas sem atrasar a intervenção de urgência).
• Obter estudos laboratoriais (p. ex., potássio, glicose, cálcio ionizado, magnésio, gasometria para avaliar o pH e a causa das alterações do pH), conforme for apropriado. Não retarde a intervenção de urgência para esses estudos.
• Avaliar o estado neurológico.
• Prever a necessidade de medicações, dependendo do tipo de distúrbio do ritmo (isto é, supraventricular ou ventricular).
• Simultaneamente, tentar identificar e tratar causas reversíveis.
Intervenções de emergência
As intervenções de emergência específicas do tratamento de taquiarritmias com pulso são ditadas pela gravidade da condição da criança. Os tratamentos também variam segundo a largura do complexo QRS observado (estreito x largo). As intervenções podem compreender:
• Manobras vagais (se a criança com uma taquicardia de complexo estreito estiver estável)
• Tratamento medicamentoso
• Cardioversão sincronizada
Manobras vagais
Em bebês e crianças normais, a frequência cardíaca diminui quando o nervo vago é estimulado. Em pacientes com TSV, a estimulação vagal pode encerrar a taquicardia, por retardar a condução através do nódulo AV. Diversas manobras podem estimular a atividade vagal.
As probabilidades de sucesso de tais manobras encerrarem as taquiarritmias variam segundo a idade, o nível de cooperação e a condição de fundo da criança.
Conceitos fundamentais: Manobras vagais
A aplicação de gelo no rosto é uma manobra vagal que pode ser realizada em crianças de todas as idades . Encha um pequeno saco plástico com uma mistura de gelo e água. Aplique-o à metade superior do rosto da criança, por 15 a 20 segundos.
Não obstrua o nariz nem a boca.
Tratamento medicamentoso
ADENOSINA
Medicamento de escolha para o tratamento da TSV • Com monitorização contínua do ECG, administre 0,1 mg/kg (dose inicial máxima: 6 mg) na forma de um bolus tanto por via acessória quanto por mecanismos de IV rápido.
• Eficaz para a TSV causada por reentrada no nódulo AV reentrada do nódulo AV) • Se o medicamento for eficaz, o ritmo se converterá em ritmo sinusal em 15 a 30 segundos depois da aplicação.
• Se não tiver efeito, administre uma dose de 0,2 mg/kg (segunda dose máxima: 12 mg); essa dose seja necessária quando o medicamento é administrado em uma veia periférica (e não central).
• Uma causa comum de “falha” com Administração da adenosina é que o medicamento é administrado lentamente demais ou com bolus IV inadequado. administre-a o mais rapidamente possível. • A adenosina pode ser administrada por via IO.
AMIODARONA
Pode ser considerada ao tratar hemodinamicamente a TSV refratária a manobras vagais, adenosina e cardioversão, perfusão deficiente, recomenda-se uma dose de ataque 5 mg/kg, infundida por 20 a 60 minutos (dose máxima única: 300 mg). Como esse medicamento pode causar hipotensão e diminuir a contratilidade cardíaca, aplicar de forma lenta
• Para arritmias supraventriculares e ventriculares com taquiarritmias atriais e ventriculares em crianças recomenda-se uma velocidade mais lenta de aplicação.
• Segura e eficaz para TV hemodinamicamente instável em crianças.
A administração rápida de amiodarona pode causar vasodilatação e hipotensão; pode também causar bloqueio cardíaco e TV polimórfica.
Cardioversão sincronizada
A cardioversão elétrica é dolorosa. Sempre que possível, estabeleça acesso vascular e forneça sedação e analgesia procedimental antes da cardioversão, sobretudo para bebês ou crianças hemodinamicamente estáveis.
Se a condição da criança estiver instável, não retarde a cardioversão sincronizada para obter acesso vascular. A sedação em situação de arritmia faz o risco aumentar. Quando a sedação procedimental for administrada nessa situação, os profissionais deverão selecionar cuidadosamente as medicações para minimizar os efeitos hemodinâmicos.
Se o paciente estiver estável e você estiver considerando cardioversão, consulte um especialista.
Importante ainda, tecer conceitos importantes sobre a cardioversão:
Os desfibriladores manuais podem administrar choques sincronizados e não sincronizados. Se não sincronizado, o choque será administrado a qualquer momento do ciclo cardíaco. Os choques sincronizados são usados para cardioversão de TSV e TV com pulso.
Se o choque for sincronizado, sua aplicação será cronometrada para coincidir com a onda R do complexo QRS do paciente. A meta é impedir uma FV, que poderia ocorrer por aplicação do choque durante o período vulnerável da onda T. Ao pressionar o botão SHOCK (choque) para administrar um choque sincronizado, o desfibrilador/cardioversor pode parecer estar fazendo uma pausa antes de administrar o choque, porque está aguardando para sincronizar a administração do choque com o próximo complexo QRS.
Para ritmos sem pulsos, não importa, clinicamente, se o choque é sincronizado.
Dessa forma, choques não sincronizados (p. ex., desfibrilações) são usados para FV e TSVP.
Considerações importantes: Em teoria, a sincronização é simples. O operador pressiona o botão SYNC (Sincronizar) do desfibrilador, carrega o dispositivo e administra o choque. No entanto, na prática, podem ocorrer alguns problemas, tais como na maioria das unidades, o botão SYNC (Sincronizar) deve ser ativado a cada tentativa de cardioversão sincronizada.
A maioria dos dispositivos volta automaticamente à posição de choque não sincronizado imediatamente após a administração de um choque sincronizado.
Se as ondas R de uma taquicardia forem indiferenciadas ou de baixa amplitude, os sensores do monitor talvez não sejam capazes de identificá-las e, logo, o choque não será administrado. Se isso ocorrer, aumente o ganho do eletrodo de ECG que está sendo monitorado ou selecione um eletrodo de ECG diferente.
A sincronização pode exigir mais tempo (p.ex, se for necessário aplicar eletrodos de ECG separados ou se o operador não estiver familiarizado com o equipamento).
Indicações: Use a cardioversão sincronizada para Pacientes hemodinamicamente instáveis (perfusão deficiente, hipotensão ou insuficiência cardíaca) com taquiarritmias (TSV, flutter atrial, TV), mas com pulsos palpáveis.
Cardioversão eletiva, sob a orientação de um cardiologista pediátrico, em crianças com TSV hemodinamicamente estável, flutter atrial ou TV com pulso.
Carga de energia: Em geral, a cardioversão requer menos energia que a desfibrilação. Comece com uma carga de energia de 0,5 J/kg a 1 J/kg para a cardioversão de TSV ou TV com pulso. Se a carga inicial for ineficaz, aumente-a para 2 J/kg. Um profissional experiente pode aumentar a carga do choque de forma mais gradual (p. ex., 0,5 J/kg; em seguida, 1 J/kg; depois 2 J/kg nas cargas posteriores). Se o ritmo não se converter em ritmo sinusal, reavalie o diagnóstico de TSV x TV. Aplique sedação, se necessário, mas não atrase a cardioversão.
Algoritmo pediátrico de taquicardia com pulso.
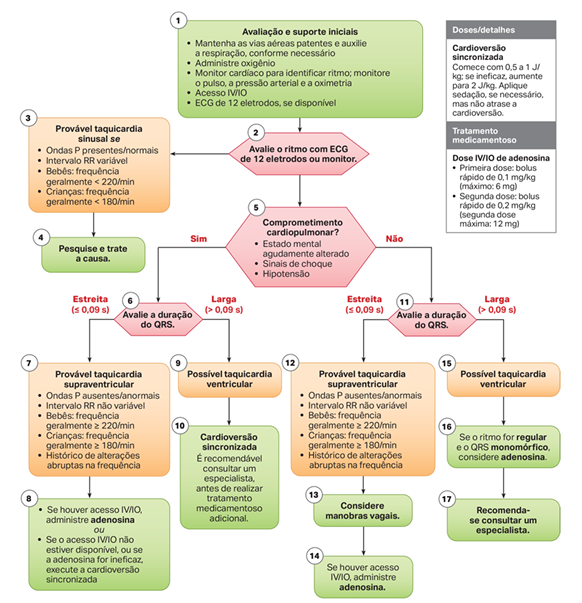
Fonte: PALS, 2020.
TRATAMENTO DE CHOQUE APÓS RCE
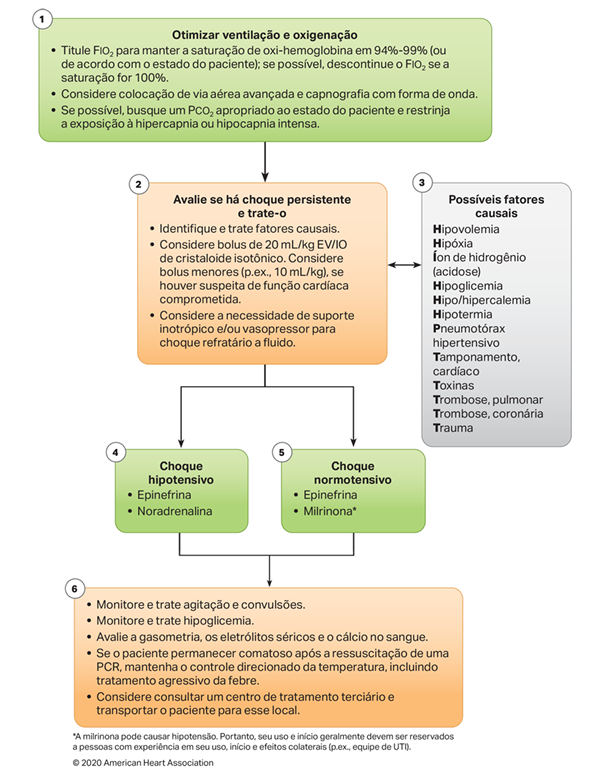
FONTE: Pals,2020.
ALGORITMO DO SAVP CHOQUE APÓS PCR
Vejamos em detalhes o algoritmo acima:
Otimizar a oxigenação e a ventilação (Etapa 1)
A obtenção de oxigenação e de ventilação adequadas é importante para manter a função cardiovascular. Titule o F1O2 para manter uma saturação de O2 de 94% a 99%;ajuste a concentração de O2 se a saturação for 100%. Considere a colocação de uma via aérea avançada e o uso da capnogrania de forma de onda, se ainda não estiverem estabelecidas. Se possível, almeje um Pco2 adequado para os problemas do paciente e limite a exposição à hipercapnia ou à hipocapnia intensa.
Fluidoterapia (Etapa 2)
A primeira intervenção a ser considerada para tratamento de choque é a administração de um bolus de 20 mLikg IV/IO de cristaloides isotônicos. Se houver suspeita de disfunção miocárdica pós-PCR, que normalmente ocorre, considere a administração de um bolus deex, figado grande, edema pulmonar, distensão venosa jugular, coração grande na radiografia), avalie, atentamente, a necessidade de suporte inotrópico elou vasopressor para choque refratário a fluidos.
Reavalie a criança com frequência e após cada bolus de fluido para determinar a resposta ao tratamento.
Possíveis fatores de contribuição (Etapa 3)
Considere fatores que podem contribuir para o choque pós-PCR, como desordens metabólicas e condições tais como hipovolemia e tamponamento cardíaco (Hs e Ts).
Choque hipotensivo (Etapa 4)
Se a criança permanecer hipotensa após a administração de fluido por bolus, considere a infusão de um dos fármacos a seguir ou uma combinação deles:
·Epinefrina: para via IV/IO, administre 0,03 a 0,2 mcg/kg por minuto e/ou ·Norepinefrina: para via IV/IO, administre 0,03 a 0,5 mcg/kg por minuto.
A faixa de dosagem de limite superior pode ser altamente variável e deve ser baseada nas situações clínicas.
Verifique se a pré-carga cardíaca está adequada; baseie sua escolha de medicação na causa mais provável da hipotensão (frequência cardíaca inadequada, contratilidade deficiente, vasodilatação excessiva ou uma combinação de fatores).
Se a frequência cardíaca estiver anormalmente baixa, a administração de catecolamina pode aumentar a frequência cardíaca e o débito cardíaco. No entanto, quando as catecolaminas causam taquicardia extrema, elas aumentam a demanda de O2 pelo miocárdio.
Epinefrina a baixa dose. Geralmente produzem efeitos β-adrenérgicos (aumento da frequência cardíaca, contratilidade e vasodilatação); doses mais altas obter o efeito clínico desejado. A epinefrina pode ser preferível à dopamina em crianças (especialmente bebês) com acentuada instabilidade circulatória e choque hipotensivo.
Norepinefrina, é um potente agente inotrópico e vasoconstritor periférico. Titule a infusão para tratar o choque com RVS baixa (séptico. anafilático, neurogênico) que não responde à administração de fluido por bolus.
Choque normotensivo (Etapa 5)
Se a criança estiver normotensa, mas permanecer com perfusão deficiente depois da administração de fluido por bolus, considere administrar um dos seguintes fármacos ou uma combinação deles:
·Eplnefrina a baixa dose: para via IVIIO, administre de 0,03 mcg/kg 0,05 mcgikg por minuto e/ou
· Milrinona: para via IV/IO, carregue com 50 mcg/kg durante 10 a 60 minutos. As doses de ataque podem causar hipotensão;infusão:0.25 mcg/kg a 0,75 mcg/kg por minuto
A milrinona é um inodilatador que aumenta o débito cardíaco com pouco efeito sobre a frequência cardíaca e a demanda de 02 pelo miocárdio. Use um inodilatador para tratar a disfunção miocárdica com maior resistência vascular sistêmica ou pulmonar. Talvez seja necessário administrar fluidos adicionais porque os efeitos vasodilatadores expandirão o espaço vascular, podendo levar a hipotensão.
Em comparação com medicamentos como dopamina e norepinefrina, os inodilatadores têm uma meia-vida longa. Além disso, sempre que a velocidade da infusão for alterada, haverá mais demora para obter um novo efeito hemodinâmico estável (4,5 horas com a milrinona). Os efeitos adversos podem persistir por várias horas após a interrupção da infusão. A milrinona é excretada pelo rim, e a dose pode precisar ser reduzida em pacientes com doença renal.
Outras considerações pós-PCR (Etapa 6)
O RCE afeta vários sistemas de órgãos. Monitore e trate a agitação e as convulsões com os medicamentos apropriados. Monitore e trate a hipoglicemia. Avalie a gasometria, o soro, os eletrólitos e o cálcio. Corrija as desordens metabólicas, observando que o tratamento da acidose metabólica é realizado melhor quando a causa subjacente da acidose é tratada (ou seja, restaure a perfusão quando em choque). Forneça controle direcionado da temperatura: considere hipotermia terapêutica para crianças que permaneçam comatosas e previna ou trate agressivamente a febre. Providencie a transferência para uma UTI pediátrica apropriada.
Administrar fluidos de manutenção
Composição do fluido de manutenção
Após a estabilização inicial, ajuste a taxa e a composição dos fluidos IV segundo o estado do paciente. Se a função cardiovascular estiver adequada, considere administrar fluidos de manutenção depois que o volume intravascular tiver sido restaurado e os déficits de fluido tiverem sido repostos. Ao calcular a necessidade de fluido de manutenção e planejar a administração de fluido, inclua o fluido administrado com infusões de fármacos vasoativos.
Nas primeiras horas após a ressuscitação, a composição apropriada de fluidos IV é um cristaloide isotônico (0,9% de Na CI ou lactato de Ringer), com ou sem dextrose, com base no quadro e na idade da criança. Evite fluidos hipotônicos em crianças gravemente enfermas na fase pós-PCR. Evidências recentes sugerem que soluções tampão (p. ex., lactato de Ringer ou outra solução isotônica que contenha eletrólitos) podem ser preferidas, pois a hipercloremia tem sido associada a resultados piores.
No entanto, se usar uma dessas soluções, você precisará garantir que a criança esteja recebendo alguma fonte de dextrose, pois a hipoglicemia provavelmente ocorrerá.
É possível adicionar componentes específicos aos fluidos de manutenção, de acordo com a condição clínica:
Inclua dextrose nos fluidos IV para bebês e crianças hipoglicêmicos ou com risco de hipoglicemia. Adicione cloreto de potássio (KCI), 1 O mEq/L a 20 mEq/L para crianças com função renal adequada e débito urinário documentado, assim que for possível fazer o monitoramento periódico de potássio. Não adicione KCI ao fluido de manutenção de crianças com hipercalemia, insuficiência renal, lesão muscular ou acidose intensa.
MÉTODOS
Trata-se de uma revisão narrativa sobre os aspectos da parada cardio respiratória em crianças e suporte avançado de vida pediátrico, para tal fim, realizou-se um levantamento bibliográfico a partir da base de dados “Lillacs”, sendo incluídos os seguintes termos para direcionar a pesquisa: “parada cardiorrespiratória em crianças, suporte avançado de vida pediátrico, PCR, RCP, RCE.
Os critérios de inclusão para a seleção dos estudos, adotaram-se: (a) artigos nos idiomas português, espanhol e inglês; (b) estudos de revisão de literatura ou de revisão sistemática; (c) ano de publicação de janeiro de 2020 a setembro de 2025; (d) relevância do estudo; (e) presença dos termos “PCR, RCP, suporte avançado de vida pediátrico” no título e/ou resumo científico. Com relação aos critérios de exclusão, foram levados em consideração: (a) estudos não relacionados ao tema; (b) artigos publicados anteriormente ao ano de 2020; (c) artigos que não contemplem os demais critérios de inclusão. Assim, foram levantados trinta e cinco artigos, restando apenas 10 selecionados para esta revisão de literatura após a utilização dos critérios de elegibilidade descritos.
CONCLUSÃO
A abordagem da criança na emergência é um tema de extrema importância, visto que demanda ações rápidas e eficazes para garantir o melhor atendimento possível em situações críticas.
A metodologia adotada para explorar essa temática foi cuidadosamente estruturada, visando fornecer informações precisas e atualizadas.
O levantamento bibliográfico permitiu a coleta de informações provenientes de diversas fontes confiáveis, incluindo literatura científica, artigos, manuais e diretrizes. A incorporação de documentos oficiais e diretrizes emitidas por organizações renomadas, como a AHA, PALS, acrescentou uma camada adicional de autoridade às informações obtidas.
A análise e síntese das informações coletadas permitiram identificar as principais práticas e diretrizes recomendadas para a abordagem da criança na emergência. A validação das fontes utilizadas foi um aspecto crítico da metodologia, garantindo a credibilidade e relevância das informações apresentadas. O resultado desse processo é um conjunto de orientações confiáveis que podem impactar positivamente a abordagem da criança na emergência, visando sempre o bem-estar e a segurança das crianças em situações críticas.
REFERÊNCIAS
Edição de e-book Português, 2021 American Heart associations.ISBN: 978-161669958-1.20-2225.
18.ed.Medicina de emergência : abordagem prática / editores Ludhmila Abrahão Hajjar … [et al.]. – 18. ed., rev. eatual. – Santana de Parnaíba [SP] : Manole, 2024.
American Heart Association. Destaques das Diretrizes de RCP e ACE de 2020 da American Heart Association. Disponível em: https://cpr.heart.org/-/media/cprfiles/cpr-guidelinesfiles/ highlights/hghlghts_2020eccguidelines_portuguese.pdf. Andersen LW, Berg KM, Saidon BZ, et al.; American Heart Association Get With The Guidelines –Resuscitation Investigators. Time to epinephrine after pediatric inhospital cardiac arrest. JAMA 2015;314(8):802-10.
Atkins DL, Everson-Stewart S, Sears GK, et al. Epidemiology and outcomes from out-of-hospitalcardiac arrest in children: the Resuscitation Outcomes Consortium Epistry-Cardiac Arrest. Circulation. 2009;119:1484-91.
Aufderheide TP, Pirrallo RG, Yannopoulos D, et al. Incomplete chest wall decompression: a clinical evaluation of CPR performance by EMS personnel and assessment of alternative manual chest compression-decompression techniques. Resuscitation. 2005;64:353-62.
Berg KM, Bray JE, Ng KC, et al. 2023 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations: Summary From the Basic Life Support; Advanced Life Support; Pediatric Life Support; Neonatal Life Support; Education, Implementation, and Teams; and First Aid Task Forces. Circulation. 2023 Dec 12;148(24):e187-e280.
Berg RA, Sanders AB, Kern KB, et al. Adverse hemodynamic effects of interrupting chest compressions for rescue breathing during cardiopulmonary resuscitation for ventricular fibrillation cardiac arrest. Circulation. 2001;104:2465-70.
Chang CY, Wu PH, Hsiao CT, et al. Sodium bicarbonate administration during inhospital pediatric cardiac arrest: A systematic review and meta-analysis. Resuscitation. 2021;162:188-97.
Girota S, Spertus J, Li Y, et al. American Heart Association Get With The Guidelines – Resuscitation Investigators l. Survival trends in pediatric in-hospital cardiac arrests: an analysis from get with the guidelines. Resusc Circ Cardiovasc Qual Outcomes. 2013;6(1):42-9.
Agency for Healthcare Research and Quality. Overview of pediatric emergency department visits, 2015. HCUP Statistical Brief #242 (August 2018). https://hcupus.ahrq.gov/reports/statbriefs/sb242-Pediatric-EDVisits-2015.jsp (accessed 2020 DEZ 10)ASSOCIATION, American Heart.
Suporte Avançado de Vida em Pediatria: Manual do Profissional. 3. ed. Rio de Janeiro: American Academy of Pediatric, 2017. p. 29-66 American Academy of Pediatrics, and American College of Emergency Physicians. Continuing medical education. American Academy of Pediatrics; 2017.
Available from: http://www.aap.org/en-us/continuing-medical-education/lifesupport/Pages/Life-Support.aspx [cited 30.03.17Benito J, Luaces-Cubells C, Mintegi S, Manrique Martínez I, De la Torre Espí M, Miguez Navarro C, et al. Evaluation and impact of the ‘Advanced Pediatric Life Support’ course in the care of pediatric emergencies in Spain.
Pediatr Emerg Care. 2017, http://dx.doi.org/10.1097/PEC.0000000000001038.DAVIS AL, Carcillo JA, Aneja RK et al. American College of Critical Care Medicine clinical practice parameters for hemodynamic support of pediatric and neonatal septic shock. Crit Care Med. 2017; 45:1061-93
