REGISTRO DOI: 10.69849/revistaft/cl10202508221728
Romero Bezerra Cavalcanti Mendes
Orientador: Prof. Dr. Epitácio Leite Rolim Filho
RESUMO
Introdução: A Síndrome Congênita do Zika vírus (SCZV) é caracterizada por muitas deficiências, especialmente no sistema nervoso central, potencialmente comprometendo o neurodesenvolvimento e causando morbidez nas articulações das mãos e punho significativa em crianças afetadas. Objetivo: Foi avaliar as alterações morfofuncionais nas mãos e punhos de crianças com síndrome congênita do Zika vírus, menores de sete anos de idade. Métodos: Esta foi uma investigação observacional transversal aninhada dentro de um estudo de coorte prospectivo de crianças diagnosticadas com o SCZV, com base num hospital de referência no Centro de Referência em Doenças Raras (RARUS), o qual realiza atendimento a crianças com microcefalia no Hospital Maria Lucinda, Recife, Pernambuco, no período entre 2020 e 2022. Realizámos avaliações da criança com microcefalia e morfofuncional através de um protocolo de semiologia da mão para medição da inspeção estática, esqueleto e movimento. Resultados: A amostra do estudo incluiu 23 crianças, Conclusão: Dado o caráter inédito do presente estudo, a interlocução com a literatura ficou comprometida em razão da não localização de outros estudos focalizando alterações nas mãos e punhos em crianças SCZV. Mesmo considerando-se estudos envolvendo a população em geral nesta faixa etária ou outros grupos, portadores de condições distintas, prevaleceu a escassez de publicações atualizadas e relevantes do ponto de vista epidemiológico, o que representou mais um desafio na condução desta pesquisa. Neste caso específico, estima-se como fundamental a condução de estudos longitudinais que deem conta da observação do processo de desenvolvimento destas crianças, garantindo a intervenção precoce e adequada, de forma a minimizar o sofrimento das crianças e de suas famílias e oportunizar uma atuação multiprofissional pertinente e efetiva.
Palavras-chave: Microcefalia. Mão. Punho. Criança. Síndrome Congênita do Zika vírus.
ABSTRACT
Introduction: Congenital Zika virus syndrome (CZVS) is characterized by many disabilities, especially in the central nervous system, potentially compromising neurodevelopment and causing significant hand and wrist joint morbidity in affected children. Objective: To evaluate the morphofunctional changes in the hands and wrists of children with congenital Zika virus syndrome, under seven years of age. Methods: This was a cross-sectional observational investigation nested within a prospective cohort study of children diagnosed with the SCZV, based in a referral hospital at the Reference Center for Rare Diseases (RARUS), which provides care for children with microcephaly at the Maria Lucinda Hospital, Recife, Pernambuco, in the period between 2020 and 2022. We carried out assessments of the child with microcephaly and morphofunctional assessments using a hand semiology protocol to measure static inspection, skeleton and movement. Results: The study sample included 23 children, Conclusion: Given the unprecedented nature of this study, the interlocution with the literature was compromised due to the fact that no other studies focusing on alterations in the hands and wrists in SCZV children were located. Even when considering studies involving the general population in this age group or other groups with different conditions, there was a scarcity of up-to-date and epidemiologically relevant publications, which represented yet another challenge in conducting this research. In this specific case, we believe it is essential to carry out longitudinal studies to observe the development process of these children, guaranteeing early and appropriate intervention in order to minimize the suffering of the children and their families and provide relevant and effective multi-professional action.
Keywords: Microcephaly. Hand. Wrist. Child. Congenital Zika virus syndrome.
1. INTRODUÇÃO
1.1 APRESENTAÇÃO DO PROBLEMA
A epidemia da síndrome congênita do Zika vírus (SCZV) atingiu aceleração epidêmica em todo o mundo, especialmente no Brasil. A sua associação com defeitos congênitos ao nascimento se tornaram um problema de saúde global. O aumento significativo do número de bebês com microcefalia no Nordeste do Brasil, especialmente no estado de Pernambuco, que registrou o maior número de casos no final de 2015, levou a uma mobilização maciça das autoridades de saúde. Isso resultou no decreto de emergência em saúde pública de importância nacional(1-6). Com aumento na incidência de recém-nascidos em 2016, foi confirmada a associação de casos de microcefalia e outras desordens neurológicas à SCZV(7,8), o Ministério da Saúde instituiu um sistema de notificação e investigação específico para infecções pré-natais e microcefalia fetal e neonatal relacionada principalmente do quadro clínico de natureza neurológica, em crianças com exposição vertical ao vírus Zika com o desenvolvimento de estratégias de intervenção, controle e prevenção, o espectro da síndrome foi estabelecido(9-11). O espectro da SCZV é caracterizado por múltiplas manifestações sensoriais, neurológicas e ortopédicas de gravidade variável. É possível que outras ocorrências congênitas sejam identificadas à medida que essas crianças envelhecem e com o avanço do conhecimento sobre essa síndrome(12).
A microcefalia tem sido associada ao conjunto de sequelas que constitui SCZV, os principais achados descritos envolvem predominantemente o sistema nervoso central, calcificações cerebrais, anormalidades estruturais, lesões oculares características e graus variados de alterações funcionais, como hiperexcitabilidade,, espasticidade e hipertonia. As crianças acometidas apresentam graus variados de redução do perímetro cefálico, além de desproporção crânio facial, deficiência auditiva, deficiência visual, malformações sistêmicas, deformidades articulares, alterações comportamentais e atraso do desenvolvimento, dentre outras possíveis anormalidades cerebrais em exames de neuroimagem, como calcificações corticais e subcorticais(13-18).
Alguns achados musculoesqueléticos relatados na SCZV foi a artrogripose, presente nos casos mais severos, causada tanto pela espasticidade quanto pela hipocinesia fetal(19-23), durante a prática clínica foram observadas algumas deformidades como contraturas, luxação de quadril, deformidade em pés, escoliose, entre outros(24-28). A avaliação sistemática na infância, especialmente durante os primeiros anos de vida – momento de maior neuroplasticidade – é fundamental para o entendimento das condições clínicas e possíveis repercussões sobre o desenvolvimento morfofuncionais nas mãos e punhos de crianças afetadas pelo SCZV. Faz-se necessário estudar suas manifestações e evolução clínica, bem como os fatores de risco ou associado estabelecido pela condição de exposição pelo SCZV. Embora geral, as deformidades pediátricas da mão e do punho podem ocorrer isoladamente ou como parte de uma síndrome maior. É importante ser capaz de reconhecer essas condições para fornecer recomendações de tratamento apropriadas e encaminhar o paciente para avaliação médica ou genética quando necessário. Existem algumas implicações congênitas de mão e punho que devem ser entendidas, pois muitas vezes direcionam o tipo de tratamento indicado.
Neste contexto, destaca-se a necessidade de acompanhamento longitudinal desta população, em especial quanto à sua evolução neuropsicomotor, desenvolvimento das limitações osteoarticulares e consequentes limitações impostas à vida utilizando-se protocolos de avaliação semiológica para mãos e punhos, devido a importante influência anatômica e funcional da atitude congênita do punho em relação às mãos(29). Assim, faltam informações relevantes sobre estudo desenvolvido para mapear, delimitando todas as alterações morfofuncionais nas mãos de crianças afetadas pelo SCZV em Pernambuco.
Há, porém, na literatura uma escassez acentuada de dados acerca da natureza das deformidades ortopédicas relacionadas à mão e punho na população pediátrica, com poucos estudos, de pequeno porte, sendo necessário um novo estudo classificando e quantificando as deformidades ortopédicas na SCZIKV. Contraturas e deformidades musculoesqueléticas em pacientes com espasticidade cerebral são relacionadas a aumento da dor e diminuição da qualidade de vida, portanto faz-se necessária uma melhor compreensão da fisiopatologia dessas deformidades, que começa pela descrição e classificação das mesmas. O presente estudo é a descrição de deformidades musculoesqueléticas mais extenso presente na literatura.
1.2 JUSTIFICATIVA
Um número crescente de infecções congênitas pelo vírus Zika com deformidades musculoesqueléticas têm sido diagnosticado em todo o mundo, no entanto, reabre toda uma discussão no conhecimento sobre essa infecção, seu mecanismo associado, momento de transmissão e descrição de achados clínicos como sinais e sintomas. Esta pesquisa possibilitará que sejam gerados subsídios técnicos para a correta avaliação clínica e acompanhamento de crianças com SCZV, sobretudo quanto às suas habilidades morfofuncionais com as mãos e punho. Consequentemente, possibilitará uma intervenção multidisciplinar apropriada, com a implementação de práticas educativas às famílias e de intervenção precoce, focada nas possíveis complicações dessa população específica, bem como na adoção de programas de saúde e educação preventivos de âmbito social e estabelecimento de procedimentos cirúrgicos ou clínico para melhora da qualidade de vida na população infantil. Portanto, ortopedistas pediátricos e cirurgiões de mão devem ter conhecimento do crescimento normal do punho em crianças e adolescentes para serem capazes de diferenciar o crescimento normal do patológico.
1.3 OBJETIVOS
1.3.1 Objetivo geral
▪ Avaliar as alterações morfofuncionais nas mãos e punhos de crianças com síndrome congênita do Zika vírus, menores de sete anos de idade.
1.3.2 Objetivos específicos
- Avaliar as características demográficas (idade e sexo);
- Avaliar as articulações do punho e mão quanto a flexão, extensão e desvios, através da goniometria;
- Avaliar eminências volares (tenar e hipotênar), quanto ao trofismo; ▪ Investigar a morfologia em relação à posição da mão em fase neutra; ▪ Avaliar a funcionalidade da mão (mobilidade ativa e passiva).
2. LITERATURA
2.1 SÍDROME CONGÊNITA DO ZIKA VÍRUS E MICROCEFALIA: TRASMISSÃO E EPIDEMIOLOGIA
O vírus Zika é transmitido às pessoas principalmente através da picada de um mosquito da espécie Aedes infectado (Ae. aegypti e Ae. albopictus), e também pode ser transmitido por relações sexuais e durante a gravidez, da mãe para o feto(2231). Pesquisadores indicam que é um vírus de RNA de sentido positivo de fita simples que pertence ao gênero Flavivirus, isso pode ser devido à ligação do genoma do RNA viral à proteína de ligação ao RNA Musashi-1 que está envolvida no neurodesenvolvimento e é altamente expressa nesses neurônios precursores. Múltiplas estratégias permitem que o ZIKV evite as respostas imunes inatas do hospedeiro para permitir a disseminação para a placenta da mãe e atravessar a barreira sangue-líquido cefalorraquidiano no plexo coroide e a barreira hematoencefálica do feto. Como muitos bebês cujas mães são infectadas pelo genoma ZIKV durante a gravidez, esse é composto por um RNA de fita simples positivo que codifica três proteínas estruturais, cápside, pré-membrana e envelope, que podendo desenvolver problemas neurológicos mais tarde na vida, o monitoramento a longo prazo dessas crianças pequenas é essencial. A avaliação sistemática na infância, principalmente nos primeiros anos de vida – momento de maior neuroplasticidade – é fundamental para a compreensão das condições clínicas e possíveis repercussões no desenvolvimento infantil(32-34).
A SCZV é uma infecção congênita emergente, resultando em graves danos ao sistema nervoso central. O aumento da disseminação do Zika vírus foi acompanhado por crescentes casos de microcefalia, bem como, outras anormalidades, chamadas de SCZV e infecção por Zika na gravidez, incluindo lesões cerebrais, audição, anormalidades visuais, cardiovasculares e musculoesqueléticas de gravidade variável microcefalia. Esses sinais e sintomas estão associados a um comprometimento geral do desenvolvimento, e a gravidade parece correlacionar-se com o momento da infecção na mãe, sendo mais grave no primeiro trimestre(12,13,18-23,35-39).
2.2 DEFORMIDADES E ESPASTICIDADE MUSCULOESQUELÉTICAS EM CRIANÇAS COM MICROCEFALIA SECUNDÁRIA À SCZV
A Síndrome Congênita do Zika SCZV é uma condição caracterizada pela presença de anormalidades no sistema nervoso central (SNC). Essas características podem impactar negativamente o desenvolvimento neurológico das crianças afetadas, resultando em significativa morbidade. As manifestações sensoriais e motoras observadas na SCZ são semelhantes às encontradas em crianças com paralisia cerebral (PC), que também enfrentam restrições musculoesqueléticas e neurais que afetam a aquisição de habilidades funcionais. As alterações motoras na SCZ frequentemente estão associadas a distúrbios cognitivos, de comunicação e comportamentais, o que pode dificultar o alcance dos marcos de desenvolvimento típicos na infância(38-44).
A síndrome congênita do Zika vírus engloba uma grande variedade de anormalidades neurológicas observadas em recém-nascidos que adquiriram o Zika vírus no útero como deformidades musculoesqueléticas(19-23,26-28,30). Comumente, deformidades não progressivas neurológicas fetais resultam em um grupo de desordens permanentes que afetam o sistema neuromuscular e musculoesquelético, levando a alterações na aquisição das habilidades motoras típicas, na postura, no tônus muscular, além de encurtamentos e deformidades ósseas que impedem a aquisição dos marcos do desenvolvimento(42,43). Um dos primeiros achados musculoesqueléticos relatados na SCZV foi entre artrogripose. Contraturas congênitas envolvendo uma ou múltiplas articulações, ou seja, artrogripose múltipla congênita ou artrogripose foram relatadas em fetos e lactentes com infecção congênita por ZIKV presumida ou confirmada laboratorialmente. O quadro clínico das contraturas congênitas varia entre os lactentes afetados em relação ao tipo (proximal ou distal), lateralidade, membro superior ou inferior e gravidade, provavelmente refletindo variações no dano neurológico(19).
A artrogripose generalizada é uma complicação séria que afeta até 7% das crianças com SCZV. Esta condição é caracterizada por uma rigidez persistente das articulações em todo o corpo. Além disso, a artrogripose predominantemente distal é observada em mais de 10% das crianças afetadas, afetando principalmente as articulações menores dos punhos, tornozelos, mãos e pés(31,45,46). Essas crianças frequentemente apresentam pé torto e outras posições anormais dos pés, bem como restrição dos movimentos das mãos e contraturas em flexão dos dedos (camptodactilias), como relatado por del Campo et al.(46) (2017).
Figura 1 – Características físicas dismórficas características da SCZV: A) Posição pescoço de cisne do segundo dedo causada por hiperextensão distônica; B) Contraturas generalizadas de grandes e pequenas articulações; C) Contraturas de todos os dedos; D) Postura dos dedos em ―pescoço de cisne‖; E) Extensão simultânea das articulações metacarpofalângicas dos dedos polegar, indicador e mínimo, com flexão das articulações metacarpofalângicas dos dedos médio e anular
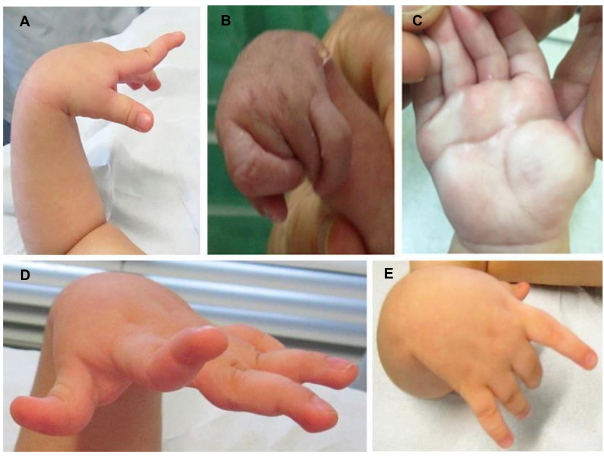
Fonte: van der Linden et al.,(36); Moura da Silva et al.(45) e del Campos et al.,(46)
A artrogripose não é um diagnóstico específico, mas é a caracterização clínica da presença de múltiplas contraturas articulares ao nascimento em segmentos corpóreos. Dentre as diversas possíveis causas, os distúrbios neurológicos são a principal hipótese para o seu surgimento, devido à redução da ativação dos neurônios motores da via piramidal da medula espinhal, ou pelo efeito direto sobre neurônios motores da medula espinhal, contribuindo para hipomotilidade fetal(20). Não foram encontradas deformidades em coluna vertebral ou articulações à investigação imaginológica, mas o estudo eletromiográfico evidenciou sinais moderados de remodelação das unidades motoras e um padrão de recrutamento reduzido, podendo corroborar com a contribuição da malformação neuronal como causa das alterações osteomusculares(10,22).
2.3 MANIFESTAÇÕES CLÍNICAS E NÍVEL MORFOFUNCIONAL MOTORA EM CRIANÇAS COM SCZV
Uma das manifestações clínicas comuns observadas em crianças é a microcefalia, uma condição na qual a cabeça e o cérebro do bebê são significativamente menores do que o esperado para a idade e sexo. No entanto, a microcefalia é apenas um dos muitos desfechos adversos associados à infecção. A exposição ao ZIKV no útero pode também resultar em várias outras anormalidades neurológicas e desafios no desenvolvimento neurológico, estendendo-se para além do tamanho reduzido da cabeça e do comprometimento cerebral estrutural. Além da microcefalia, crianças infectadas congenitamente pelo ZIKV podem apresentar uma gama de outras características clínicas, incluindo, mas não se limitando a:(10,40,47-55)
❖ Epilepsia: Transtornos convulsivos que podem variar em frequência e gravidade, afetando significativamente a qualidade de vida e requerendo manejo clínico específico.
❖ Disfagia: Dificuldades na deglutição que podem afetar a nutrição e o desenvolvimento da criança, além de aumentar o risco de aspiração e infecções respiratórias.
❖ Deficiências auditiva e visual: Problemas sensoriais que podem impactar a capacidade da criança de interagir com o ambiente, comunicar-se efetivamente e aprender.
❖ Anomalias osteoarticulares: Alterações nos ossos e articulações que podem afetar a mobilidade e a postura, exigindo frequentemente intervenções ortopédicas e fisioterapêuticas.
A SCZV é, portanto, um espectro de defeitos estruturais e deficiências funcionais resultantes da infecção fetal pelo ZIKV, refletindo a severidade e a variedade dos impactos que o vírus pode ter no desenvolvimento fetal(56). O reconhecimento e a descrição da SCZV são essenciais para o diagnóstico adequado, o manejo clínico e o suporte às famílias afetadas, assim como para a formulação de políticas de saúde pública visando à prevenção e ao tratamento dessas condições.
O ZIKV é intensamente neurotrópico. Infecções congênitas com ZIKV podem interromper a embriogênese cerebral e resultar não apenas em microcefalia (MC), mas também em uma série de anormalidades neurológicas e do neurodesenvolvimento. Outras características clínicas comuns observadas em crianças congenitamente infectadas pelo ZIKV incluem epilepsia, disfagia, deficiência auditiva e visual e anormalidades osteoarticulares. Esse amplo espectro de defeitos estruturais e deficiências funcionais é reconhecido coletivamente como
SCZV(12,14). Embora as características do comprometimento do SNC em crianças com SCZV, especialmente alterações no tônus e postura consistentes com as de crianças com paralisia cerebral (PC)(12), sejam cada vez mais bem descritas, os prejuízos funcionais relacionados à SCZ e suas evolução ao longo do tempo permanecem em grande parte desconhecidas. Atualmente, não existem estudos quantitativos descrevendo o impacto da SCZ no desempenho motor grosso ao longo
do tempo.
À medida que as crianças com SCZV crescem, é crucial monitorar seu
desenvolvimento motor utilizando ferramentas de avaliação padronizadas(40,57). O Gross Motor Function Measure (GMFM) foi especificamente desenvolvido para avaliar mudanças longitudinais na função motora grossa em crianças afetadas pela SCZV. Ao ser utilizado em conjunto com o GMFCS, essas medidas fornecem informações valiosas sobre o prognóstico motor e orientam o manejo clínico das
crianças com SCZV(57). Essas avaliações ajudam os profissionais de saúde a entender o progresso motor das crianças ao longo do tempo e a adaptar as intervenções conforme necessário para otimizar seu desenvolvimento e qualidade de vida.
Durante a avaliação do elevado número de casos de recém-nascidos com microcefalia foram observadas inúmeras alterações clínicas e anatômicas nos pacientes portadores da doença. Crianças com comprometimento neurológico podem apresentar alteração de tônus em todo o corpo ou alguns segmentos corporais, afetando a postura e o movimento. Nos casos em que a criança apresente hipertonia (espasticidade), pode ocorrer o surgimento de deformidades
osteomusculares, principalmente no cotovelo, que permanece fletido longos períodos; no punho, com flexão e desvio ulnar; nos dedos que ficam também fletidos e no polegar que, muitas vezes, permanece fletido, aduzido e empalmado. A avaliação da espasticidade é muito importante no contexto clínico para orientar o paciente na intervenção mais adequada e quantificar seus resultados, sendo possível avaliar os efeitos da reabilitação, atualmente os mais utilizados são escalas
descritivas, que por sua vez dependem da expertise de cada terapeuta(54,55).
Considerando que a Síndrome Congênita do Zika Vírus provoca alterações no SNC e no Desenvolvimento Neuropsicomotor (DNPM), crianças que apresentam esse diagnóstico tendem a apresentar um desenvolvimento atípico e, portanto, déficit na funcionalidade. Diante disso, faz-se relevante conhecer e utilizar marcadores que ajudem a compreender e identificar o nível funcional motor e as características do controle do osteomuscular apresentadas por esses infantes.
3. MÉTODOS
3.1 POPULAÇÃO E LOCAL DE ESTUDO
Foram avaliadas crianças, diagnosticadas com síndrome congênita do Zika vírus, através do exame de sorologia ao nascimento, no período entre 2020 e 2022, no Centro de Referência em Doenças Raras (RARUS), o qual realiza atendimento a crianças com microcefalia no Hospital Maria Lucinda, Recife, Pernambuco.
3.2 DESENHO DO ESTUDO
Trata-se de um estudo observacional transversal.
3.3 CRITÉRIO DE INCLUSÃO
- Crianças afetadas pelo ZIKA Vírus confirmado através do exame de sorologia ao nascimento;
- Com e sem alterações morfofuncionais nas mãos e punhos;
3.4 CRITÉRIOS DE EXCLUSÃO
- Crianças com microcefalia congênita devido a causas genéticas e/ou infecções de outra etiologia conhecida (Toxoplasmose, Rubéola, Citomegalovirose, Herpes, Lues e HIV).
3.5 SELEÇÃO DA AMOSTRA
A amostra foi composta de 23 crianças de ambos os sexos, entre 3 e 7 anos de idade, nascidos com síndrome congênita do Zika vírus, provenientes do Centro de Referência em Doenças Raras (RARUS), que conta com atendimento de neurologista, neuropediatra, ortopedia pediátrica, fisioterapeuta e outros serviços.
3.6 PROCEDIMENTOS TÉCNICOS
3.6.1 Avaliação de crianças com microcefalia
A avaliação de crianças com microcefalia, definida como perímetro cefálico (PC) ≤ 32 cm ao nascimento para idade gestacional de 37 a 42 semanas, foi usada para sugerir infecção congênita associada ao Zika vírus. O diagnóstico de microcefalia foi baseado em ultrassonografia durante a gestação ou ao nascimento, bem como na presença de desproporção crânio-facial. A microcefalia foi confirmada com PC 2 desvios padrão abaixo da média para idade gestacional e sexo, de acordo com a curva de Fenton(63). Exames laboratoriais excluíram infecções por citomegalovírus, rubéola, toxoplasmose e HIV. As crianças com microcefalia confirmada por escore z ≤ -2 DP e alterações típicas em exames de imagem ultrassonografia ou tomografia) foram convidadas a participar do estudo. A definição de Síndrome Congênita do Zika (SZCV) foi baseada nas especificações de França et al.(63):

3.6.2 Avaliação e diagnóstico morfofuncionais das mãos e punhos
Os padrões morfofuncionais são aqueles padrões de movimentos permitidos pela anatomia da mão, com menor probabilidade de gerar estresse para a articulação, como por exemplo: extensão do punho com flexão de dedos, flexões de punho com extensão de dedos, extensão de punho com desvio radial, flexão de punho com desvio ulnar.
A avaliação ortopédica foi realizada especificamente nas mãos e punhos dos pacientes com microcefalia, através de exames físico:
Figura 2 – A avaliação da goniometria e articulação das mãos e punhos dos pacientes
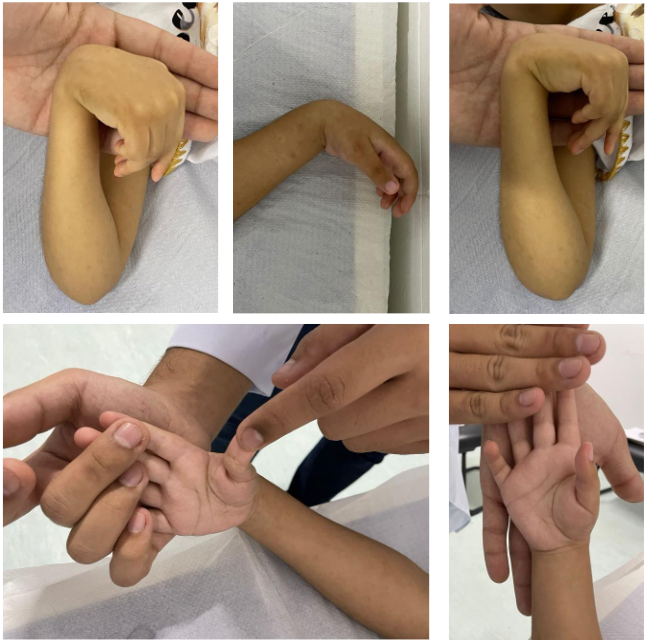
Quadro 1 – Protocolo de semiologia da mão para pesquisa(29,59)
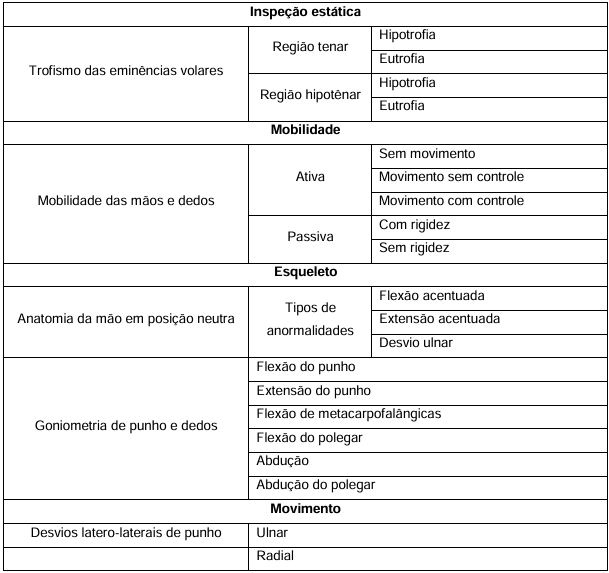
Figura 3 – Avaliação da amplitude de movimentos medido os ângulos através do goniômetro.
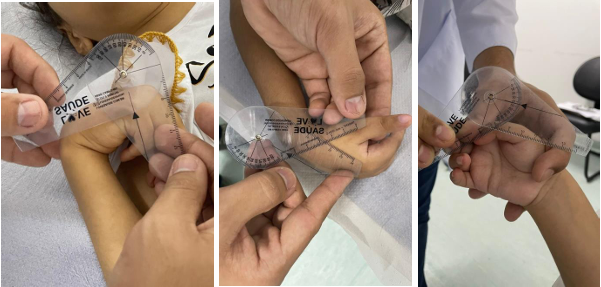
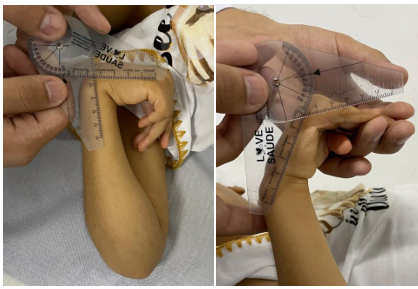
3.7 INSTRUMENTOS DE COLETA DE DADOS
A coleta teve início com o primeiro paciente que preencheu os critérios de inclusão da pesquisa, atendido no serviço selecionado ou já cadastrado.
O tamanho da amostra foi calculado com base na prevalência de outras doenças infecciosas congênitas que cursam com alterações morfofuncionais nos membros superiores.
3.8 RISCO
Durante o preenchimento dos questionários você poderá se sentir constrangido, mas esse risco será minimizado pelo fato de que a qualquer momento a sua participação na pesquisa pode ser encerrada. Caso haja dano decorrente da pesquisa o pesquisador principal se compromete a prover ressarcimento e indenização relativos aos danos causados devido a participação na pesquisa. Existe risco de vazamento de dados e perda de confidencialidade, o mesmo será minimizado devido ao fato de que os seus dados serão guardados em computador pessoal protegido por senha.
3.9 BENEFÍCIOS
A pesquisa irá ajudar primeiramente na avaliação da melhora, das mãos e punhos da criança afetada pela doença pode, está pesquisa possibilitará que sejam gerados melhora significante para acompanhamento de crianças com Síndrome de Zika congênita, sobretudo quanto às suas habilidades motoras com as mãos, ajudando no estado geral do seu filho (dor, movimentação, atividades do dia-a-dia). Além disso, por participar em uma pesquisa sobre tratamento de uma complicação da síndrome congênita do zika vírus você estará colaborando com o desenvolvimento de conhecimento sobre o tratamento de crianças como seu filho. Por fim, os dados gerados por esta pesquisa, especialmente o questionário sobre qualidade de vida, servirão para que possamos conhecer melhor as necessidades suas e de seu filho, ajudando na sua reabilitação.
3.10 PROCEDIMENTOS ANALÍTICOS
Os dados serão analisados no software Statistical Package for the Social Sciences (SPSS) – versão 13. A análise estatística descritiva dos dados será efetivada por meio do cálculo das frequências relativas e absolutas, média e desvio padrão ou mediana, conforme padrão de normalidade da variável, avaliada pelo teste de Kolmogorov-Smirnov. As correlações entre variáveis nominais e contínuas foram realizadas através do teste U de Mann-Whitney. Já entre as variáveis contínuas, foi utilizada regressão linear simples, com análise de variância (ANOVA). Para análise correlacionar a presença e ausência das deformidades ortopédicas entre os pacientes do 1º trimestre gestacional com os dos demais, foi utilizado o teste exato de Fisher, de uma cauda
3.11 ASPECTOS ÉTICOS
O projeto aprovado pelo Comitê de Ética em Pesquisa em Seres Humanos do Centro de Ciências da Saúde da UFPE para análise e aprovação, como também seguirá os princípios que regem o Código de Ética Médica vigente, na Resolução 466/12 do Conselho Nacional de Saúde-CONEP (ANEXO B).
Os pais ou responsáveis pelas crianças foram informados sobre os objetivos da pesquisa, os riscos e benefícios da mesma, quando então foi solicitado o seu consentimento para participar da mesma e para a realização da coleta de dados, fotografias e filmagens (APÊNDICES A e B). Foram explicados os benefícios da pesquisa quanto à importância da avaliação das alterações morfofuncionais das mãos existentes para o desenvolvimento do seu filho que será encaminhado para avaliação com um especialista se houver necessidade e da possibilidade de incrementos nas possibilidades terapêuticas. A mãe foi informada que a sua participação e a do seu filho é voluntária, e caso não aceite participar, isto não trará nenhum prejuízo em seu atendimento no hospital de referência.
4. RESULTADOS
4.1 CARACTERÍSTICAS DOS PACIENTES
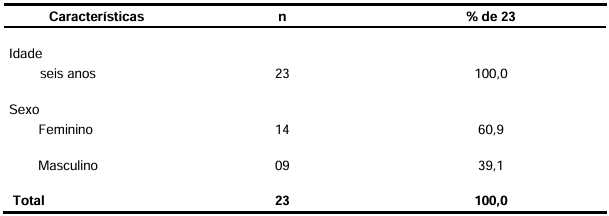
Demografia dos pacientes: Ao todo, foram avaliadas 23 crianças portadoras da SCZV, todas apresentavam seis anos de idade, 14 (60,9%) eram do sexo feminino e 9 (39,1%) do sexo masculino, como apresentado na tabela 1.
Tabela 1 – Características demográficas dos pacientes
4.2 TROFISMO DE EMINÊNCIAS VOLARES
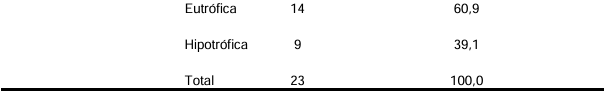
A análise do trofismo das eminências volares dos 23 pacientes com SCZV revelou que 10 crianças (43,5%) apresentavam hipotrofia na região tênar, enquanto 13 (56,5%) apresentavam essa região eutrófica. Na região hipotênar, 9 crianças (39,1%) apresentavam hipotrofia, enquanto 14 (60,9%) tinham essa região eutrófica. Essas observações indicam que uma parcela significativa dos pacientes apresenta algum grau de hipotrofia nas eminências volares, o que pode impactar a funcionalidade das mãos e a capacidade de realizar atividades diárias.
Tabela 2 – Trofismo de eminências volares.

Avaliação morfofuncional
- Região tênar: Hipotrofia: a presença de hipotrofia em 43,5% dos pacientes na região tênar sugere uma fraqueza no músculo responsável pela oposição do polegar, que é crucial para a preensão e manipulação de objetos; Eutrofia: os 56,5% dos pacientes com eutrofia têm uma vantagem funcional, mantendo uma melhor capacidade de preensão;
- Região hipotênar: Hipotrofia: a hipotrofia em 39,1% dos pacientes na região hipotênar pode indicar uma fraqueza nos músculos responsáveis pelo movimento do dedo mínimo, afetando a estabilidade e a destreza da mão; Eutrofia: os 60,9% dos pacientes com eutrofia na região hipotênar têm uma melhor funcionalidade global da mão.
4.3 ANATOMIA DA MÃO EM POSIÇÃO NEUTRA
Em relação a anatomia da mão em posição neutra, dos 23 pacientes avaliados, 12 (47,83%) apresentavam alguma anormalidade, sendo que 6 (26,09%) apresentavam flexão acentuada, 3 (13,04%) apresentavam extensão acentuada e 2 (8,70%) apresentavam desvio ulnar, como maior característica da mão em posição neutra, como mostra a tabela 3.
Tabela 3 – Anatomia da mão em posição neutra

Avaliação morfofuncional
Tipos de Anormalidades
- Flexão acentuada (26,09%): Impacto morfofuncional – a flexão acentuada pode limitar a capacidade de estender completamente os dedos, afetando a preensão de objetos maiores e a realização de tarefas que requerem uma mão aberta. Intervenções – terapias que envolvem exercícios de extensão e o uso de órteses podem ser úteis para melhorar a amplitude de movimento;
- Extensão acentuada (13,04%): Impacto morfofuncional – a extensão acentuada pode dificultar a flexão adequada dos dedos, essencial para agarrar objetos pequenos e realizar movimentos precisos. Intervenções – terapias focadas em fortalecimento dos músculos flexores e o uso de dispositivos adaptativos podem ajudar a corrigir ou compensar essa anormalidade;
- Desvio ulnar (8,70%): Impacto morfofuncional – O desvio ulnar pode causar dificuldades na preensão e na manipulação de objetos, devido à alteração no alinhamento dos dedos. Intervenções – a correção pode envolver exercícios específicos, uso de órteses e, em casos graves, intervenções cirúrgicas.
4.4 DESVIOS LATERO-LATERAIS DE PUNHO
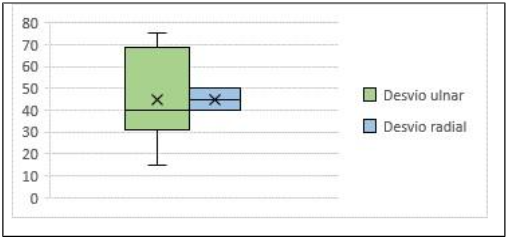
Em relação aos desvios, dos 23 pacientes estudados, 10 (53,48%) apresentavam alguma forma de desvio latero-lateral da mão, sendo 8 (34,78%) apresentavam desvio ulnar e 2 (8,70%) apresentava desvio radial, como apresentado na tabela 4. Os desvios ulnares variaram entre 15º e 75º, com a média de 45º e mediana de 40º, já os desvios radiais encontrados foram de 40º e 50º, como apresentado no gráfico 1.
Tabela 4 — Desvios latero-laterais de punho
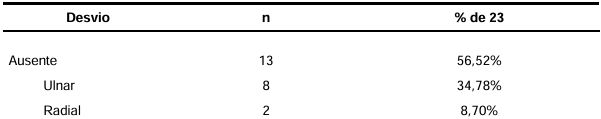

Figura 4 — Representação box plot da dispersão dos valores dos desvios encontrados
Avaliação morfofuncional
Avaliação morfofuncional
❖ Desvio Ulnar: A maior frequência de desvios ulnares (34,78%) em comparação aos radiais (8,70%) pode indicar uma tendência biomecânica ou patológica que favorece o desvio em direção à ulna. A ampla variação dos ângulos de desvio ulnar destaca a necessidade de uma abordagem individualizada para o diagnóstico e tratamento.
❖ Desvio Radial: Embora menos frequentes, os desvios radiais de 40º e 50º ainda representam um desafio clínico significativo, necessitando de atenção especial no manejo terapêutico.
4.5 MOBILIDADE DAS MÃOS E DEDOS
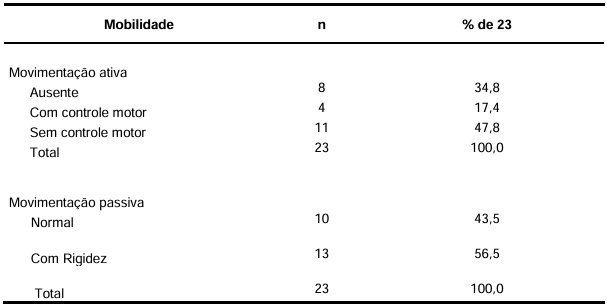
Em relação à mobilidade ativa das mãos, dos 23 pacientes estudados, 8 (34,8%), não conseguiam mover ativamente a mão, 11 (47,8%) conseguiam movê-la, sem controle motor e apenas 4 (17,4%) conseguiam mover a mão com bom controle motor, como mostrado na tabela 5.
Já em relação à movimentação passiva, todos os 23 pacientes possuíam mobilidade passiva, sendo que 13 deles (56,5%) apresentavam algum grau de rigidez ao movimento, como mostrado na tabela 5.
Tabela 5 – Mobilidade de mão e dedos
Avaliação morfofuncional
Mobilidade Ativa
- Sem Movimento (34,8%): Impacto morfofuncional – a incapacidade de mover ativamente a mão indica uma severa limitação funcional, impedindo a realização de qualquer atividade que envolva o uso da mão. Intervenções – terapias intensivas, incluindo fisioterapia e terapia ocupacional, podem ser necessárias para estimular qualquer potencial de movimento e prevenir contraturas;
- Movimento sem Controle (47,8%): Impacto morfofuncional – a capacidade de mover a mão sem controle motor adequado compromete a precisão e a eficiência das tarefas manuais. Intervenções – treinamento motor específico e técnicas de reeducação neuromuscular podem ajudar a melhorar o controle motor;
- Movimento com Controle (17,4%): Impacto morfofuncional – apenas uma pequena fração dos pacientes tem movimento ativo com bom controle motor, permitindo uma funcionalidade relativamente normal. Intervenções – manutenção do controle motor através de exercícios regulares e terapia para prevenir a regressão funcional.
Mobilidade Passiva
- Com rigidez (56,5%): Impacto morfofuncional – a presença de rigidez ao movimento passivo sugere que a articulação está se tornando menos flexível, o que pode levar a deformidades e maior perda de função. Intervenções – alongamentos regulares, mobilizações articulares e uso de órteses podem ajudar a manter a amplitude de movimento e prevenir a rigidez;
- Sem rigidez (43,5%): Impacto morfofuncional – a ausência de rigidez indica que há potencial para preservar ou melhorar a mobilidade, facilitando intervenções terapêuticas. Intervenções – programas de manutenção da mobilidade através de exercícios de amplitude de movimento e atividades diárias assistidas. A análise da mobilidade das mãos e dedos é crucial para determinar o nível de assistência e as intervenções necessárias para cada paciente. A limitação na mobilidade ativa e a rigidez na mobilidade passiva são desafios significativos que requerem uma abordagem multidisciplinar para gerenciar e melhorar a funcionalidade das mãos.
4.6 GONIOMETRIA DE PUNHO E DEDOS
Em relação a amplitude de movimentos de punho e mão desses pacientes, a flexão de punho variou de 30º a 90º, com a média de 67º e mediana de 65º. Já a extensão de punho, variou de 0º a 70º, com a média de 25º e mediana de 30º. A flexão de metacarpofalângicas variou de 30º a 90º, com a média de 67º e mediana de 70º. A flexão de polegar teve no intervalo de 40º e 90º, com média de 67º e mediana de 70º. A adução e abdução do polegar variaram respectivamente entre 10º e 55º, e 10º a 50º; tiveram as médias, respectivamente de 32º e 27º, e medianas de 35º e 25º, respectivamente, como apresentado no gráfico 2.
Figura 5 – Representação box plot da dispersão dos valores da amplitude de movimentos de punho e mão dos pacientes
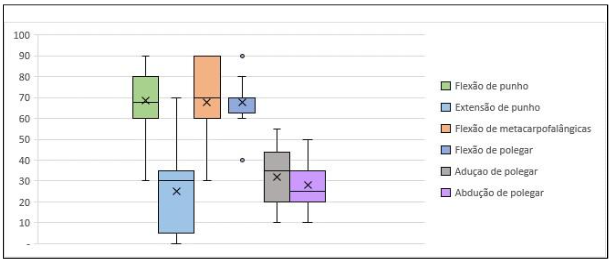
Avaliação morfofuncional
- Flexão do punho: Impacto morfofuncional – uma amplitude média de flexão de 67º indica uma funcionalidade relativamente preservada, embora a variação ampla sugira que alguns pacientes enfrentam limitações significativas. Intervenções – exercícios de alongamento e fortalecimento podem ajudar a melhorar a amplitude de movimento em pacientes com flexão limitada;
- Extensão do punho: Impacto morfofuncional – a média de 25º para a extensão do punho é relativamente baixa, o que pode comprometer a capacidade de realizar tarefas que exigem estiramento ou levantamento. Intervenções – programas de fisioterapia focados na extensão do punho podem ajudar a aumentar a amplitude de movimento;
- Flexão de metacarpofalângicas e polegar: Impacto morfofuncional – a média de 67º sugere uma boa capacidade de flexão, essencial para tarefas de preensão e manipulação de objetos. Intervenções – exercícios de flexão podem ser benéficos para manter ou aumentar essa amplitude de movimento;
- Flexão do polegar: Impacto morfofuncional – a flexão do polegar é crucial para a função de pinça e preensão fina. A média de 67º indica uma funcionalidade adequada para essas tarefas. Intervenções – exercícios específicos para o polegar podem ajudar a preservar e melhorar essa amplitude de movimento;
- Abdução: Impacto morfofuncional – A adução é importante para a capacidade de segurar objetos contra a palma da mão. A média de 32º sugere uma funcionalidade razoável. Intervenções – Exercícios de adução podem ser implementados para melhorar a estabilidade da preensão;
- Abdução do polegar: Impacto morfofuncional – A abdução do polegar é fundamental para abrir a mão e pegar objetos. A média de 27º é relativamente baixa e pode limitar a funcionalidade. Intervenções – Exercícios para aumentar a abdução do polegar são recomendados para melhorar a amplitude de movimento.
5. DISCUSSÃO
5.1 JUSTIFICATIVA DO ESTUDO: A BUSCA DO TRATAMENTO
As sequelas da microcefalia dependem de sua etiologia e da idade gestacional em que ocorreu o evento, sendo que, quanto mais precoce a afecção, mais graves serão as anomalias do sistema nervoso central (SNC)(59). As anormalidades neurológicas ocasionam repercussões importantes observadas em crianças com SCZV que incluem hipertonia espástica severa com hiperreflexia, irritabilidade e hiperexcitabilidade(55). Embora o insulto cerebral seja estático, a doença musculoesquelética é progressiva. A manifestação clínica pode variar amplamente, desde espasticidade leve na mão com inteligência normal até total dependência de cadeira de rodas, incapacidade de comunicação e falta de uso do membro superior afetado. No membro superior é evidenciada uma predominância de deformidades distais, sendo 87% das deformidades localizadas no punho e mão(60), sendo as mesmas características tanto de pacientes com espasticidade quanto de pacientes com artrogripose (camptodactilia, flexo de punho).
A atuação do Zika vírus no SNC pode causar algumas alterações, como diminuição do diâmetro da medula espinhal, microcefalia severa com crânio em aspecto de casco de tartaruga, convulsões de difícil controle, espasticidade severa, entre outros. Chama a atenção, ainda, a maior parte dos casos serem consequências de infecção durante o primeiro trimestre de gravidez, seguidos pelo segundo e terceiro trimestre, respectivamente, além da idade gestacional média de infecção de 13,22 semanas. Isso reflete ao fato de que as gestantes no primeiro trimestre de gestação são consideradas população de risco para infecção por Zika vírus, por ser a fase de formação fetal, no segundo trimestre existe o risco de malformação desencadeada pelo vírus, porém em menor grau e a partir do terceiro trimestre os riscos estão reduzidos, visto que o feto se encontra já formado(61).
Dado o caráter inédito do presente estudo, a interlocução com a literatura ficou comprometida em razão da não localização de outros estudos focalizando alterações nas mãos e punhos em crianças SCZV. Mesmo considerando-se estudos envolvendo a população em geral nesta faixa etária ou outros grupos, portadores de condições distintas, prevaleceu a escassez de publicações atualizadas e relevantes do ponto de vista epidemiológico, o que representou mais um desafio na condução desta pesquisa. Ainda assim, considera-se que estudos inéditos, descritivos e exploratórios, são fundamentais para o estabelecimento de hipóteses e fundamentação teórica metodológica para o delineamento de abordagens futuras.
5.2 LIMITAÇÃO DO ESTUDO
A principal limitação deste estudo é o pequeno tamanho da amostra. Contudo, as crianças com SZC apresentam um grau de comprometimento neurológico significativo, e usualmente não são submetidas a exames na neuroimagem de rotina, a não ser em situações de descompensação aguda ou sintomas neurológicos atípicos que demandam uma investigação diagnóstica mais aprofundada para um esclarecimento preciso(62).
Neste contexto, destaca-se a necessidade de acompanhamento longitudinal desta população, em especial quanto ao seu desenvolvimento neuropsicomotor, desenvolvimento das limitações osteoarticulares e consequentes limitações impostas à vida utilizando-se protocolos de avaliação semiológica para mãos e punhos, devido a importante influência anatômica e funcional da atitude do punho em relação às mãos(29).
5.3 AVALIAÇÃO DOS RESULTADOS
5.3.1 Características dos pacientes
Observando os dados demográficos é possível traçar algumas inferências acerca do Zika Vírus. A primeira é tendo em vista que a maioria dos pacientes inseridos no estudo teve em torno de seis anos de idade com microcefalia que apresentaram alteração neurológica, dado que contrasta com a grande incidência de deformidades musculoesqueléticas. Isso reflete o surto de 2015 ocorrido no estado de Pernambuco, de forma com que, no momento, em 2024, haja uma prevalência maior desses casos na população entre 7 e 8 anos de idade. Essa incidência precoce de deformidades contrasta marcadamente com a história natural da paralisia cerebral, apontando para um acometimento mais grave na SCZV, em concordância com a base de conhecimentos da literatura médica acerca da fisiopatologia dessa doença, que acomete tanto o sistema nervoso central quanto o periférico.
A maior proporção de meninas (60,9%) em comparação com meninos (39,1%) pode indicar uma variação no impacto do vírus entre os sexos ou pode ser um reflexo da amostra específica do estudo. Essa distribuição de gênero é interessante e pode levantar questões sobre se há uma predisposição biológica ou se fatores externos influenciam a prevalência da SCZV entre meninas e meninos. Estudos adicionais seriam necessários para determinar se essa distribuição é representativa de uma população maior ou se é uma peculiaridade desta amostra específica.
Além disso, a uniformidade na idade das crianças permite uma análise mais focada das manifestações clínicas e das necessidades de cuidados específicos para essa faixa etária. A SCZV pode ter impactos variados no desenvolvimento das crianças, e compreender as diferenças de gênero pode ajudar a personalizar as intervenções e suportes necessários.
5.3.2 Trofismo de eminências volares
Ao analisar o trofismo de eminências volares, percebe-se que uma parcela significativa dos pacientes com SCZV apresenta algum grau de hipotrofia nas eminências volares. A hipotrofia das regiões tênar e hipotênar pode impactar significativamente a funcionalidade das mãos, dificultando a realização de atividades diárias que envolvem movimentos finos e a manipulação de objetos. A presença de hipotrofia nas eminências volares é um indicador importante de comprometimento neuromuscular em crianças com SCZV. Esse comprometimento pode necessitar de intervenções terapêuticas específicas, como fisioterapia e terapia ocupacional, para melhorar a força muscular e a funcionalidade das mãos. Além disso, a identificação precoce desses sinais pode ajudar na personalização do tratamento e no planejamento de estratégias de reabilitação mais eficazes.
5.3.3 Anatomia da mão em posição neutra
A análise da posição neutra da mão revela uma alta incidência de anormalidades anatômicas entre os pacientes com SCZV, indicando que quase metade (47,83%) apresenta alguma deformidade que pode comprometer a funcionalidade das mãos. A presença dessas anormalidades anatômicas destaca a necessidade de avaliações periódicas e intervenções terapêuticas direcionadas para prevenir a progressão das deformidades e melhorar a funcionalidade das mãos.
Abordagens personalizadas, baseadas no tipo de anormalidade, podem maximizar os benefícios terapêuticos e a qualidade de vida dos pacientes.
5.3.4 Desvios latero-laterais de punho
Os desvios latero-laterais da mão são indicadores importantes de comprometimento morfofuncional em pacientes com SCZV. A identificação precoce desses desvios é fundamental, pois permite a implementação de intervenções direcionadas para corrigir ou minimizar o impacto funcional. Isso, por sua vez, melhora a qualidade de vida dos pacientes. Portanto, avaliações regulares e intervenções terapêuticas personalizadas são essenciais para gerenciar os desvios latero-laterais da mão em pacientes com SCZV. Essas medidas são cruciais para manter ou restaurar a funcionalidade das mãos, permitindo que os pacientes realizem suas atividades diárias de maneira mais eficaz e com maior independência.
5.3.5 Mobilidade das mãos e dedos
A avaliação da mobilidade das mãos e dedos destaca uma significativa limitação funcional nos pacientes com SCZV. A mobilidade ativa limitada e a presença de rigidez na mobilidade passiva têm implicações importantes para a funcionalidade diária e a qualidade de vida desses pacientes. Além de ser capaz de revelar sinais precoces de comprometimento funcional, permitindo intervenções adequadas que podem prevenir a progressão das limitações.
Compreender a extensão das limitações de mobilidade permite que os profissionais de saúde desenvolvam planos de tratamento personalizados, adaptados às necessidades específicas de cada paciente.
5.3.6 Goniometria de punho e dedos
A avaliação da amplitude de movimentos de punho e dedos nos pacientes com SCZV é fundamental para identificar variações significativas nas limitações funcionais. A goniometria oferece insights valiosos que permitem desenvolver intervenções personalizadas, focadas nas necessidades individuais de cada paciente. Abordagens terapêuticas personalizadas, baseadas em avaliações precisas, são essenciais para otimizar a funcionalidade das mãos e melhorar a qualidade de vida dos pacientes com SCZV.
5.4 PERSPECTIVAS
Essas descobertas destacam a importância de avaliações detalhadas e contínuas do trofismo muscular em crianças com SCZV. Intervenções precoces e adequadas podem ajudar a minimizar o impacto da hipotrofia nas atividades diárias e melhorar a qualidade de vida dessas crianças.
A alta prevalência de anormalidades na posição neutra da mão entre crianças com SCZV sugere a importância de incluir avaliações detalhadas das mãos como parte dos cuidados padrão. Intervenções precoces e contínuas são essenciais para mitigar os impactos dessas deformidades, promover a independência morfofuncional e melhorar a qualidade de vida dos pacientes.
A alta incidência de desvios latero-laterais, especialmente os desvios ulnares, sugere a necessidade de uma abordagem multidisciplinar no manejo desses pacientes. Fisioterapeutas, terapeutas ocupacionais e cirurgiões devem trabalhar em conjunto para desenvolver planos de tratamento eficazes que abordem tanto a prevenção quanto a correção dos desvios, garantindo uma melhor funcionalidade e qualidade de vida para as crianças afetadas pela SCZV. Intervenções precoces e contínuas são essenciais para maximizar o potencial funcional, prevenir complicações adicionais e melhorar a qualidade de vida dos pacientes.
A ampla variação nas amplitudes de movimento observada na flexão e extensão do punho, bem como na flexão e abdução/adução do polegar, destaca a necessidade de uma abordagem individualizada na reabilitação desses pacientes. Programas de fisioterapia e terapia ocupacional devem ser adaptados às necessidades específicas de cada paciente para maximizar a funcionalidade e a qualidade de vida. Avaliações regulares e ajustes nas intervenções são essenciais para acompanhar o progresso e fazer as adaptações necessárias no plano de tratamento.
A continuidade de estudos e pesquisas na área é vital para aprofundar a compreensão das necessidades específicas das crianças com SCZV. A aplicação de novas estratégias terapêuticas e educacionais, bem como a adaptação das já existentes, pode oferecer melhorias contínuas na qualidade de vida e na funcionalidade dessas crianças. A promoção de uma abordagem integrativa e centrada no paciente deverá permanecer como foco central nas práticas clínicas e nas políticas de saúde pública.
6. CONCLUSÃO
As investigações sobre as características morfofuncionais quanto às alterações nas estruturas das mãos e punho na primeira infância, em crianças com microcefalia decorrentes da exposição fetal ao SCZV, levaram às seguintes conclusões:
- A análise abrangente das condições morfofuncionais de crianças com SCZV reforça a necessidade de uma abordagem multidisciplinar e personalizada na gestão dessa condição. A colaboração entre diferentes profissionais de saúde, a realização de avaliações regulares e a implementação de intervenções personalizadas são essenciais para otimizar a funcionalidade das mãos e melhorar significativamente a qualidade de vida dos pacientes.
- Nossos resultados destacam a necessidade premente de atenção ao neurodesenvolvimento dessa população. A implementação de programas de estimulação precoce, juntamente com políticas de saúde e educação inclusiva, é importante para reduzir o peso da doença. Essas iniciativas não apenas apoiam o desenvolvimento das crianças, mas também permitem um melhor estudo morfofuncional das mãos e punho em crianças afetadas pela SCZV.
REFERÊNCIAS
- Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância das Doenças Transmissíveis. Protocolo de vigilância e resposta à ocorrência de microcefalia relacionada à infecção pelo vírus Zika / Ministério da Saúde, Secretaria de Vigilância em Saúde, Departamento de Vigilância das Doenças Transmissíveis. – Brasília: Ministério da Saúde. 55p. 2015.
- Pernambuco. Secretaria Estadual de Saúde de Pernambuco. Secretaria Executiva de Vigilância em Saúde. Protocolo Clínico e Epidemiológico para investigação de casos de microcefalia no estado de Pernambuco. Versão N° 02. Pernambuco: Secretaria Estadual de Saúde. 42p, 2015.
- Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Orientações integradas de vigilância e atenção à saúde no âmbito da Emergência de Saúde Pública de Importância Nacional: procedimentos para o monitoramento das alterações no crescimento e desenvolvimento a partir da gestação até a primeira infância, relacionadas à infecção pelo vírus Zika e outras etiologias infecciosas dentro da capacidade operacional do SUS [Internet]. Brasília: Ministério da Saúde; 2017. Disponível em: https://bvsms.saude.gov.br/bvs/publicacoes/orientacoes_ integradas_vigilancia_atencao_emergencia_saude_publica.pdf. Acesso em: 20 mai 2024.
- Costello A, Dua T, Duran P, Gulmezolglu M, Oladapo OT, Perea W. et al. Defining the syndrome associated with congenital Zika virus infection. Bull World Health Organ. 2016;94(6):406-506A.
- Mlakar J. et al. Zika Vírus Associated with Microcephaly. N Engl J Med. 2016; 374:951958.
- Lowe R, Barcellos C, Brasil P, Cruz OG, Honório NA, Kuper H, et al. The Zika virus epidemic in Brazil: from discovery to future implications. Int J Environ Res Public Health. 2018;15(1):96.
- World Health Organization (WHO). Zika situation report. 2016. Available at: http://www.who.int/emergencies/zika-virus/situation-report/3-november2016/en/. Accessed in: 10 Jun 2024.
- Organização Pan-Americana de Saúde (OPAS). Surto do vírus Zika continua um ano após emergência global. 2017. Disponível em: https://www.paho.org/pt/noticias/3-2-2017-surto-do-virus-zika-continua-um-anoaposemergenciaglobal#:~:text=3%20de%20fevereiro%20de%202017,transtornos%20neurol%C3%B3gicos%20e%20malforma%C3%A7%C3%B5es%20cong%C3%AAnitas. Acesso em: 04 mar 2024.
- Costello A, Dua T, Duran P. Defining the syndrome associated with congenital Zika virus infection. Bull World Health Organ. 2016;94(6):406-506A.
- Moore CA, Staples JE, Dobyns WB, Pessoa A, Ventura CV, Fonseca EB, et al. Characterizing the pattern of anomalies in congenital Zika syndrome for pediatric clinicians. JAMA Pediatr. 2017;171(3):288-95.
- Albuquerque MFPM, Souza WV, Araújo TVB, Braga MC, Miranda-Filho DB, Ximenes RAA. Epidemia de microcefalia e vírus Zika: a construção do conhecimento em epidemiologia. Cad Saúde Púb. 2018; 34(P):e00069018.
- Manssetti T, Herrero D, Alencar J, Silva T, Moriyama C, Gehrke F, et al. Clinical characteristics of children with congenital Zika syndrome: a case series. Arq Neuropsiquiatr. 2020;78(7):403-11.
- Aragão MFV, van der Linden V, Brainer-Lima AM, Coeli RR, Rocha MA, Silva OS, Carvalho MDCG, et al. Clinical features and neuroimaging (CT and MRI) findings in presumed Zika virus related congenital infection and microcephaly : retrospective case series study. BMJ. 2016;353(1901):1-10.
- Aragão MFV, Holanda AC, Brainer-Lima AM, Petribu NCL, Castillo M, van der Linden V, et al. Nonmicrocephalic Infants with Congenital Zika Syndrome Suspected Only after Neuroimaging Evaluation Compared with Those with Microcephaly at Birth and Postnatally: How Large Is the Zika Virus ―Iceberg‖? AJNR Am J Neuroradiol. 2017;38(7):1427–34.
- Levine D, Jani JC, Castro-Aragon I, Cannie M. How does imaging of congenital zika compare with imaging of other torch infections? Radiology. 2017;285(3):744–61.
- Neuberger I, Garcia J, Meyers ML, Feygin T, Bulas DI, Mirsky DM. Imaging of congenital central nervous system infections. Pediatr Radiol. 2018;48(4):513–23.
- Niemeyer B, Hollanda R, Muniz B, Marchiori E. What we can find beyond the classic neuroimaging findings of congenital zika virus syndrome? Eur Neurol. 2020;83(1):17–24.
- Alves LV, Hazin AN, Alves JGB. Neuroimaging in Children Born With Congenital Zika Syndrome: A Cohort Study. J Child Neurol. 2021;36(12):1066–70.
- van der Linden V, Rolim Filho EL, Lins OG, van der Linden A, Vasco Aragão MFV, Brainer-Lima AM, et al. Congenital Zika syndrome with arthrogryposis: retrospective case series study. BMJ. 2016; 354: i3899.
- Aragão MFVV, Brainer-Lima AM, Holanda AC, van der Linden V, Vasco Aragão L. et al. Spectrum of Spinal Cord, Spinal Root, and Brain MRI Abnormalities in Congenital Zika Syndrome with and without Arthrogryposis. AJNR Am J Neuroradiol; 2017;38(5):1045-53.
- Schüler-Faccini L. Orthopedic findings in arthrogryposis and congenital Zika syndrome: A case series. Birth Defects Res. 2020;112(5):385-92.
- Serpa SC, Melo ACMG, Lins OG, van der Linden V, Rolim Filho EL, Santos ACO. Orthopedic findings in arthrogryposis and congenital Zika. Bir Def Res. 2020;112(1):385-92.
- Contreras-Capetillo SN, Palma-Raquedano JR, Valadês-González N, ManriqueSaide P, Barrera-Pérez AM, Pinto-Escalante DP, et al. Case report: congenital arthrogryposis and unilateral absences of distal arm in congenital Zika syndrome. Front Med. 2021;9(4):499016.
- Pessoa A, Van Der Linden V, Yeargin-Allsopp M, Carvalho MDCG, Ribeiro EM, van Naarden Braun K, et al. Motor abnormalities and epilepsy in infants and children with evidence of congenital zika virus infection. Pediatrics. 2018;141:S167–79.
- Melo ACMG, van der Linden V, Serpa SC, Rolim Filho EL, Lins OTG. Electromyography in congenital Zika syndrome. J Clin Neurofisiol. 2023;40(4):350-4.
- Almeida TDR, Carvalho PRC, Cavalcanti BS, Aires VGB, Siqueira CCB, Rolim Filho EL. Análise da eficácia da tenotomia no tratamento da subluxação espástica do quadril de crianças com Síndrome congênita do Zika: um estudo pioneiro. Acta Ortop Bras. 2023;31(1):215-20.
- Aires VGB, Sanchez AU, Torban B, Oliveira ECP, Barros FC, Malheiros Junior HJA, et al. Orthopedic abnormalities in patients presenting with Congenital Zika syndrome: an analysis of 157 patients. Braz J Healt Rev. 2023;6(1): 25357-66.
- Cavalcanti BS, Oliveira ECP, Almeida TDR, Oliveira Neto FC, Aires VGB. Oliveira HFV, et al. Avaliação do uso de toxina botulínica em pacientes portadores de microcefalia secundaria a síndrome do vírus Zika congênito. Braz J Dev. 2021;7(1):15223-38.
- Caetano EB, Caetano M. Anatomia funcional do punho e da mão, 4ª ed. In: Traumatismo das mãos; 2016.
- Flor CJDRV, Guerreiro CF, Anjos JLM. Desenvolvimento neuropsicomotor em crianças com microcefalia associado ao zika vírus. Rev Pesqui Fisioter. 2017;7(3):313-18.
- van der Linden V, Pessoa A, Dobyns W, Barkovich AJ, van der Linden Jr H, Rolim Filho EL, et al. Description of 13 infants born during october 2015–january 2016 with congenital zika virus infection without microcephaly at birth – Brazil. MMWR Morb Mortal Wkly Rep. 2016;65(47):1343-8.
- Araújo TVBM, Rodrigues LC, Ximenes RAA, Miranda-Filho DB, Montarroyos UR, Melo APL. Association between Zika virus infection and microcephaly in Brazil, January to May, 2016: preliminary report of a case-control study. Lancet. 2016;16(12):1356-63.
- Brasil. Ministério da Saúde. Protocolo de vigilância e resposta à ocorrência de microcefalia e/ou alterações do sistema nervoso central (SNC). March 10, 2016. Available in: http://combateaedes.saude.gov.br/images/sala-de-situacao/ Microcefalia-Protocolo-de-vigilancia-e- resposta-10 mar2016 –18h.pdf. Accessed in: 8 mai 2024.
- Matos MA, Nascimento MAST, Merriman JW. Orthopaedic approach to the congenital Zika syndrome. Inter Orthop. 2021;45(3):559-64.
- Leal MC, Muniz LF, Ferreira TSA, Santos CM, Almeida LC, van der Linden V, et al. Hearing loss in infants with microcephaly and evidence of congenital Zika virus infection – Brazil, November 2015 – May 2016. MMWR Morb Mortal Wkly Rep. 2016;65(34):917-9.
- van der Linden V, Filho EL, van der Linden A. Congenital Zika syndrome: clinical aspects. In: Aragão MF, ed. Zika in Focus. Springer International Publishing; 2017. p.33-45.
- Ventura LO, Ventura CV, Lawrence L, van der Linden V, van der Linden A, Gois AL, et al. Visual impairment in children with congenital Zika syndrome. JAAPS, 2017;21(4):295-9.
- Ribeiro CTM, Hamanaka T, Pone S, Aibe MS, Gomes SC, Nielsen-Sianes K, et al. Gross motor function in children with congenital Zika Syndrome from Rio de Janeiro, Brazil. Eur J Ped. 2022;181(1):783-8.
- Marques FJP, Teixeira MCS, Barra RR. Children born with congenital Zika syndrome display atypical gross motor development and a higher risk for cerebral palsy. J Child Neurol. 2018;34(2):81–85
- Saad T, PennaeCosta AA, de Goes FV. Neurological manifestations of congenital Zika virus infection. Childs Nerv Syst. 2018;34(1):73–78.
- Ferreira HNC, Schiariti V, Regalado ICR et al (2018) Functioning and disability profile of children with microcephaly associated with congenital Zika virus infection. Int J Environ Res Public Health. 2018;15(6):1107.
- Amundsen KR, Evensen KA. Physical therapy intervention for a child with congenital Zika virus syndrome: a case report. Child Neurol Open. 2020;7(1):2329004X19896190.
- Pan American Health Organization. Guideline for Zika virus disease and complications surveillance. Washington: PAHO; 2016.
- Melo A, Gama GL, Silva Júnior RA, Assunção PL, Tavares JS, Silva MB, Costa KNFS, Vânia ML, Evangelista MA, Amorim MMR. Motor function in children with congenital Zika syndrome. DMCN. 2020;62(2):221-6.
- Moura da Silva AA, Gans JS, Souza PD, Doriqui MJ, Ribeiro MR, Branco MD, et al. growth and neurological outcomes in infants with probable congenital Zika virus infection. Em Inf Diseases. 2016;22(1):1953–6.
- del Campo M, Feitosa IML, Ribeiro EM, Pessoa AL, França GV, Garcıa-Alix A, et al. The phenotypic spectrum of congenital Zika syndrome. Am J Med Gen Part A 2017;173A:841–57.
- Da Silva Pone MV, Moura Pone S, Araujo Zin A, Barros Mendes PH, Senra Aibe M, Barroso de Aguiar E, de Oliveira Gomes da Silva T. Zika virus infection in children: Epidemiology and clinical manifestations. Childs. Nerv. Syst. 2018;34(1):63–71.
- De Araújo T, Ximenes R, Miranda-Filho DB, Souza WV, Montarroyos UR, de Melo A. et al. Association between microcephaly, Zika virus infection, and other risk factors in Brazil: Final report of a case-control study. Lancet Infect Dis. 2018;18(1):328–36.
- Nielsen-Saines K, Brasil P, Kerin T, Vasconcelos Z, Gabaglia CR, Damasceno L, Pone M, Abreu de Carvalho LM, Pone SM, Zin AA. et al. Delayed childhood neurodevelopment and neurosensory alterations in the second year of life in a prospective cohort of ZIKV-exposed children. Nat Med. 2019;25(1):1213–7.
- Sobral da Silva PF, Eickmann SH, Arraes de Alencar Ximenes R, Ramos Montarroyos U, de Carvalho Lima M, Turchi Martelli CM. et al. Pediatric neurodevelopment by prenatal Zika virus exposure: A cross-sectional study of the microcephaly epidemic research group cohort. BMC Pediatr. 2020;20(1):472.
- Peçanha PM, Gomes Junior SC, Pone SM, Pone M, Vasconcelos Z, Zin A, Vilibor R. et al. Neurodevelopment of children exposed intra-uterus by Zika virus: A case series. PLoS ONE. 2020;15(2):e0229434.
- Carvalho M, Ximenes R, Montarroyos UR, da Silva P., Andrade-Valença L, Eickmann SH, Ramos RC, Rocha MAW. Early epilepsy in children with Zikarelated microcephaly in a cohort in Recife, Brazil: Characteristics, electroencephalographic findings, and treatment response. Epilepsia. 2020;61(3):509–18.
- Oliveira D, Miranda-Filho DB, Ximenes R, Montarroyos UR, Martelli C, Brickley EB. et al. Comparison of oropharyngeal dysphagia in Brazilian children with prenatal exposure to Zika Virus, with and without Microcephaly. Dysphagia. 2021;36(4):583–94.
- Cavalcanti BS, Oliveira ECP, Almeida TDR, Oliveira Neto FC, Aires VGB, Oliveira HFV. Evaluation of the use of botulinic toxin in patients with microcephaly seconding the Congenital Zika Virus Syndrome. BJD. 2021; 7(2):15233-8.
- de Oliveira RC, de Freitas LB, Gomes RR, Cliquet A Jr. Orthopedic related comorbidities in spinal cord-injured individuals. Sutiãs Acta Ortop. 2020;28(4):199-203.
- van der Linden V, Pessoa A, Dolbyns W, Barkovich AJ, van der Linden Junior H, Rolim Filho EL, et al. Description of 13 infants born during October 2015-January 2016 with congenital Zika virus infection without microcephaly at birth—Brazil. MMWR Morb Mortal Wkly Report. 2016;65(1):1343–8.
- Bertolli J, Attell JE, Rose C, Moore CA, Melo F, Staples JE, Kotzky K. et al. Functional Outcomes among a Cohort of Children in Northeastern Brazil Meeting Criteria for Follow-Up of Congenital Zika Virus Infection. Am J Trop Med Hyg. 2020;102(5):955-63.
- Romeo DM, Ricci D, Brogna C, Mercuri E. Use of the Hammersmith Infant Neurological Examination in infants with cerebral palsy: a critical review of the literature. Dev Med Child Neurol. 2016;58(3):240-5.
- Barros Filho TEP, Lech O (eds). Exame físico em ortopedia [3.ed.]. São Paulo: Sarvier, 2017. 409p.
- Ferreira HNC, Schiariti V, Regalado ICR, Souza KG, Pereira SA, Fechine CPNS et al. Functioning and disability profile of children with microcephaly associated with congenital Zika virus infenction. Int J Environ Res Public Health. 2018;15(6):1107.
- Cunha RV, Geniole LAI, Brito CAA, França NPS, Santos Neto OG, Nascimento DDG, et al. Zika: abordagem clínica na atenção básica. Cuiabá: UFMS, Fiocruz; Brasília (DF): Ministério da Saúde, UNA-SUS; 2016 [citado2024jul11]. http://www.saude.pi.gov.br/uploads/warning_document/file/276/livro.pdf.
