DEEP VEIN THROMBOSIS AND PULMONARY EMBOLISM: ADVANCES IN DIAGNOSIS, MANAGEMENT, AND PREVENTION
REGISTRO DOI: 10.69849/revistaft/ma10202504301604
Désio Antônio dos Santos Costa1
Tiago Emanoel Soares2
Pedro Arthur Guimarães Vasconcelos Peixoto3
Andre Luis Ribeiro Bernal Filho4
Mateus Ruperto Mallosto das Chagas5
João Victor Gualberto Rodrigues6
Ágata Raposo de Medeiros7
Livia Rachel Abrantes Dias8
Resumo
A tromboembolia venosa (TEV), que abrange a trombose venosa profunda (TVP) e o tromboembolismo pulmonar (TEP), constitui uma importante causa de morbimortalidade no cenário médico atual. A fisiopatologia da TEV é fundamentada na tríade de Virchow: estase sanguínea, lesão endotelial e hipercoagulabilidade. A TVP afeta predominantemente os membros inferiores e pode ser assintomática ou apresentar sinais como dor, edema e empastamento muscular. O TEP, por sua vez, manifesta-se de forma variável, desde dispneia leve até colapso cardiovascular, dependendo da extensão da obstrução vascular e da repercussão hemodinâmica. O diagnóstico da TVP é realizado principalmente por ultrassonografia com Doppler, enquanto a angiotomografia de tórax é o exame de escolha para o TEP. A estratificação de risco, por meio de escores clínicos como o de Wells e Geneva, é essencial para a conduta diagnóstica e terapêutica. O tratamento baseia-se na anticoagulação, sendo utilizados heparinas, anticoagulantes orais diretos ou antagonistas da vitamina K. Em casos graves de TEP, pode-se recorrer à trombólise sistêmica ou dirigida por cateter, respeitando contraindicações específicas. A classificação do TEP em maciço, submaciço e de baixo risco orienta a abordagem terapêutica. A prevenção da TEV é fundamental e envolve medidas farmacológicas e mecânicas, além da deambulação precoce e avaliação individualizada do risco trombótico. Protocolos de profilaxia em ambientes hospitalares demonstram significativa redução da incidência de eventos tromboembólicos. Conclui-se que o reconhecimento precoce, o uso racional dos escores clínicos e a implementação de estratégias preventivas são fundamentais para reduzir a morbimortalidade da TEV, além de promover condutas terapêuticas mais seguras e eficazes.
Palavras-chave: Trombose Venosa Profunda. Tromboembolismo Pulmonar. Anticoagulação. Prevenção de TEV.
1 INTRODUÇÃO
O tromboembolismo venoso (TEV) é uma condição clínica potencialmente grave que engloba duas manifestações principais: a trombose venosa profunda (TVP) e o tromboembolismo pulmonar (TEP) (GOLDMAN et al., 2019; JAMESON et al., 2018). A TVP caracteriza-se pela formação de coágulos sanguíneos nas veias profundas, predominantemente nos membros inferiores, podendo obstruir parcial ou totalmente o fluxo venoso (SBACV, 2015). A mobilização desses trombos pode culminar em embolia pulmonar, tornando o TEP a complicação mais temida da TVP, devido ao risco elevado de morbidade e mortalidade (GOLDMAN et al., 2019).
Estudos indicam que o TEV é responsável por desfechos clínicos importantes, como isquemia tecidual, disfunção vascular e óbito, além de impactar significativamente a saúde mental e a qualidade de vida dos pacientes (JAMESON et al., 2018). A atenção a grupos de risco específicos, como gestantes e pacientes oncológicos, é essencial, visto que essas populações apresentam incidência mais elevada da condição (CARAMELLI et al., 2004; SBACV, 2015).
O diagnóstico do TEV exige alto grau de suspeição clínica, sendo baseado na associação entre história clínica, exame físico, escores de probabilidade e exames complementares. O tratamento varia conforme a gravidade e localização do trombo, incluindo terapias anticoagulantes, medidas não farmacológicas e, em casos selecionados, intervenções invasivas.
Estima-se que, globalmente, aproximadamente 600.000 casos de TEV sejam diagnosticados por ano, com cerca de 80.000 mortes atribuídas às suas complicações (KAHN, 2016). A incidência é semelhante entre os sexos, mas aumenta significativamente com o avanço da idade. Em gestantes, destaca-se a maior frequência de trombos em veias proximais, especialmente no membro inferior esquerdo, com forte associação à síndrome de May-Thurner. Nessas situações, a evolução para TEP ocorre em até metade dos casos de TVP proximal, reforçando a importância da intervenção precoce (BATES et al., 2012).
Diante da relevância clínica e epidemiológica do tromboembolismo venoso, este estudo tem como objetivo revisar seus principais aspectos, incluindo definição, fatores de risco, diagnóstico, complicações e estratégias de manejo, com base nas evidências científicas atuais.
2 METODOLOGIA
Trata-se de uma revisão sistemática da literatura realizada em abril de 2025, por meio de pesquisas nas bases de dados PubMed, SciELO, BVS e Google Scholar. Utilizaram-se os descritores (“Venous Thromboembolism” OR “Deep Vein Thrombosis” OR “Pulmonary Embolism”) AND (“Diagnosis” OR “Risk Assessment” OR “Thrombolytic Therapy” OR “Anticoagulants”) AND (“Evidence-Based Medicine” OR “Disease Prevention” OR “Hospital Mortality”), resultando em um total de 63 artigos, os quais foram submetidos aos critérios de elegibilidade.
Foram incluídos estudos publicados nos últimos 15 anos, nos idiomas português ou inglês, que abordassem as temáticas propostas e estivessem disponíveis na íntegra. Foram excluídos artigos duplicados, restritos ao formato de resumo, que não tratassem diretamente do objeto de estudo ou que não atendiam aos critérios de inclusão estabelecidos. Após a aplicação desses critérios, oito estudos foram selecionados e submetidos à leitura detalhada para extração de dados.
Adicionalmente, foi utilizada a Diretriz para diagnóstico, tratamento e prevenção da trombose venosa profunda e do tromboembolismo pulmonar da Sociedade Brasileira de Angiologia e de Cirurgia Vascular.
Os resultados foram apresentados de forma descritiva e tabelas.
3 RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
A trombose venosa profunda (TVP) e o tromboembolismo pulmonar (TEP) representam manifestações clínicas distintas de uma mesma condição patológica denominada tromboembolia venosa (TEV). A TVP caracteriza-se pela formação de coágulos sanguíneos, usualmente nos membros inferiores, enquanto o TEP ocorre quando esses trombos se deslocam até a circulação pulmonar, provocando obstrução das artérias pulmonares. Essa entidade clínica constitui um importante problema de saúde pública, sendo responsável por elevada morbimortalidade em todo o mundo (SBACV, 2021; ESC, 2019).
A fisiopatologia da TEV é explicada pela tríade de Virchow, que compreende três fatores principais: estase sanguínea, lesão endotelial e estado de hipercoagulabilidade. A estase sanguínea ocorre em situações de imobilização prolongada, insuficiência venosa crônica ou obesidade. A lesão endotelial pode ser provocada por traumas, procedimentos cirúrgicos ou processos inflamatórios. Já o estado de hipercoagulabilidade pode ser de origem hereditária, como nas trombofilias (déficits de proteína C, proteína S, antitrombina III, mutações do fator V de Leiden e da protrombina), ou adquirido, como em pacientes com neoplasias, gestação, uso de anticoncepcionais orais, síndrome nefrótica, entre outros (KAHN, 2016; GOLDHABER; BOUVIER, 2012; KONSTANTINIDES et al., 2020).
No TEP, a obstrução das artérias pulmonares pelo êmbolo leva ao aumento súbito da resistência vascular pulmonar, gerando sobrecarga aguda do ventrículo direito, redução do débito cardíaco e hipóxia. A liberação de mediadores inflamatórios, como serotonina, tromboxano e histamina, potencializa a vasoconstrição e agrava o comprometimento hemodinâmico. Quando não tratado precocemente, o TEP pode evoluir para colapso cardiovascular e morte súbita (BATES et al., 2012).
A apresentação clínica da TVP pode variar amplamente. Em muitos casos, é assintomática, especialmente em tromboses distais. Quando sintomática, os sinais clássicos incluem dor localizada, edema assimétrico, empastamento muscular, aumento da temperatura local e eritema. O sinal de Homans — dor na panturrilha à dorsiflexão passiva do pé — é descrito, mas possui baixa especificidade. A presença de veias colaterais superficiais dilatadas também pode ser observada em casos mais extensos (SBACV, 2021).
O TEP, por sua vez, tem apresentação clínica altamente variável, o que dificulta o diagnóstico imediato. Em casos leves, pode manifestar-se apenas por dispneia de esforço, dor torácica pleurítica ou tosse seca. Em apresentações moderadas a graves, surgem sintomas como taquipneia, taquicardia, hemoptise, sudorese, síncope e hipotensão. Em pacientes com embolia maciça, ocorre colapso hemodinâmico, podendo evoluir rapidamente para choque obstrutivo e parada cardiorrespiratória (KONSTANTINIDES et al., 2020; BATES et al., 2012).
Pacientes com TEP submaciço podem apresentar sinais de sobrecarga do ventrículo direito, como turgência jugular, hepatomegalia e B3 audível à ausculta cardíaca. Em idosos, sintomas atípicos como confusão mental e queda do nível de consciência podem predominar. A ausculta pulmonar, muitas vezes, é normal, o que reforça a necessidade de avaliação complementar em casos suspeitos (GOLDHABER; BOUVIER, 2012).
A variabilidade das manifestações clínicas torna essencial o uso de escores preditivos, como o escore de Wells, para estratificação da probabilidade clínica e orientação na escolha dos exames complementares (SBACV, 2021; ESC, 2019).
O diagnóstico da TVP é feito prioritariamente por meio de ultrassonografia com Doppler venoso, exame de escolha por ser não invasivo, amplamente disponível e de boa acurácia. Em casos de TEP, o exame de primeira linha é a angiotomografia de tórax, considerada padrão-ouro por permitir visualização direta do trombo nas artérias pulmonares.
A cintilografia de ventilação-perfusão (V/Q) pode ser empregada quando a angiotomografia é contraindicada, como em pacientes com insuficiência renal grave ou alergia ao contraste iodado (BATES et al., 2012; KONSTANTINIDES et al., 2020).
Exames laboratoriais, como o dímero-D, têm alta sensibilidade, mas baixa especificidade. Assim, são úteis para excluir TEV em pacientes com baixa probabilidade clínica. Marcadores como troponina e peptídeo natriurético tipo B (BNP) são utilizados para estratificação de risco nos casos de TEP, sendo indicativos de disfunção ventricular direita e pior prognóstico (KAHN, 2016).
Dois escores amplamente utilizados para estratificação da probabilidade clínica são o escore de Wells e o escore de Genebra, conforme tabelas a seguir:
Tabela 1 – Escore de Wells para TVP
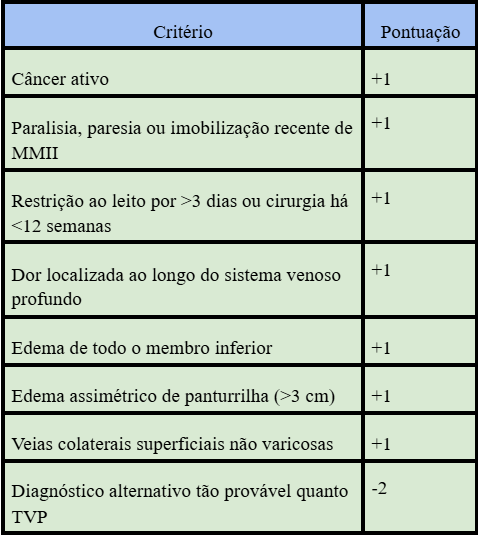
Interpretação do Escore de Wells para TVP:
- ≥3 pontos: alta probabilidade;
- 1-2 pontos: probabilidade moderada;
- 0 ou menos: baixa probabilidade.
Tabela 2. Escore de Wells para TEP
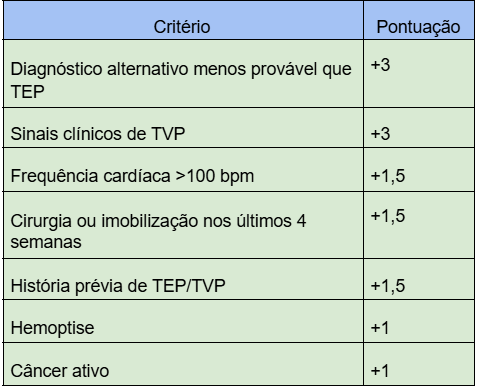
Interpretação do Escore de Wells para TEP
- >6 pontos: alta probabilidade;
- 2-6 pontos: probabilidade moderada;
- <2 pontos: baixa probabilidade.
O diagnóstico diferencial da TVP inclui celulite, linfangite, tromboflebite superficial, trauma muscular e cisto de Baker roto. Para o TEP, os principais diagnósticos diferenciais envolvem infarto agudo do miocárdio, dissecção de aorta, pneumotórax, pericardite e pneumonia, devido à semelhança dos sintomas respiratórios e torácicos (SBACV, 2021).
A classificação do TEP em três grupos principais auxilia na tomada de decisão terapêutica:
- TEP maciço: presença de hipotensão sustentada (<90 mmHg), choque ou parada cardíaca.
- TEP submaciço: sem hipotensão, mas com disfunção do ventrículo direito (evidenciada por ecocardiograma) e marcadores laboratoriais elevados.
- TEP de baixo risco: pacientes hemodinamicamente estáveis, sem disfunção ventricular ou elevação de marcadores (BATES et al., 2012).
O tratamento da TEV baseia-se na anticoagulação, que visa prevenir a progressão do trombo, a embolização e eventos recorrentes. Inicialmente, pode-se utilizar heparina não fracionada (HNF), heparina de baixo peso molecular (HBPM) ou anticoagulantes orais diretos (DOACs), como rivaroxabana, apixabana ou dabigatrana. A escolha da medicação depende do perfil clínico do paciente, comorbidades, risco de sangramento e custo (GOLDHABER; BOUVIER, 2012; KEARON et al., 2016).
Nos casos graves de TEP com instabilidade hemodinâmica, pode-se lançar mão da trombólise sistêmica com alteplase ou estreptoquinase, ou trombólise dirigida por cateter, que oferece menores taxas de sangramento.
As contraindicações absolutas ao uso de trombolíticos incluem: hemorragia intracraniana prévia, neoplasia cerebral conhecida, AVC isquêmico nos últimos 3 meses, sangramento ativo ou discrasias sanguíneas graves. Contraindicações relativas incluem: cirurgia recente, hipertensão arterial não controlada, úlcera péptica ativa, gestação e retinopatia diabética proliferativa (KONSTANTINIDES et al., 2020).
Em pacientes com contraindicação absoluta à anticoagulação, como hemorragias ativas, está indicada a colocação de filtro na veia cava inferior (BATES et al., 2012).
A duração do tratamento varia conforme a etiologia. Casos provocados por fatores transitórios, como cirurgia recente, geralmente requerem três meses de anticoagulação. Já nos episódios idiopáticos, recidivantes ou relacionados a trombofilias, recomenda-se tratamento prolongado ou até mesmo indefinido, após avaliação da relação risco-benefício (KAHN, 2016; KONSTANTINIDES et al., 2020).
A prevenção da TEV é fundamental, especialmente em pacientes hospitalizados e em pós-operatório, com uso de profilaxia farmacológica (HBPM, HNF) e medidas mecânicas (meias compressivas, dispositivos de compressão pneumática intermitente). Além disso, a deambulação precoce e a hidratação adequada são medidas adjuvantes importantes, especialmente em pacientes acamados ou com mobilidade reduzida.
A profilaxia deve ser individualizada de acordo com o risco trombótico e hemorrágico de cada paciente, utilizando escores clínicos como o de Caprini ou o Padua Score. Em cirurgias ortopédicas, oncológicas e em pacientes internados em UTI, a adesão a protocolos de prevenção mostra-se especialmente eficaz.
O uso prolongado de anticoagulantes profiláticos também pode ser indicado após a alta hospitalar, dependendo do risco residual. A educação do paciente e da equipe de saúde sobre os fatores de risco e os sinais precoces de TEV é essencial para sua prevenção eficaz (SBACV, 2021; WHO, 2023; NICE, 2020).
4 CONCLUSÃO
A tromboembolia venosa, englobando a trombose venosa profunda e o tromboembolismo pulmonar, representa uma condição clínica de alta prevalência e relevância na prática médica, sendo responsável por significativa morbimortalidade. A compreensão de sua fisiopatologia, manifestações clínicas e diagnóstico é essencial para uma abordagem terapêutica eficaz e segura. O manejo adequado, baseado na estratificação de risco e na individualização do tratamento, é fundamental para reduzir complicações e melhorar o prognóstico dos pacientes. Além disso, medidas preventivas devem ser amplamente adotadas, sobretudo em populações de risco, reforçando o papel da medicina preventiva na redução do impacto da TEV nos sistemas de saúde.
REFERÊNCIAS
BATES, S. M. et al. Diagnosis of pulmonary embolism: a clinical practice guideline. Chest, v. 141, n. 2, p. e419S-e496S, 2012.
GOLDHABER, S. Z.; BOUVIER, N. M. Pulmonary embolism and deep vein thrombosis. In: LONGO, D. L. et al. Harrison’s principles of internal medicine. 18. ed. New York: McGraw-Hill, 2012.
KAHN, S. R. The post-thrombotic syndrome: evidence-based prevention, diagnosis, and treatment. Hematology Am Soc Hematol Educ Program, v. 2016, n. 1, p. 413-418, 2016.
KEARON, C. et al. Antithrombotic Therapy for VTE Disease: CHEST Guideline and Expert Panel Report. Chest, v. 149, n. 2, p. 315-352, 2016.
KONSTANTINIDES, S. V. et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism. European Heart Journal, v. 41, p. 543-603, 2020.
SBACV – SOCIEDADE BRASILEIRA DE ANGIOLOGIA E DE CIRURGIA VASCULAR. Diretriz para diagnóstico, tratamento e prevenção da trombose venosa profunda e do tromboembolismo pulmonar. 2021. Disponível em: https://www.sbacv.org.br/. Acesso em: 9 abr. 2025.
WORLD HEALTH ORGANIZATION (WHO). WHO report on the global burden of thrombosis. Geneva, 2023. Disponível em: https://www.who.int/publications/i/item/9789240079093. Acesso em: 9 abr. 2025.
NATIONAL INSTITUTE FOR HEALTH AND CARE EXCELLENCE (NICE). Venous thromboembolism in over 16s: reducing the risk of hospital-acquired deep vein thrombosis or pulmonary embolism. NICE guideline [NG89], 2020. Disponível em: https://www.nice.org.uk/guidance/ng89. Acesso em: 9 abr. 2025.
