INVESTIGATION OF THE INFLUÊNCIA OF ECOSYSTEMS ON PHYSICOCHEMICAL VARIABLES OF APIS MELLÍFERA HONEY FROM PARÁ
REGISTRO DOI: 10.69849/revistaft/pa10202503162018
Gilberto Nascimento do Vale1; Matheus Ramon Blanco Camarão2; Marcos Vinicios Pompeu Amaro3; Rennan da Silva Vale4; Marllon Cardoso Oliveira de Freitas5; Neliano Gonçalves Gomes6; Caio Henrique Borges Lima7; Ewerton Carvalho de Souza8; Antonio dos Santos Silva9
RESUMO
O mel é um produto alimentício produzido pelas abelhas melíferas, a partir do néctar das flores ou de excreções de insetos sugadores de plantas, que as abelhas recolhem, transformam, combinam com substâncias específicas próprias, armazenam e deixam maturar nos favos da colmeia, seu sabor e aroma variam de acordo com a origem da planta. O mel é extremamente concentrado em açúcares. Este estudo realizou uma análise físico-química em vinte méis da espécie Apis mellífera em um único município do nordeste do Pará, discriminando as amostras de acordo com o seu ecossistema (mangue ou capoeira) através de métodos estatísticos multivariados, contribuindo com o seu controle de qualidade. Os resultados encontrados sugerem boa qualidade das amostras, mas que se deve ter cuidados ao serem armazenadas, além do que diversas variáveis físico-químicas se mostraram dependentes de sua origem (mel de mangue e mel de capoeira).
Palavras-chave: Amazônia. Análises químicas. Produto de origem animal.
SUMMARY
Honey is a food product produced by honey bees, from the nectar of flowers or excretions of plant-sucking insects, which the bees collect, transform, combine with their own specific substances, store and leave to mature in the hive’s combs. Its flavor and aroma vary according to the origin of the plant. Honey is extremely concentrated in sugars. This study carried out a physical-chemical analysis on twenty honeys of the Apis mellífera species in a single municipality in the northeast of Pará, discriminating the samples according to their ecosystem (mangrove or capoeira) through multivariate statistical methods, contributing to their quality control. The results found suggest good quality of the samples, but care must be taken when storing them, in addition to the fact that several physicochemical variables were shown to be dependent on their origin (mangrove honey and capoeira honey).
Keywords: Amazon. Chemical analyses. Product of animal origin.
1. INTRODUÇÃO
O mel é um alimento natural elaborado pelas abelhas por meio do néctar e secreções liberadas pelas plantas, juntamente com as excreções das abelhas, que elaboram o mel a partir de transformações e adições de compostos específicos, fazem a desidratação, deposição e armazenamento do favo de mel a fim de obter estimular o seu amadurecimento. Ele é extremamente concentrado em açúcares, com destaque para a D-glicose e D-frutose (Rybak- Chmielewska, 2004). No mel há também vitaminas, minerais e enzimas, sendo que essas últimas são incorporadas para alterar a estrutura do monossacarídeo e assim aumentar o tamanho dos carboidratos. Em relação aos outros componentes, 21 % da composição do mel é constituída por água. Já a participação dos ácidos garante a integridade do mel e o protegem da proliferação de microrganismos, os dissacarídeos em maior quantidade são a sacarose e a maltose. Em menores quantidades temos as proteínas provenientes das glândulas salivares das abelhas, sendo a prolina a representante de maior ocorrência (Camargo, 2002).
Em se tratando do clima, a produção do mel é mais propícia em áreas que possuem estações muito bem definidas. Pois, após o período das chuvas a quantidade de flores vai ser maior. Além disso, é preciso haver controle da temperatura para não ocorrer grandes alterações tendo em vista a necessidade de manter o apiário entre 20º C e 30° C (SEBRAE, 2019).
O Brasil apresenta uma variabilidade climática que permite a produção do mel ao longo do ano todo, e a diferença entre os locais, os tipos de clima e floradas contribuem para tornar o mel um produto diversificado e com diversas texturas, aromas, gostos e cores (Ananias, 2010).
Os manguezais são ecossistemas de grande importância no equilíbrio ecológico, sendo um berçário favorável para o desenvolvimento de muitas espécies de animais e plantas (Dantas, 2005), sendo um dos ecossistemas costeiros mais produtivos; porém, também como um dos mais vulneráveis aos efeitos do desenvolvimento econômico e do crescimento desordenado das populações humanas, permite uma série de atividades socioeconômicas, bens e serviços gerados graças aos seus recursos; além das atividades mais costumeiras, esse ambiente ainda apresenta um potencial para a apicultura e meliponicultura, atividade essencial para a economia familiar do trópico úmido (Bezerra, 2004).
Por outro lado, a capoeira ou floresta secundária pode ser definida como a vegetação secundária que se refere a toda vegetação antrópica que cresce onde houve intervenção humana para uso da terra, seja com finalidade mineral, agrícola ou pecuária, descaracterizando a vegetação primária (IBGE, 2004).
Na Amazônia, os ecossistemas de capoeira são possíveis de serem definidos como áreas que se surgem a partir do crescimento de espécies que regeneram naturalmente em agro ecossistemas ou após o seu abandono (Vieira; Proctor, 2007; Salomão et al., 2012). Podem ser tomadas como exemplos de ecossistemas de capoeira, na Amazônia, as regiões de pousio no sistema agrícola de corte e queima e a vegetação arbustivo-arbórea formada após o abandono de áreas de pastagens, geralmente muito degradadas, além de áreas de cultivos agrícolas semiperenes (pimenta-do-reino e cana-de-açúcar) e perenes (cacau e café), abandonadas (Pereira; Vieira, 2001; Salomão et al., 2012).
Assim, o presente trabalho teve como objetivo trazer os resultados alcançados para méis da espécie Apis mellífera produzidos por apicultores de um município do Nordeste do Pará, tanto do ponto de vista físico-químico, quanto por métodos estatísticos multivariados, buscando investigar a influência do ecossistema das amostras de acordo com a sua localidade geográfica e entre si, contribuindo, dessa forma, com o seu controle de qualidade.
2. REVISÃO DA LITERATURA
2.1 O Mel e a Apicultura
Segundo a legislação brasileira, o mel é um produto alimentício produzido pelas abelhas melíferas, a partir do néctar das flores ou das secreções procedentes das partes vivas das plantas ou de excreções de insetos sugadores que ficam sobre as plantas (Brasil, 2000), sendo um produto consumido pela humanidade desde tempos pré-históricos. De acordo com Santos (2015), o momento exato da história no qual o ser humano percebeu a possibilidade de usar o mel como alimento é desconhecido, contudo, é possível afirmar que já se tinha conhecimento dele ainda nos momentos iniciais do processo de manuseio das primeiras ferramentas. Posteriormente, durante o Egito antigo, a prática da apicultura tornou-se um serviço bastante comum e o mel era um alimento muito apreciado pelo faraó.
Segundo Hammad (2018) o mel é descrito na literatura egípcia como um alimento divino, devido ao fato de Rá, figura mitológica da região, ter chorado lágrimas que se tornaram abelhas, ao mesmo tempo a sociedade da época considerou a substância um símbolo de fertilidade e sexualidade, além de relacioná-lo a questões religiosas e culturais. Com a expansão da apicultura do Egito para outros territórios, muitos povos tiveram contato com o mel e passaram a consumir o produto (Santos, 2015).
Na idade média, as técnicas de coleta do mel avançaram e o apicultor para retirar os favos lançava uma fumaça para dispersar as abelhas, ao invés de ter que eliminá-las. A preocupação em manejar corretamente as colmeias representavam uma grande evolução, pois outrora, o responsável por fazer o trabalho da coleta não tinha o preparo adequado para realizar a tarefa sem causar prejuízo ao enxame, logo por danificar o ninho dos produtores era preciso localizar novos pontos de extração (Visconde, 2016).
O conhecimento do potencial fitoterápico do mel é antigo e através dos séculos as suas propriedades cicatrizantes foram sendo descobertas, em muitos casos relatou-se a capacidade de reduzir as infecções de feridas (Escobar; Xavier, 2013). Nos dados levantados por Aroucha et al. (2008), mostrou-se a atividade anti-inflamatória, analgésica, sedativa e expectorante do mel, sendo que umas das substâncias que contribui para isso é H2O2, que provocaria danos às células bacterianas (Brudzynski, 2011). Já Da Silva (2013) diz que os compostos fenólicos colaboram para promover a ação antioxidante dos méis.
O mel possui propriedades essenciais para a manutenção da saúde como o estímulo da atividade antioxidante no organismo e a capacidade de favorecer a proteção contra doenças do trato digestório, sendo que tais atribuições dão ao produto um aspecto mais abrangente, no qual além de ser um produto feito para adoçar é capaz também de auxiliar no tratamento de doenças (Silva et al., 2008).
A produção do mel é feita pelas abelhas melíferas com destaque para a espécie Apis mellífera que é a principal responsável pela polinização no meio ambiente. Outro grupo que também realiza essa atividade faz parte da tribo dos meliponíneos conhecidas como abelhas sem ferrão. Embora produza mel em menor quantidade, as abelhas sem ferrão (nativa) fornecem um produto diferenciado do mel de Apis mellífera, possuindo consumidores distintos, dispostos a pagar altos preços pelo produto. Segundo Souza et al. (2004), o mel das abelhas sem ferrão (nativa) é um produto que tem apresentado uma demanda crescente de mercado, obtendo preços mais elevados que o das abelhas do gênero Apis em diferentes regiões do Brasil.
O mel é constituído por diversos açúcares e outras substâncias como ácidos orgânicos, enzimas, e partículas sólidas coletadas pelas abelhas, sendo que sua aparência varia de quase incolor a marrom escuro, podendo ser fluido, viscoso ou até mesmo sólido e seu sabor e aroma variam de acordo com a origem da planta. Desta forma, as variedades de mel podem ser identificadas por sua cor, gosto, sabor, e maneira de cristalização (Silva, 2008).
Técnicas analíticas são cada vez mais importantes para que haja um estabelecimento de parâmetros físico-químicos de cada um dos diversos tipos de mel existentes, de tal forma que se possam identificar possíveis adulterações do produto, e definir padrões de qualidade dos méis, de tal forma que eles se tornem mais competitivos em um mercado cada vez mais exigente (Oliveira; Medeiros; Moraes, 2017)
2.2 Ecossistema de mangue e de Capoeira
Os manguezais são ecossistemas abertos, que apresentam grande complexidade, onde acontecem significantes conexões entre o solo, o estuário, o oceano e o sistema atmosférico, ocorrendo na interface entre os ambientes marinhos e terrestres, tendo como principal característica a sua dependência das marés (Londe et al., 2013).
O Brasil possui cerca de 25.000 km2 de florestas de mangue (Figura 1), que representam mais de 12 % dos manguezais do mundo inteiro, os quais estão distribuídos desde o Amapá até a Laguna, em Santa Catarina, no Litoral brasileiro (Balata, 2008).
Figura 1. Distribuição dos manguezais no Brasil

Fonte: James Onning (2012).
A costa brasileira possui a maior área contínua de manguezal do mundo, medindo, aproximadamente, 1,38 milhões de hectares, cuja vegetação apresenta sua maior exuberância nas latitudes próximas à linha do Equador (litoral amazônico), na faixa compreendida entre a foz do rio Oiapoque (extremo norte do Estado do Amapá) e a baia de São Marcos (Estado do Maranhão), em uma região conhecida, singularmente, como Costa Norte (Balata, 2008). Sendo, então, um ecossistema muito comum no nordeste do Pará.
No mangue, a vegetação é com posta por uma grande diversidade de formas, composta por gramíneas, arbustos, palmeiras, samambaias e árvores, que crescem na zona intertidal (entre marés). Tais plantas pertencem a aproximadamente de 20 famílias, sendo uma dessas famílias da Divisão Pteridophyta (samambaia) e as demais plantas da Divisão Angiospermae (Duke; Ball; Ellison, 1998). E há cerca de 110 espécies de mangue, cerca de 20 gêneros de 16 famílias, que ocorrem apenas em habitats de mangue (Kuenzer et al., 2011). Alguns dos gêneros de manguezais são: Acanthus, Acrostichum, Aegialitis, Aegiceras, Avicennia, Bruguiera, Camptostemon, Ceriops, Conocarpus, Derris, Diospyros, Excoecaria, Heritiera, Kandelia, Laguncularia, Lumnitzera, Osbornia, Pelliciera, Rhabdadenia Rhizophora, Scyphiphora, Sonneratia, Xylocarpus e a palma Nypa (Woodroffe; Grindrod, 1991; Kuenzer et al., 2011).
Em termos de Brasil há 3 gêneros: Avicennia, Laguncularia e Rhizophora, com as espécies: Avicennia germinans (L.) L., Avicennia schaueriana Stapf. & Leechman, Laguncularia racemosa (L.) C. F. Gaertn., Rhizophora mangle L., Rhizophora harrisonii Leechman e Rhizophora racemosa G. Mey. Algumas espécies ocorrem na faixa de transição para ambientes terrestres como: Conocarpus erectus L., Hibiscus tiliaceus L., Hibiscus pernambucensis Arruda, Acrostichum aureum (L.) Mett., Spartina alterniflora Loisel, além de outras (Schaeffer-Novelli; Cintrón, 1983).
O ecossistema de capoeira ou mata de capoeira é um tipo de vegetação, tida como secundária, que nasce depois da derrubada da vegetação original ou primária de uma dada região, sendo que a origem deste termo é do tupi, significando “mato que nasceu no lugar de vegetação cortada” (Da Silva et al., 2024).
Sabe-se que a Amazônia é a maior floresta tropical da Terra, ocupando uma área de 4.196.943,00 km², que equivale a 49,29 % do território brasileiro, mas ela já perdeu grande parte da sua floresta primária, e, atualmente, aproximadamente 22 % desta área florestal já foi desmatada (Da Silva et al., 2024).
No Estado do Pará, conforme informações do IMAZON (2022), até o ano de 2021, mais de 39 % das áreas de floresta primária do Estado já haviam sofrido desnatamento, sendo que parte dessa área que sofreu desmatamento é abandonada e vem a sofrer um processo natural em que ocorre a regeneração através da sucessão ecológica, levando à formando de florestas secundárias ou capoeiras (Salomão et al., 2012).
Da Silva et al. (2024) destacam que tais formações florestais “podem fornecer habitat para salvaguardar a biodiversidade, especialmente onde a vegetação nativa é altamente fragmentada ou onde há pouca floresta primária remanescente”.
3 MATERIAIS E MÉTODOS
3.1 Amostragem
Vinte amostras de mel de abelha produzidas pela espécie Apis mellífera (aproximadamente 150 mL) provenientes do município de Tracuateua, na região nordeste do Pará (Figura 2), foram obtidas entre os meses de julho e setembro de 2022, diretamente dos apicultores ou de cooperativas locais. Tais amostras são provenientes de apiários localizados em dois ecossistemas distintos: mangue e capoeira, sendo que de cada ecossistema foram adquiridas dez amostras distintas, denominadas de amostra M (1 a 10), para as de mangue, e amostras C (1 a 10), para as de capoeira. Todas as amostras foram levadas ao Laboratório de Física Aplicada à Farmácia (LAFFA), da UFPA, sendo mantidas em temperatura ambiente e no seu próprio recipiente, sob o abrigo da luz direta, até a execução de suas análises.
Figura 2. Localização do município de Tracuateua, no nordeste paraense

Fonte: (a) Da Silva; Carvalho (2021), adaptada; (b) google maps (2025).
3.2 Análises Físico-Químicas dos Méis
Todas as análises executadas foram realizadas em triplicata e seguiram metodologias oficiais (Brasil, 2000; AOAC, 2000; CAC, 2001; Cechi, 2003; Adolfo Lutz, 2008).
A determinação de umidade, sólidos solúveis totais (SST) e densidade das amostras de mel foi realizada através do método refratométrico, tendo sido utilizado um refratômetro portátil da marca INSTRUTHERM, modelo ART-90, específico para análises de méis, contendo três escalas internas: uma escala de umidade, com valores entre 12 % e 27 %, com intervalo de 0,1 %; uma escala de SST, variando entre 58º Brix e 90º Brix, com intervalos de 0,5º Brix; e uma terceira escala para medição em graus Baumé, com valores entre 30º Be e 50º Be, e intervalos de 1º Be. Sobre o prisma do aparelho, duas ou três gotas de cada uma das vinte amostras de mel foram depositadas e devidamente espalhadas sobre a superfície do prisma. Então as leituras dos valores de SST e umidade foram obtidas diretamente no visor do aparelho, de suas respectivas escalas, ao passo que a densidade foi obtida através da leitura na escala Baumé, e usando a equação (1) para conversão para densidade. Nesta equação, Be é o valor lido na escala Baumé e d é a densidade obtida.

Uma solução de mel foi preparada se pesando 5,0 g de cada uma amostra de mel em um Erlenmeyer de 125 mL, onde se acrescentou 75 mL de água destilada para diluição do mel. A solução formada foi homogeneizada se agitando o sistema por 30 minutos e, em seguida, realizado a leitura da condutividade elétrica (CE) e do pH. No caso da CE, um eletrodo de um condutivímetro portátil modelo AKSO, AK51, previamente calibrado com solução de 143 µS/cm, foi inserido na solução de mel e o valor lido de forma direta no visor do aparelho. Já o pH foi obtido se introduzindo um eletrodo de um pHmetro de bancada da marca GONDO, modelo PP206K, previamente calibrando em dois pontos com soluções padrão de pH 4,00 e pH 7,00, na solução de mel e a leitura feita diretamente no visor do aparelho.
A viscosidade das vinte amostras de mel foi determinada com o emprego de viscosímetros do tipo copos Ford (números 4 e 5), da marca NALGON. O copo Ford foi preenchido com a respectiva amostra de mel, tapando o seu orifício até ser preenchido ao seu nível máximo e nivelado com uma espátula, retirando o excesso do produto. O orifício foi liberado e o cronômetro acionado ao mesmo tempo. A partir da primeira interrupção do fluxo, o cronômetro foi parado e anotado o tempo, em segundos. O tempo de escoamento foi transformado para viscosidade através das equações (2) e (3), para os Copos Ford tipo 4 e 5, respectivamente, fornecida pelo fabricante do aparelho, em que v é a viscosidade (em cSt) e t é o tempo de escoamento medido em segundos (s).

A determinação de sólidos insolúveis totais (SIT) foi realizada através do método gravimétrico. Foram pesados 2,0 g de amostra em béquer de 500 mL e a esta massa foi adicionado cerca de 100 mL de água destilada aquecida a 80º C, necessária para dissolver o mel. Em seguida, a solução foi filtrada em papel de filtro previamente seco a 105º C em estufa, por 2 h, e resfriados em dessecador até temperatura ambiente. O papel de filtro e o béquer foram lavados com água destilada a 80º C sucessivas vezes até a ausência de açúcares. Após a filtração e lavagem do papel de filtro, estes foram secos a 105º C por cerca de 2 h e resfriados em dessecador até temperatura ambiente e depois pesados em balança analítica. O teor de SIT foi determinado através da equação (4), em que mf é a massa do papel filtro após a filtração; ms é a massa do papel filtro seco; e ma é massa total da amostra.

A determinação de turbidez foi executada com o emprego de um turbidímetro digital da marca POLICONTROL, modelo T 1000 WT, com faixa de trabalho de 0 a 1000 Unidades de Turbidez Nefelométrica (NTU). O procedimento para a determinação ocorreu através do preparo de uma solução do mel a ser analisado, preparada com 2,00 g de amostra e 100 mL de água destilada. A solução obtida foi transferida cuidadosamente para as cubetas até o nível marcado e os valores de turbidez foram lidos diretamente no visor do aparelho, já expressos em NTU.
A acidez foi determinada através do método titulométrico, empregando a volumetria de neutralização. Foi pesado 1,00 g de amostra e diluído com a adição de 15 mL de água destilada. A solução resultante foi titulada com uma solução padronizada 0,01 mol L-1 de NaOH, empregando como indicador a fenolftaleína a 1%. O ponto de viragem da titulação foi apontado pelo aparecimento de coloração rosa na solução e anotado o volume de NaOH gasto na bureta. A acidez foi determinada pela equação (5), em que V é o valor em mL de solução de NaOH 0,01mol L-1 gasto na titulação; Fc é o fator de correção da solução de NaOH 0,01mol L-1 ; N é a concentração de NaOH e A é a massa da amostra.

A determinação de cor das amostras de mel utilizou um espectrofotômetro UV-Vis, operando em comprimento de onda de 560 nm, com cubetas ópticas de volume igual a 4,5 mL e 1 cm de caminho óptico, além de se usar glicerina pura como referência. Através da leitura direta do visor do equipamento, a absorbância foi registrada e posteriormente transformada para mm de Pfund, de acordo com a equação (6), e a classificação da coloração do mel, feita pela escala de Pfund, disposta na Tabela 1.

A determinação de cinzas totais (CT) foi executada através do método gravimétrico. Foram pesados 2,0 g de mel em cadinhos de porcelana de 75 mL, de forma alta, que foi antecipadamente seco em estufa a 105 ºC por 24 h. Logo após a pesagem, o conjunto cadinho mais amostra foi levado para incineração em forno mufla a 450º C até as amostras serem convertidas a cinzas brancas e a massa mantida constante, sendo, em seguida, esfriada em dessecador até a temperatura ambiente e pesadas. O teor de cinzas totais foi determinado através da equação (7), onde mf é a massa após a incineração; mc é a massa do cadinho; e mi é a massa inicial do mel.

Para a determinação de AR, a metodologia empregada foi o método titulométrico, que é conhecida como método de Lane-Eynon. Tal método se baseia na capacidade dos açúcares redutores, como a glicose e a frutose, reduzirem o cobre presente na solução cuproalcalina (soluções de Fehling), mantida sob ebulição (Cecchi, 2003). Para a análise de cada uma das amostras de mel, foi preparada uma solução de mel a 20 % (m/v) e desta se retirou uma alíquota de 5,0 mL, sendo transferida para balão volumétrico de 100,0 mL. Esta solução foi titulada com outra solução contendo 5,0 mL de solução de Fehling A e 5,0 mL de solução Fehling B, mais 20,0 mL de água e uma gota de solução 1% de azul de metileno, como indicador. Os resultados foram encontrados utilizando a seguinte equação (8), onde T é o título da solução de Fehling; V é o volume em mL de amostra gasta na titulação; P é a massa da amostra, em gramas.

3.3 Análises Estatísticas
As análises estatísticas descritivas foram executadas via Excel 2010 e os resultados expressos em termos de média e desvio padrão correspondentes a análises executadas em triplicata. Testes t de Student para dados não pareados e análises multivariadas foram executadas no programa MINITAB 18, sendo que a análise de componentes principais (ACP) foi conduzida com dados padronizados e a análise hierárquica de agrupamentos (AHA) foi realizada se considerando distâncias euclidianas e ligações simples e resultados expressos em termos de similaridade entre as amostras, em um dendrograma. Um nível de significância de 95 % foi considerado em todos os testes.
4 RESULTADOS E DISCUSSÕES
4.1 Resultados Físico-Químicos
Os resultados obtidos para as variáveis físico-químicas estão dados nas Tabelas 2 e 3.
Tabela 2. Resultados de condutividade elétrica, pH, viscosidade, sólidos insolúveis totais, sólidos solúveis totais

Legenda: M1-10 amostras de mangue, C1-10 amostras de capoeira. CE = condutividade elétrica; SST = sólidos solúveis totais; SIT = sólidos insolúveis totais. Valores médios seguidos de desvio-padrão. Letras iguais sobre as médias de uma variável significa não haver diferença significativa conforme teste t de Student para dados não pareados e 95 % de confiança.
Fonte: Os autores (2024).
A CE média dos méis foi de 0,37 mS/cm (mel de mangue) e 0,36 mS/cm (mel de capoeira), havendo diferença significativa entre elas, conforme a localidade de origem (Tabela 2). Esses resultados são superiores aos encontrados por Silva (2010), que foram entre 0,14 mS/cm e 0,35 mS/cm para méis de Apis mellífera também do Nordeste do Pará. Na legislação Brasileira não há limites estipulados para essa propriedade do mel, todavia, na legislação internacional há adoção da faixa entre 0,20 e 0,80 mS/cm como aceitável para a condutividade elétrica de méis de Apis mellífera, estando os valores encontrados no presente trabalho totalmente dentro desta faixa de valores (CAC, 1990). De acordo com Gois et al. (2013), a CE é importante por fornecer informações que dizem que o mel pode ou não ser estocado durante o inverno ou ser refrigerado. Além do mais, tal caracterização pode substituir a análise de cinzas e determinar botanicamente o mel, aumentando, ainda, seu valor dentro do mercado internacional.
Em termos de pH, os valores médios encontrados foram de 3,54 (mel de mangue) e 2,89 (mel de capoeira) (Tabela 2). Esses resultados sugerem que a localidade geográfica pode ser indicativa de diferenças nesta propriedade. Os resultados das duas regiões estão próximos daqueles encontrados por Menezes, Mattietto e Lourenço (2018) que obtiveram para méis não pasteurizado pH de 3,46. Já Welke et al. (2008), para méis de A. mellífera produzidos em dois anos consecutivos, cujo valores de 2005 (pH = 4,0) e 2006 (pH = 3,8) apresentaram pHs próximos aos aqui pesquisados, bem como os achados por Júnior et al. (2020) que encontrou uma variação de pH para o município de Santa Maria do Pará de 3,12. Esta discrepância pode ser dada pela época de coleta, composição do solo, espécies vegetais, alterando as suas características físico-químicas (Júnior et al., 2020). Todas as amostras também estiveram próximo dos méis de Apis mellífera da região Sul do Estado de Tocantins, sendo que Abadio Finco, Souza e Silva (2010) encontraram pH médio igual a 3,7, com um máximo de 4,2. A legislação brasileira também não possui valores definidos para essa propriedade físico-química, mas esta caracterização é importante, pois ela avalia a qualidade dos méis, tanto do ponto de vista fermentativo, quanto ao processo de adulteração (Welke et al., 2008). Há de ser ressaltado que tal parâmetro é fundamental para a atividade antimicrobiana e antifúngica, de forma que o elevado pH pode deixar o mel suscetível ao crescimento de fungos (Gois et al., 2013).
Os resultados obtidos para a viscosidade dos méis foram de 2.473,91 cSt (mel de mangue) e 305,48 (mel de capoeira) (Tabela 2) sendo esses valores significativamente discrepantes entre si. Sodré et al. (2007) encontraram viscosidade mínima para méis A. mellífera de 1.130 cSt e máximos de 2.080 cSt, valores estes dentro da faixa para as amostras do mangue. As propriedades reológicas dos méis são dependentes de vários fatores, como: conteúdo de água, temperatura, composição, proteínas, açúcares, proteínas, entre outros. Além do mais, a viscosidade é uma das propriedades mais importantes do mel, por afetar os aspectos sensoriais do alimento e de processamento deste. Portanto, dentro do processo de controle de qualidade, a determinação deste parâmetro pode ser essencial para linhas de produção, planejamento de equipamentos e processos (Parpellim, 2016; Queiroz et al., 2007; Yanniotis, Skaltsi, Karaburnioti, 2006). Dado a sua importância, a legislação nacional e internacional carece de valores específicos para essa propriedade.
As médias obtidas para a análise de SIT foram de 0,28 % (mel do mangue) e 0,40 % (mel de capoeira) (Tabela 2), sendo esses valores significativamente distintos entre si. A legislação nacional estabelece um limite máximo de SIT de 0,1 % (Brasil, 2000). Desta forma, os méis analisados extrapolaram tal limite, e transgrediram o que determina a IN de nº 11 de 2000, que determina que as análises macro e microscópicas devem estar livres de insetos, larvas, cera, areia, entre outros. Porém, isso ocorreu também em estudo de mel feito por Silva (2010), que encontrou 25 % de suas amostras com valores superiores ao máximo estabelecido na legislação. Dias et al. (2009) descobriu diferentes porcentagens de sólidos insolúveis para seis amostras de mel, que apresentaram intervalos de 0,04% a 0,32%, sendo o último valor mais próximo com o mel de capoeira aqui investigado. Por outro lado, os valores achados por Evangelista-Rodrigues et al. (2005) para méis de abelha Apis e Meliponas estão todos de acordo com o que determina a legislação nacional (0,01%) e discrepantes com os aqui descobertos. Da mesma forma, Schlabitz, Silva e Souza (2010) tiveram resultados para 12 amostras de méis de diferentes floradas produzidas no Vale do Taquari valores que vão de 0,08% a 0,12%, sendo nenhum desses próximos com os pesquisados. A presença de quantidade considerável de sólidos insolúveis pode estar atrelada a vários fatores: quantidade significativa de matéria terrosa, partes de inseto (inclusive resíduos das próprias abelhas), não decantação e/ou filtração no final do processo de retirada do mel, alterando a pureza do produto final (Dias et al., 2009). O valor médio encontrado para os méis de capoeira foi o mais elevado em termos de SST (77,00º Brix), já para os méis de mangue a média foi de 75,81º Brix (Tabela 2). Não existe limite legal para essa propriedade do mel de Apis mellífera, haja vista que inexiste na legislação brasileira valores máximos ou mínimos para tal propriedade. Lacerda et al. (2010) encontraram resultados para SST que variaram de 77,00º Brix a 83,30º Brix para méis do Sudoeste da Bahia, valores esses se aproximam aos obtidos para as amostras. Méis de Apis mellífera produzidos no sertão Paraibano tiveram valores de SST que variaram de 61,7 ºBrix a 81,17º Brix e estão dentro da faixa dos valores obtidos para os dois ecossistemas (Oliveira et al., 2013). Porém, foram totalmente contrários a aqueles analisados por Santos (2016) para amostras de méis de Apis da comunidade Solta no município de Carolina (MA), o autor encontrou SST mínimo de 78,2º Brix e máxima 82,3º Brix e média das dez amostras de 80,80º Brix, não sendo compatíveis com todas as localidades atualmente pesquisadas. O teor de SST fornece informações a respeito dos sólidos que estão dissolvidos em água, expresso em gramas, e está intrinsecamente relacionado a quantidade de açúcares no mel, sendo em grande quantidade neste alimento (Gois et al., 2015).
Os resultados médios para densidade foram de: 1,30 g mL-1 tanto para o mel de mangue como para o mel de capoeira (Tabela 2). A legislação nacional quanto a internacional carece de dados a respeito sobre essa propriedade física para méis de abelha. No entanto, Silva (2010) teve resultados de densidade mínimos de 1,376 g mL-1 e máximos de 1,415 g mL-1, com uma média de 1,405 g mL-1, onde todos os valores estiveram concatenados com o do presente estudo. Bendini e Souza (2008) também estiveram alinhados com os valores das densidades dos méis de todos os municípios, onde dispuseram de uma média de 1,41 g mL-1 e intervalos de 1,34 g mL-1 a 1,44 mL-1 para a região do Nordeste do Brasil. Por outro lado, Silva e colaboradores (2018) alcançaram valores de 1,41 g mL-1 a 1,49 g mL-1 para méis comercializados em feiras livres do município de Assis de Chateaubriand, Paraná, sendo então, todas as amostras divergentes com os resultados encontrados.
Tabela 3. Resultados de umidade, turbidez, cor, acidez, açúcares redutores (AR) e cinzas totais encontrados para as amostras de mel Apis mellífera de Tracuateua, Pará

Legenda: M1-10 amostras de mangue, C1-10 amostras de capoeira. AR= Açúcares Redutores, CT = cinzas totais. Valores médios seguidos de desvio padrão. Letras iguais sobre as médias de uma variável significa não haver diferença significativa conforme teste t de Student para dados não pareados e 95 % de confiança.
Fonte: Os autores (2024).
Os valores médios encontrados para umidade dos méis foram de 21,00 % (mel de mangue) e 22,00 % (mel de capoeira), sendo valores significativamente diferentes entre si (Tabela 3). A legislação brasileira (Brasil, 2000) define o limite máximo de umidade para méis de 20 %, sendo assim, tanto as amostras do mangue como as de capoeira estão com a umidade média acima do limite legal, o que pode estar relacionado aos próprios ecossistemas da região, processamento indevido ou colheita inoportuna (Meireles; Cançado, 2003). Porém, em seu trabalho com mel de abelha do Pará, Silva (2010) encontrou um intervalo de umidade em suas amostras entre 18,5 % e 22,0 %, estando essa faixa condizente para a maioria dos valores encontrados no presente trabalho. Segundo Gois et al. (2013) a umidade se constitui no segundo componente em termos percentuais de massa do mel, e é uma propriedade importante, pois influencia na sua viscosidade, densidade, maturidade, sabor e conservação, além do fato de que os microrganismos tolerantes açúcar, que estão presentes nos corpos das abelhas, no néctar, no solo, nas áreas de extração e armazenamento podem provocar fermentação no mel quando o teor de água for muito alto. É importante ressaltar que em região costeira, como Tracuateua, o teor de umidade pode ser acima do especificado por conta da propriedade de higroscopicidade do mel.
As médias encontradas para a turbidez das amostras de mel foram de 9,16 NTU (mel de mangue) e 20,63 NTU (mel de capoeira) (Tabela 3). A legislação não estabelece limites de turbidez para méis de Apis mellífera, porém, para Huidobro e Simal (1984) a turbidez é um parâmetro para o seu controle de qualidade, haja vista que está relacionado à quantidade de matéria em suspensão, que pode corresponder a outras partes que não seja o mel. Tal característica, de acordo com a Farmacopeia Brasileira (2022), fornece valores quantitativos de substâncias em função da turbidez das suspensões, na qual apresenta proporcionalidade ao efeito Tyndall. Okaneku e colaboradores (2020) realizaram análises de turbidez em três amostras de méis de abelha A. mellífera adquiridas em uma feira livre do município de Manaus em diferentes meses. Os resultados dos autores foram bem acima do que os aqui encontrados, sendo que para a amostra A obtida por eles em outubro de 2018 apresentou turbidez de 67,40 NTU, amostra B de fevereiro de 2019 alcançou 87,40 NTU, ao passo que a amostra C no período de maio de 2019 teve turbidez de 28,83 NTU.
Em termos de sua cor, as amostras das duas localidades apresentaram uma absorbância média que caracterizou esses méis como sendo do tipo “extra-branco” (Tabela 3). Esses valores estão consonantes com a legislação brasileira (2000) que define a aceitabilidade do mel, enquanto os aspectos de cores, variações dentro do branco-água a âmbar escuro. As amostras de mel mais escuras apresentam maior atividade antioxidante por conta da maior presença de compostos fenólicos, sendo um alimento apropriado para uma alimentação saudável (Gomes, 2009). Lacerda et al. (2010) encontraram um perfil de cores obtidos em amostras de A. mellífera entre 25 % de cor branco, 17 % de cor Âmbar claro, 13 % de cor Branco-água, e 4 % de cor Extra-branco. Freitas et al. (2022) encontraram cores de méis de Apis da região da Ilha do Marajó que variaram do Âmbar extra-claro ao Âmbar-escuro que estão dentro do limite legal, contudo, divergentes para a maioria das amostras. Vale ressaltar que pelo estudo do autor ser realizado com méis de A. mellífera em região do Nordeste paraense, a diversidade botânica, fatores climáticos, armazenamento, minerais, temperatura do mel durante na colmeia, localização geográfica pode ser determinante para esta característica sensorial (Mantilla et al., 2012; Gois et al., 2013), ao comparar com as outras seis localidades do Nordeste Paraense. Durante o processo de extração do mel é importante cuidados durante a sua manipulação, tendo em vista que pode ocorrer contaminação, perpassando desde a escolha do recipiente para armazenagem, contato com resíduos, fuligem de fumaça, local inapropriado, entre outros (Mantilla et al., 2012).
Os valores médios para os teores de acidez titulável foram de 2,44 meq/kg (mel de mangue) e 1,98 meq/kg (mel de capoeira) (Tabela 3). Todas as amostras estão de acordo com o que determina a Instrução Normativa Nº 11 do Ministério da Agricultura, Pecuária e Abastecimento, que estabelece que a acidez máxima em méis deve ser de até 50 meq/kg (Brasil, 2000). Dessa forma, esses valores indicam a inexistência de fermentação nos méis, aprovando as amostras investigadas. Sodré et al. (2007) encontrou valores de acidez mínimo de 10 meq/kg e máximo de 42 meq/kg para méis Apis do Estado do Ceará, enquanto Welke et al. (2008) obtiveram médias de 30,1 a 39,8 meq/kg, valores estes que estão bem acima para os resultados das todas as amostras , mas ainda dentro do especificado pela legislação. De Moura Júnior et al. (2021) encontrou resultados mais próximos com o do presente estudo, com teores de acidez de 1,68 meq/kg a 4,70 meq/kg. Alves (2008) aponta que a acidez do mel é devida aos minerais e ácidos orgânicos nele contido, sendo que o principal ácido é o glutâmico que se forma pela ação da enzima glicose-oxidadse produzida nas glândulas hipofaringeanas das abelhas e pela ação das bactérias ao longo do processo de maturação do mel. Já Marchini et al. (2004) relatam que a acidez do mel atua na estabilidade do produto frente ao desenvolvimento microbiológico, pois apresenta diversos ácidos nele dissolvidos: acético, benzóico, butírico, cítrico, fenilacético, glucônico, isovalérico, láctico, maléico, oxálico, propiônico, piroglutânico, succínico e valérico, que produzem íons de hidrogênio.
As médias obtidas para os AR foram de 60,03 % (mel de mangue) e 60,61 % (mel de capoeira) (Tabela 3), sendo que todas as médias indicaram não haver diferenças estatísticas significativas entre si, e estão abaixo do preconizado pela legislação brasileira, que estipula um valor mínimo de 65 % (Brasil, 2000), porém em conformidade com valores aceitos internacionalmente, onde se estipula um mínimo de 60 % (CAC, 2001). Caracterizando mel de A. mellífera scutellata produzida no Pantanal, na sub-região da Nhecolândia, Bertoldi, Gonzaga e Reis (2004) encontraram valor médio de açúcares redutores de 68,20 %, estando acima das amostras dos dois ecossistemas paraenses pesquisados no presente trabalho. É valido salientar que este parâmetro contribui na pressão osmótica de méis de abelha, contribuindo na sua conservação, haja vista que o açúcar em grande quantidade, cria um meio inóspito para o desenvolvimento de bactérias, algumas leveduras e mofos (Gava, 1984; Silva, 2006). Tais resultados sugerem que as amostras estudadas são suscetíveis a reprodução e ação desses microrganismos, requerendo cuidados quanto a sua estocagem e conservação.
O teor de CT médios encontrados foram de 0,14 % (mel do mangue) e 0,16% (mel de capoeira) (Tabela 3). Por ser uma determinação intrinsecamente ligada à pureza, a legislação nacional determina como limite máximo para o teor de CT de mel de abelha o valor de 0,60 % (ou 0,6g/100g) (Brasil, 2000). Assim sendo, as amostras, estiveram concordantes com o limite legal estipulado, comprovando a pureza dos méis testados. Esses valores também são inferiores aos encontrados por De Moura Júnior et al. (2021) que obtiveram um intervalo entre 1,45 % e 3,05 % para amostras de méis Apis do Nordeste do Pará. Segundo Bertoldi et al. (2010), as cinzas totais expressam a quantidade de minerais presentes no mel de abelha, sendo que, em geral, o seu teor é relativamente baixo, sendo que a variação de tal teor se deve principalmente ao tipo de solo onde o néctar das flores foi coletado. Desta forma o mel proveniente do ecossistema mangue deve apresentar uma maior concentração de elementos minerais do que os méis de capoeira.
4.2 Resultados das Análises Multivariadas
A aplicação da técnica multivariada de análise de componentes principais (ACP) aos dados referentes as sete variáveis físico-química que mostraram diferença entre os dois grupos de amostras, mel de mangue (M1 a M10) e de capoeira (C1 a C10), de acordo com o teste t de Student aplicado (Tabelas 2 e 3) gerou o gráfico das duas componentes principais apresentado na Figura 3.
Figura 3. Gráfico das duas primeiras componentes principais (CP)

Fonte: Os autores (2024).
Observa-se uma perfeita separação das amostras em dois grupos distintos, um do lado direito do gráfico que é formado pelas dez amostras de mel do ecossistema de mangue, e o outro do lado esquerdo do gráfico, formado pelas dez amostras de mel de capoeira. Isso evidencia que as variáveis estudadas são suficientes para discriminar os méis de acordo com o ecossistema de origem. Também pode-se inferir que os méis desses dois ecossistemas são de constituições distintas. A Tabela 4 apresenta as contribuições de cada uma das sete variáveis usadas sobre cada uma das sete componentes principais formadas e apresenta a porcentagem de explicação do modelo devida a cada uma das sete componentes geradas pela técnica de ACP.
Tabela 4. Contribuição (peso) de cada variável para cada uma das sete variáveis empregadas em ACP
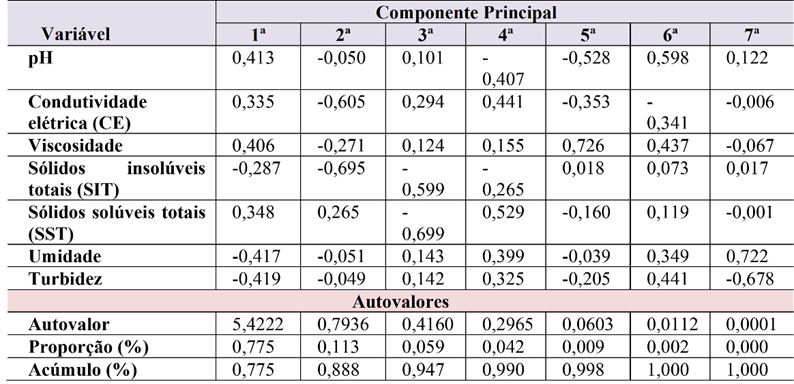
Fonte: Os autores (2024).
A primeira componente principal explica 77,5 % da variabilidade dos dados e a segunda explica 11,3 %, sendo que juntas, essas duas componentes acumulam 88,8 % da explicação do modelo, logo são suficientes paras as análises, o que se confirma na Figura 4, onde aparece o gráfico dos autovalores associados a cada uma das componentes principais. Neste gráfico se percebe que após a 2ª componente principal, a linha se torna praticamente uma reta horizontal, indicando o pouco acréscimo de informações dadas pelas componentes de ordem superior a dois.
Figura 4. Gráfico dos autovalores associados a cada uma das componentes principais

Fonte: Os autores (2024).
Pelos pesos das variáveis contribuintes na formação da primeira componente principal, dados na Tabela 4, nota-se que todas as variáveis tiverem uma contribuição semelhante ao modelo, pois seus pesos, em módulos são muito próximos, sendo o SIT a variável que menos contribui, tendo um peso, em módulo, de 0,287. Assim, as sete variáveis contribuem significativamente para agrupar as amostras de acordo com o ecossistema de origem. Já a segunda componente principal teve maior influência das variáveis CE e SIT, quase foi desprezível as contribuições das outras cinco variáveis. Assim sendo, CE e SIT são as variáveis que mais contribuíram para a dispersão ocorrida dentro dos dois grupos.
A aplicação da técnica AHA, considerando dados padronizados, ligações completas e distâncias euclidianas, gerou o dendrograma contido na Figura 5.
Figura 5. Dendrograma para as amostras de mel estudadas

Fonte: Os autores (2024).
No dendrograma aparecem dois grupos de amostras que apresentam total falta de similaridade, ou seja, são grupos formados por dez amostras cada, que podem ser considerados totalmente diferentes entre si, do ponto de vista das variáveis estudadas. Desta forma a AHA confirma os resultados apresentados pela ACP.
5 CONSIDERAÇÕES FINAIS
Os méis de Tracuateua, tanto da região de mangue como de capoeira, se mostraram concordantes em termos das principais propriedades físico-químicas, podendo ser considerados de boa qualidade, mas se devendo ter cuidado com sua armazenagem, precisando ser armazenados em potes de plástico ou vidro devidamente esterilizados, de preferência escuros e guardados em geladeiras, evitando-se o calor excessivo, para evitar possível desenvolvimento microbiológico e consequente fermentação não desejada, pois apresentam quantidades de água (umidade) mais elevada que o estipulado por lei, o que pode favorecer o desenvolvimento de microrganismos.
Os méis foram distinguidos em termos de sua origem, o ecossistema onde se desenvolveram, através de sete variáveis físico-químicas (pH, condutividade elétrica, turbidez, sólidos solúveis totais, sólidos insolúveis totais, viscosidade e umidade)e as técnicas estatísticas multivariadas de ACP e AHA, podendo, então, serem identificadas conforme sua origem, e, assim, as informações contidas neste trabalho poderá contribuir com o controle de qualidade do produto.
REFERÊNCIAS
ADOLFO LUTZ. Normas Analíticas do Instituto Adolfo Lutz. Métodos químicos e físicos para análise de alimentos. 4. ed. São Paulo: IMESP, 2008.
ALVES, E. M. Identificação da flora e caracterização do mel orgânico de abelhas africanizadas das Ilhas Floresta e Laranjeira, do Alto Rio Paraná. 63 f. Tese (Doutorado em Zootecnia)–Universidade Estadual de Maringá, Maringá, PA, 2008.
ANANIAS, K. R. Avaliação das condições de produção e qualidade do mel de abelhas (Apis melliferas L.) produzida na microrregião de Pires do Rio, no estado de Goiás. 2010. 70 f. Dissertação (Mestre em Ciência e Tecnologia de Alimentos) – Escola de agronomia e engenharia de alimentos: Universidade Federal de Goiás, Goiás, 2010.
AOAC. Association of Official Analytical Chemists. Official Methods of Analysis of AOC International. 17 ed. Horwitz, W. Association of Official Analytical Chemists: Gaithersburg, MD, 2000. p. 22 – 33.
AROUCHA, E. M. M.; DE OLIVEIRA, A. J. F.; NUNES, G. H. S.; MARACAJÁ, P. B.; SANTOS, M. C. A. Qualidade do mel de abelha produzidos pelos incubados da Iagram E Comercializado No Município De Mossoró/RN. Revista Caatinga. Mossoró, v. 21, n. 1, p. 211-17, jan./mar., 2008.
BALATA, R. A. CARACTERIZAÇÃO DA CRIAÇÃO DE ABELHAS AFRICANIZADAS (Apis melifera L.) EM UM ECOSSISTEMA DE MANGUE – CAMPO DE PERIZES–MA. 2008.Dissertação (MESTRADO EM AGROECOLOGIA) Universidade Estadual do Maranhão, São Luiz, 2008.
BERTOLDI, F.C.; DOS REIS, V. D. A.; GONZAGA, L. V.; CONGRO, R. F. C. R.. Mel Silvestre: Qualidade para a Valorização e Competitividade da Apicultura no Pantanal. Boletim de Pesquisa e Desenvolvimento 98. Corumbá: Embrapa Pantanal, 2010.
BERTOLDI, F. C.; GONZAGA, L.; REIS, V. D. A. Características físico-químicas do mel de abelhas africanizadas (Apis mellifera scutellata), com florada predominante de hortelã-do-campo (Hyptis crenata), produzido no Pantanal. In: IV Simpósio sobre Recursos Naturais e Sócio-econômicos do Pantanal. Anais… Corumbá, 2004.
BÖHLKE, P. B.; PALMEIRA, E. M. Inserção competitiva do pequeno produtor de mel no mercado internacional. Rev Acad Economía, v. 71, p. 1-7, 2006.
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Instrução Normativa nº11 de 20 de outubro de 2000. Aprova o Regulamento Técnico de Identidade e Qualidade do Mel. Diário Oficial da União, Brasília, DF, 23 de outubro de 2000.
BRUDZYNSKI, K.; ABUBAKER, K.; CASTLE, A. Re-examining the role of hydrogen peroxide in bacteriostatic and bactericidal activities of honey. Frontiers in microbiology, v. 2, p. 213, 2011.
CAC. CODEX ALIMENTARIUS COMMISSION. CAC/VOL III, Suppl. 2. ed. 1. Roma: FAO/WHO, 1990.
CAC. CODEX ALIMENTARIUS COMMISSION. CODEX STAN 12: Revised Codex Standard for Honey, Standards and Standard Methods, Food and Agriculture Organization of The United Nations, v. 11, 2001. 7 p.
CAMARGO, R. C. R. de. Produção do Mel. Sistemas de Produção, Teresina: Embrapa, 2002.
CECCHI, H. M. Fundamentos Práticos e Teóricos em Análise de Alimentos. 2ª Edição. Editora UNICAMP, 2003.
DA SILVA, D. O.; CARVALHO, N. C. NARRATIVAS DE CRIANÇAS SOBRE O SABER/FAZER EM FESTAS AMAZÔNICAS: O CASO DA MARUJADA DE SÃO BENEDITO E SÃO SEBASTIÃO EM TRACUATEUA/PA. NOVA REVISTA AMAZÔNICA, v. IX, n.01, 2021. ISSN: 2318-1346.
DA SILVA, I. A. A.; DA SILVA, I. A. A.; DA SILVA, T. M. S.; CAMARA, C. A.; QUEIROZ, N.; MAGNANI, M.; DE NOVAIS, J. S.; DE SOUZA, A. G. Phenolic profile, antioxidant activity and palynological analysis of stingless bee honey from Amazonas, Northern Brazil. Food chemistry, v. 141, n. 4, p. 3552-3558, 2013. DOI: 10.1016/j.foodchem.2013.06.072.
DA SILVA, T. C.; DA CONCEIÇÃO, M. E. C.; DE SOUSA, D. B.; CASTRO, L. M. R. FLORÍSTICA DO ESTRATO HERBÁCEO-SUBARBUSTIVO EM CAPOEIRA NA REGIÃO DO XINGU, PARÁ-BRASIL. ENCICLOPÉDIA BIOSFERA, Centro Científico Conhecer – Jandaia-GO, v.21 n.48; p. 101-113, 2024. DOI: 10.18677/EnciBio_2024B9.
DE MOURA JUNIOR, J. M. N., NEGRÃO, C. A. B.; ROCHA, R. M.; DE SOUZA, E. C.; SILVA, A. S. Estudo Físico-Químico e Quimiométrico de Méis do Estado do Pará. Rev.virtual Quim., v 13, n.1, p. 222- 233, 2021.
DERAL. Divisão de Conjuntura Agropecuária. Boletim semanal: MEL, 2021.
ESCOBAR, A. L. S.; XAVIER, F. B. Propriedades fitoterápicas do mel de abelhas. Uningá Journal, v. 37, n. 1, 2013.
DUKE, N. C.; BALL, M. C.; ELLISON, J. C. Factors influencing biodiversity and distributional gradients in mangroves. Global Ecology and Biogeography Letters, n. 7, p. 27– 47, 1998.
GAVA, A. J. Princípios de Tecnologia de Alimentos. São Paulo, SP: Editora Nobel, 1984.
GOIS, G. C.; DE LIMA, C. A. B. ; DA SILVA, L. T.; EVANGELISTA-RODRIGUES, A.. COMPOSIÇÃO DO MEL DE APIS MELLIFERA: REQUISITOS DE QUALIDADE. Acta Veterinaria Brasilica, v.7, n.2, p.137-147, 2013.
HAMMAD, M. B. BEES AND BEEKEEPING IN ANCIENT EGYPT. Journal of Association of Arab Universities for Tourism and Hospitality, v. 15, n. 1, p. 1-16, 2018.
HUIDOBRO, J. F.; SIMAL, J. Determinacion del color y de la turbidez en las mieles. Analytical Bromatology, v. 36, p. 225-245, 1984.
IBGE. INSTITUTO BRASILEIRO DE GEOGRAFIA E ESTATÍSTICA . Geoestatísticas de recursos naturais da Amazônia Legal, 2011. Disponível em: < http://www.ibge.gov.br/home/geociencias/recursosnaturais/diagnosticos_levantamentos/amazonia_legal/a mazonia_legal.pdf>. Acesso em: 20 dezembro 2022.
JAMES ONNING. Ilustração da distribuição dos manguezais no Brasil. [S.l.:s.n.], 2012.
KUENZER, C.; BLUEMEL, A.; GEBHARDT, S.; QUOC, T.; DECH, S. Remote sensing of mangrove ecosystems: a review. Remote Sensing, n. 3, p. 878-928, 2011.
LONDE, V.; SALLES, D. M.; LEITE, M. G. P.; ANTONINI, Y. ESTRUTURA DA VEGETAÇÃO DE MANGUE ASSOCIADA AO GRADIENTE DE INUNDAÇÃO NO LITORAL NORTE DO ESPÍRITO SANTO, BRASIL. Revista Árvore, Viçosa-MG, v.37, n.4, p.629-637, 2013.
MARCHINI, L. C.; SODRÉ, G. S.; MORETI, A. C. C. C.. Mel brasileiro: composição e normas. Ribeirão Preto: A. S. Pinto, p.111, 2004.
OKANEKU, B. M.; SOUZA, A. Q. L.; ARAÚJO, D. L.; ALVES, T. C. L.; CARDOSO, D. N. P.; SANTOS, W. G.. Análise físico-química e microbiológica do mel de abelhas africanizadas (Apis mellifera). Tecnologia de Alimentos: Tópicos Físicos, Químicos e Biológicos – Volume 1, 2020.
OLIVEIRA, F. D. C.; MEDEIROS, C. D. C.; MORAES, F. A. D. S. Análise de mel de abelha coletado em comércio informal na cidade de Teresina, PI. Higiene Alimentar, 3 (268-269), P.01-05, 2017
PEREIRA, C. A.; VIERIRA, I. C. G.. A importância das florestas secundárias e os impactos de sua substituição por plantios mecanizados de grãos na Amazônia. Interciencia 26(8): 337-341, 2001.
ROSA, A. G.; PEREIRA, F. S.; COSTA, A. N. M.; PINHEIRO, C. P. S.. Estudo climatológico dos eventos extremos de precipitação no município de Tracuateua, PA (Brasil). Revista Ibero Americana de Ciências Ambientais, v.12, n.1, p.192-201, 2021. DOI: http://doi.org/10.6008/CBPC2179-6858.2021.001.0016.
RYBAK-CHMIELEWSKA, H.; SZCZÊSNA, T. HPLC study of chemical composition of honeybee (Apis mellifera L.) venom. Journal of Apicultural Science, v. 48, n. 2, p. 103-109, 2004.
SALOMÃO, R. P.; VIEIRA, I. C. G.; BRIENZA JÚNIOR, S.; AMARAL, D. D.; SANTANA, A. C. Sistema Capoeira Classe: uma proposta de sistema de classificação de estágios sucessionais de florestas secundárias para o estado do Pará. Bol. Mus. Para. Emílio Goeldi. Cienc. Nat., Belém, v. 7, n. 3, p. 297-317, 2012.
SANTOS, J. O. dos et al. Um estudo sobre a evolução histórica da apicultura. 2015. 95 f. Dissertação (Mestrado em Sistemas Agroindustriais) – Departamento de Ciências e Tecnologia: Universidade Federal de Campina Grande, Pombal, 2015.
SEBRAE. Serviço Brasileiro de Apoio às Micro e Pequenas Empresas. Conheça as Técnicas de Manejo para a Produção do Mel. 2019. Disponível em https://www.sebrae.com.br/sites/PortalSebrae/artigos/conheca-tecnicas-de-manejo-para-a-producao-domel,8068fa2da4c72410VgnVCM100000b272010aRCRD. Acesso em 04 março 2023.
SCHAEFFER-NOVELLI, Y. CINTRÓN, G. Métodos para la descripción y estudio de areas de manglar. In: VIVALDI, J. L. Compendio Enciclopédico de los Recursos Naturales de Puerto Rico. San Juan: Departamento de Recursos Naturales, v. 3, 1983. 49 p.
SILVA, E. V. C. Caracterização e pasteurização de méis de abelhas Melípona fasciculata (Uruçu cinzenta) e Apis mellifera (Africanizada). Dissertação (Mestrado em Tecnologia de Alimentos) – Universidade Federal do Pará, 2006. 66 p.
SILVA, R. A.; MAIA, G. A.; SOUSA, P. D.; COSTA, J. D. Composição e propriedades terapêuticas do mel de abelha. Alimentos e Nutrição Araraquara, v. 17, n. 1, p. 113-120, 2008.
VARGAS, T. Avaliação da Qualidade do Mel Produzido na Região dos Campos Gerais do Paraná. Dissertação (Mestrado em Ciência e Tecnologia de Alimentos) – Universidade Estadual de Ponta Grossa, 2006. 134 p.
VIEIRA, I. C. G.; PROCTOR, J. Mechanisms of plant regeneration during succession after shifting cultivation in eastern Amazonia. Plant Ecology 192(2):303-315, 2007.
VISCONDE, J. V. et al. Estrutura organizacional da atividade apícola nos municípios de Silvânia, Vianópolis e Orizona, Goiás. 2016. 86 f. Dissertação (Mestre em Zootecnia) – Escola de veterinária e zootecnia: Universidade Federal de Goiás, Goiânia, 2016.
WOODROFFE, C. D.; GRINDROD, J. Mangrove biogeography the role of Quaternary environmental and sea-level change. Journal of Biogeography, n. 18, p. 479-492, 1991.
1 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: gilberto.vale@ics.ufpa.br
2 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: matheusramon93@gmail.com
3 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: marcos.amaro@ics.ufpa.br
4 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: silvarennan738@gmail.com
5 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: marllonfreitaaas@gmail.com
6 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: nelianogoncalves84@gmail.com
7 Discente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém, e-mail: caioh.borges18@gmail.com
8 Docente do Curso Superior de Agronomia do Instituto de Ciências Agrárias da UFRA, Campus Belém. Doutor em Química (PPGQ/UFPA). e-mail: ewerton.carvalho@ufra.edu.br.
9 Docente do Curso Superior de Farmácia do Instituto de Ciências da Saúde da UFPA, Campus Belém. Doutor em Química (PPGQ/UFPA). e-mail: ansansil@ufpa.br.
