IMPACT OF STATIN THERAPY ON STABILIZATION OF ATHEROSCLEROTIC PLAQUES
REGISTRO DOI: 10.69849/revistaft/ra10202502191720
Cleiane Santana Pinheiro de Moraes1; Suelen Garcia Machado1; Patrícia Sebastiana Duarte1; Rafael Dolci Kloster1; Marina Braga Silveira2; Lucas Henrique Lins2; Jéssica da Silva Nogueira2; Brenda Luiza Teixeira Izabel2; Rafael Pontes de Oliveira2; Layanne Pires Amorim Santos2; Rafael Caldas Trindade2; Mônica Vassi Cardoso2; Vívian Piva Luz da Maia2; Guilherme Valente Jorge2; Raony Ramalho Tavares3
Resumo
La Enfermedad Aterosclerótica (EA) o aterosclerosis es un proceso inmunoinflamatorio crónico caracterizado por el depósito de grasa, calcio y otros elementos principalmente en la pared de arterias medianas y de grandes calibres, reduciendo su luz y provocando un déficit sanguíneo en los tejidos irrigados por ellas. Para el tratamiento clínico se desarrolló la terapia con fármacos que actúan estabilizando la placa aterosclerótica dentro de las arterias, destacando el uso de las estatinas, que de todos los fármacos con acción hipolipemiante, son los más recetados y se utilizan para tratar la dislipidemia sin eliminar la necesidad de realizar cambios en el estilo de vida. Por tanto, el objetivo de este estudio es demostrar la importancia del uso de estatinas en la estabilización de las placas ateroscleróticas, además de analizar sus daños y beneficios. Las bases de datos utilizadas en la investigación fueron Google académico, LILACS y PUBMED, fueron seleccionados artículos publicados entre 2019 y 2024, en portugués, español e inglés. Las estatinas se consideran los únicos agentes farmacológicos que han demostrado de manera realista efectos anti ateroscleróticos, cabe mencionar los diferentes tipos de estatinas disponibles, destacando el principal factor diferenciador que es la capacidad de reducir los niveles de colesterol LDL. Apesar de los avances significativos en la prevención y el tratamiento de la EA, persisten desafíos en la implementación efectiva de estrategias de prevención primaria y secundaria. Por tanto, está claro que las estatinas favorecen la regresión y estabilización de la placa de ateroma.
Palavras-chave: estatinas. aterosclerosis. placas de ateroma. colesterol. tratamiento.
1 INTRODUCCIÓN
Según la Organización Mundial de la Salud (OMS), las enfermedades cardiovasculares son consideradas la principal causa de morbilidad y mortalidad a nivel mundial y la principal causa de muerte en las últimas cinco décadas. Las enfermedades cardiovasculares (ECV) se definen como enfermedades crónicas no transmisibles (ENT), siendo una combinación de problemas que afectan al corazón y los vasos sanguíneos, y la mayoría de las veces están relacionados con malos hábitos de vida, que pueden incluir la dieta y la falta de actividad física (1).
La Enfermedad Aterosclerótica (EA) o aterosclerosis es un proceso inmunoinflamatorio crónico caracterizado por el depósito de grasa, calcio y otros elementos principalmente en la pared de arterias medianas y de grandes calibres, reduciendo su luz y provocando un déficit sanguíneo en los tejidos irrigados por ellas. Su desarrollo es lento y progresivo, debiendo existir una obstrucción arterial importante, en torno al 75% del calibre de una arteria, para que aparezcan los primeros síntomas isquémicos (síntomas derivados de la falta de sangre) (1,2).
Aunque cualquier órgano o tejido del cuerpo puede verse afectado, la enfermedad aterosclerótica sintomática se localiza con mayor frecuencia en las arterias que irrigan el corazón, el cerebro, los riñones, las extremidades inferiores y el intestino delgado. El infarto agudo de miocardio (IAM), la insuficiencia cardíaca (IC) y los accidentes cerebrovasculares (ACV) son ejemplos de enfermedades cardiovasculares que resultan de la enfermedad aterosclerótica y que contribuyen a las principales causas de muerte en todo el mundo (3).
El evento que desencadena el proceso aterosclerótico es la disfunción endotelial, que inicia la respuesta inflamatoria y promueve la entrada de moléculas de colesterol ligadas a lipoproteínas de baja intensidad (c-LDL) en la pared arterial. La posterior interacción entre las partículas de c-LDL oxidadas y las células del sistema inmunitario, en particular los macrófagos, conduce a la formación de células espumosas y al inicio de la formación de placas de ateroma. Posteriormente, las células del músculo liso vascular migrarán al sitio de la lesión y contribuirán a la formación de una capa fibrosa que encapsula el núcleo lipídico. La interacción entre mediadores inflamatorios, estrés oxidativo y metabolismo lipídico aumenta la inestabilidad de la placa de ateroma, haciéndola susceptible a rotura y posterior trombosis (3).
En vista de esto, el colesterol alto en sangre es una de las principales causas de la EA, por lo que es sumamente importante mantener bajos los niveles de colesterol y LDL para reducir el riesgo cardiovascular. Para eso, las modificaciones en el estilo de vida son un componente importante cuando se trata de prevenir y tratar la EA (3,4).
Las directrices actuales sobre el manejo de la aterosclerosis recomiendan fomentar la adopción de una serie de medidas no farmacológicas con un efecto directo sobre la progresión de la enfermedad, en concreto la adopción de una dieta saludable, baja en grasas y rica en verduras, frutas y cereales integrales. Además, el ejercicio físico regular y dejar de fumar también tienen un efecto significativo en la mejora del perfil lipídico y la reducción de la inflamación (3,4).
Cuando el riesgo cardiovascular es elevado o las medidas no farmacológicas resultan insuficientes, se puede recomendar el tratamiento farmacológico. Sin embargo, para el tratamiento clínico se desarrolló la terapia con fármacos que actúan estabilizando la placa aterosclerótica dentro de las arterias, destacando el uso de las estatinas (1,3).
Las estatinas son, de todos los fármacos con acción hipolipemiante, los más recetados. Se utilizan para tratar la dislipidemia sin eliminar la necesidad de realizar cambios en el estilo de vida. Se utilizan tanto como método de prevención primaria, en el caso de niveles elevados de LDL, colesterol y triglicéridos, como de prevención secundaria, en individuos con antecedentes de un evento cardiovascular isquémico (5).
Las estatinas actúan inhibiendo la HMG-CoA reductasa, enzima encargada de convertir la HMG-CoA en ácido valónico (un precursor temprano del colesterol), inhibiendo así la síntesis de colesterol y provocando una disminución del colesterol hepático, induciendo un aumento del número de receptores de LDL y en consecuencia ocurre una disminución de los niveles plasmáticos de c-LDL. Las estatinas también tienen actividad antioxidante y antiinflamatoria, un papel importante adicional en la fisiopatología del desarrollo de la placa de ateroma (6).
Por tanto, el objetivo de este estudio es demostrar la importancia del uso de estatinas en la estabilización de las placas ateroscleróticas, además de analizar sus daños y beneficios.
De esta manera, es posible difundir información actualizada y con base científica a profesionales y académicos del área de la salud, con el objetivo de cubrir cada vez más individuos con riesgo de ECV y prevenir estos eventos.
2 METODOLOGIA
Para el desarrollo de esta revisión, pasamos por los pasos recomendados por la literatura: delimitación del tema y formulación de la pregunta guía; establecimiento de criterios para la selección de publicaciones; definición de la información a extraer de los estudios seleccionados; evaluación de los estudios incluidos en la revisión e interpretación de los datos (7).
Las bases de datos utilizadas en la investigación fueron las siguientes: Google académico, LILACS y PUBMED, fueron seleccionados artículos publicados entre 2019 y 2024, en portugués, español e inglés. Se adoptó como criterio que el artículo debía abordar al menos uno de los descriptores, a saber: placa aterosclerótica, estatinas, estabilización e inflamación crónica. Después de la evaluación inicial, todos los artículos fueron revisados en su totalidad y los que tengan que ser ajustado a lo criterio de inclusión, quedaron para la redacción del artículo de revisión.
3 MARCO TEÓRICO
La Enfermedad Aterosclerótica (EA) se caracteriza por la acumulación de lípidos y/o tejido fibroso en la íntima, la capa más interna de las arterias, provocando la aparición de una placa de ateroma, que con el tiempo puede volverse cada vez más fibrosa. Este proceso inflamatorio causa daño a la pared arterial y contribuye abrumadoramente a una tasa de mortalidad (aproximadamente la mitad o más de todas las muertes) y una morbilidad, en el mundo occidental, que supera la de cualquier otra enfermedad. Ser de distribución mundial, alcanzando proporciones epidemiológicas en sociedades económicamente desarrolladas (3).
A nivel mundial, alrededor de 620 millones de personas viven con enfermedades cardíacas y circulatorias, y desde 1997 hasta la fecha el número de personas que viven con estas enfermedades se ha duplicado. En el Paraguay, la ECV es la primera causa de mortalidad, al producir el 27% del total de muertes. La tasa de mortalidad por enfermedades del aparato circulatorio fue de 113.2 por 100,000 habitantes en el año 2017, con una tasa de mortalidad por enfermedades isquémicas del corazón de 40.2 por 100,000 habitantes (3,8).
Los factores de riesgo asociados a la EA se subdividen en factores ambientales y condiciones genéticas. El tabaquismo, una dieta rica en lípidos y el sedentarismo son factores ambientales y modificables, mientras que el género, la Diabetes Mellitus (DM), la Hipertensión Arterial Sistémica (HAS) y los antecedentes familiares tienen un fuerte componente genético y no modificables. La edad, la DM, la hipertensión, la dislipidemia y el tabaquismo son los principales factores asociados a un mayor riesgo de ECV, que tiene como principal desencadenante la aterosclerosis (9).
La patogénesis de la enfermedad aterosclerótica está relacionada con la lesión o disfunción de las células endoteliales, determinada por varios factores de riesgo, modificables o no, que crean un ambiente proinflamatorio y protrombótico, representado por el aumento de la permeabilidad vascular, la entrada de lípidos (colesterol y ésteres de colesterol), adhesión de monocitos y linfocitos sanguíneos, adhesión de plaquetas y expresión de factores de crecimiento con proliferación de fibras musculares lisas y su migración a la íntima, donde producen matriz extracelular (9).
La placa aterosclerótica así formada tendrá un núcleo lipídico, formado por colesterol y ésteres de colesterol presentes en macrófagos activados y células de músculo liso (células espumosas) o extracelularmente en forma de cristales de colesterol, linfocitos y restos necróticos, además de una capa fibrosa formado por colágeno producido por fibras musculares lisas que migraron a la íntima. La proporción variable de estos elementos determina diferentes aspectos morfológicos que, a su vez, se relacionan con diferentes comportamientos clínicos y se asocian a un riesgo cardiovascular variable (9).
El núcleo lipídico es una región hipocelular cargada de lípidos y constituye el núcleo de las placas de ateroma. A medida que se desarrolla la placa de ateroma, el núcleo necrótico aumenta de tamaño esencialmente debido a la muerte de los macrófagos y a la eferocitosis ineficiente, como se ilustra en la Figura 1. Estos fenómenos contribuyen al desarrollo de un ambiente inflamatorio y al aumento del estrés oxidativo, promoviendo la muerte de las células circundantes, como las células del músculo liso vascular, promoviendo la vulnerabilidad de la placa de ateroma (3).
La capa fibrosa se encuentra entre la luz del vaso y el núcleo necrótico y está compuesta por células de músculo liso (CML), macrófagos y linfocitos. Esta capa sirve como soporte estructural para evitar la liberación de material protrombótico del núcleo. Las células diferenciadas del músculo liso presentes en la túnica media presentan un fenotipo contráctil que garantiza el control del diámetro de los vasos sanguíneos y del flujo sanguíneo. Sin embargo, en respuesta al daño, estas células cambian su fenotipo a uno sintético, en el que prevalece la actividad migratoria y proliferativa. En consecuencia, las células espumosas, plaquetas y células endoteliales activadas estimularán la producción de factores de crecimiento, por ejemplo, las células espumosas producirán Factor de Crecimiento Derivado de Plaquetas (PDGF), citocinas y otros factores de crecimiento, contribuyendo directamente al proceso de migración y proliferación de las células del músculo liso (3).
Así, en respuesta a los estímulos generados, las células del músculo liso presentes en la túnica media migrarán a la íntima. En la íntima, estas células proliferarán y las células del músculo liso con un fenotipo sintético ahora formado aumentarán la producción de compuestos de la matriz extracelular como el colágeno intersticial, la elastina y los proteoglicanos. Estas células de músculo liso proliferantes acompañadas de la producción de matriz extracelular culminan en la formación de una capa fibrosa alrededor de la lesión formada, con el fin de evitar su rotura. Las características de la capa fibrosa, a saber, espesor, contenido celular, composición de la matriz y contenido de colágeno, son determinantes importantes de la estabilidad de la placa de ateroma (Figura 1) (3).
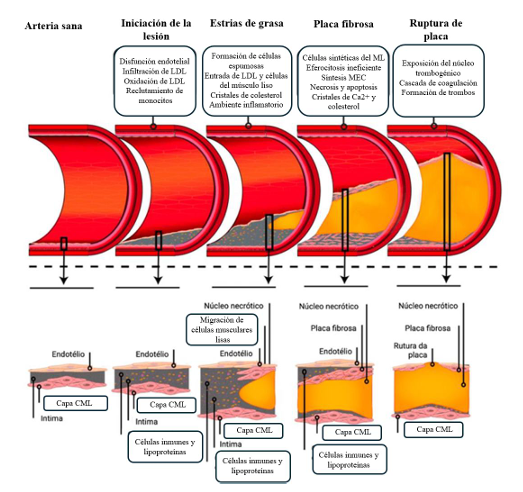
Figura 1. Representación esquemática de la formación de placas de ateroma. Fuente Adaptado (3).
La estabilidad de la placa de ateroma es un determinante importante del riesgo de eventos cardiovasculares, concretamente ictus e infarto de miocardio. La degradación de la capa fibrosa puede provocar la rotura de la placa de ateroma y desencadenar eventos trombóticos y/u oclusión del vaso afectado. La placa se considera vulnerable cuando la lesión tiene un núcleo lipídico grande, una capa fibrosa delgada y una respuesta inflamatoria aumentada. El aumento de la inflamación contribuye a la ruptura de la placa fibrosa ya que promueve la producción de proteasas como MMP y catepsinas, capaces de degradar la capa fibrosa, comprometiendo la integridad de la placa de ateroma (3).
Así, la placa de ateroma puede volverse inestable debido a una serie de factores, entre ellos el aumento de la inflamación y el estrés mecánico. La ruptura de la placa ocurre cuando se destruye la capa fibrosa, exponiendo el núcleo lipídico al torrente sanguíneo, lo que puede mejorar la formación de trombos al desencadenar un proceso de coagulación (3).
La aterosclerosis es una enfermedad de progresión lenta, lo que explica por qué la mayoría de los casos permanecen asintomáticos durante décadas. Cuando aparecen los síntomas, generalmente están relacionados con una disminución del flujo sanguíneo. La presentación clínica de la enfermedad aterosclerótica puede ser aguda o crónica y varía sustancialmente según el área vascular involucrada (10).
El crecimiento de la placa de ateroma aumenta el riesgo de obstrucción de los vasos y reduce el flujo sanguíneo en la región afectada. Este fenómeno a nivel de las arterias coronarias causa el Síndrome Coronario Agudo (SCA), que implica la formación de placas ateroscleróticas en las arterias coronarias. Cuando estas placas se rompen, exponen material que activa la coagulación y forma un trombo, bloqueando el flujo sanguíneo. Este trombo puede bloquear completamente la arteria o bloquearla parcialmente. La obstrucción impide que el oxígeno y los nutrientes lleguen al músculo cardíaco afectado, provocando isquemia (10).
El síntoma principal que pone en marcha la cascada diagnóstica y terapéutica es la aparición de dolor torácico (angina de pecho), pero la clasificación de los pacientes se basa primordialmente en el electrocardiograma (ECG). El interrogatorio sigue siendo el método de examen más adecuado para reconocer la isquemia miocárdica, el dolor isquémico cardiaco o angina de pecho se percibe sobre la zona retroesternal; “zona de la corbata”, es de carácter constrictivo, con sensación de opresión (aplastamiento o atenazamiento); rara vez transfictivo (sensación de ser atravesado hacia la espalda o los hombros), con una irradiación que se propaga al borde cubital del brazo, antebrazo y la mano (anular; ,meñique) izquierdo (10).
Si la obstrucción es completa o casi completa, puede desencadenar IAM. El IAM es la lesión isquémica del músculo cardíaco, es decir, el momento en el que se produce la muerte de las células del miocardio provocada por la isquemia. Durante el infarto, los miocitos mueren y luego comienza la inflamación, seguida de la eliminación de los restos necróticos y su reparación, provocando una cicatriz en la región (10).
En estúdios histologicos de la placa de ateroma en arterias coronarias de falecidos, dentro de las características demográficas y clínicas, se puede observar que predominar el sexo masculino (81,0%), la edad mayor de 50 años (85,7%) y el color blanco de la piel (66,7%). El hábito de fumar fue el factor de riesgo aterogénico más frecuentemente encontrado (66,7%), las 3/4 partes de los fallecidos tenían un infarto miocárdico previo y solo uno de cada 5 pacientes tenía una fracción de eyección del ventrículo izquierdo normal. Todos tenían más afectada la descendente anterior, el 52,4% tenía enfermedad de três vasos y al mismo porcentaje se le injertaron dos hemoductos. Como era de esperar en pacientes fallecidos, predominaron las placas graves, que representaron el 77,8% de las 149 lesiones ateroscleróticas encontradas en todas las arterias coronarias estudiadas (11).
La placa grave es la continuidad biológica evolutiva de la progresión de la placa fibrosa. Se conoce la incidencia que tienen los factores de riesgo en la progresión y gravedad del proceso aterosclerótico, por lo cual consideramos que la coexistencia de varios de ellos en los individuos de la muestra estudiada determinó el predominio de la lesión aterosclerótica avanzada y la baja presentación de la inicial: la estría adiposa (11).
Otras posibles complicaciones surgen por el desprendimiento del trombo de la pared arterial, lo que produce un coágulo también conocido como émbolo que circulará por el sistema cardiovascular. El émbolo acaba alojándose en las arterias distales, dando lugar a diversas complicaciones como enfermedad isquémica local o disfunción a nivel del órgano afectado (10).
Se pueden utilizar diferentes métodos para diagnosticar la ateroesclerosis y sus complicaciones, como la ecografía Doppler que puede mostrar qué tan líquida es la sangre en las arterias; un ecocardiograma también puede mostrar el flujo sanguíneo; una tomografía computarizada puede mostrar un estrechamiento de las arterias; y una angiografía, que utiliza tintes y rayos X, muestra una imagen de las arterias; el electrocardiograma que es la herramienta diagnóstica de primera línea en la evaluación de pacientes con sospecha de SCA (12).
Según las directrices actuales de la Sociedad Europea de Cardiología (SEC), se puede proponer el siguiente esquema para el tratamiento y prevención de la EA y sus complicaciones: evaluar el riesgo CV general del individuo; determinar los objetivos de la terapia según el riesgo presente; involucrar al paciente en las decisiones sobre la gestión del riesgo CV y elegir un régimen de estatinas y, cuando sea necesario, terapias adicionales (ezetimiba, inhibidores de PCSK9) que puedan cumplir los objetivos de la terapia (porcentaje y valor absoluto) (3).
Como consecuencia, las intervenciones efectivas para detener las complicaciones y la respuesta inflamatoria ocurren mediante la prevención de complicaciones primarias y secundarias (mediante una terapia hipolipemiante), la placa de ateroma puede estabilizarse y el flujo sanguíneo se mantendrá (10).
La prevención primaria de la arterosclerosis juega un papel crucial en la reducción de su incidencia. Esto implica adoptar cambios en el estilo de vida, como ejercicio físico regular, una dieta equilibrada y dejar de fumar. Además, el control estricto de los factores de riesgo, como la presión arterial alta, los niveles elevados de glucosa en sangre y los niveles anormales de lípidos, es esencial para prevenir el desarrollo de complicaciones en individuos de alto riesgo. La educación y la conciencia pública también son componentes esenciales de la prevención primaria, cuyo objetivo es promover hábitos saludables e identificar los factores de riesgo tempranamente. Los estudios han demostrado la eficacia de la prevención primaria para reducir la incidencia de EAC, destacando la importancia de las intervenciones tempranas y los enfoques holísticos en el manejo de factores de riesgo cardiovasculares (12).
Por otro lado, la prevención secundaria tiene como objetivo reducir el riesgo de eventos cardiovasculares recurrentes en pacientes que ya tienen ECV establecida. Esto incluye tratamiento farmacológico. Se sabe que ha sido de importancia el uso de fármacos para la regresión de la placa aterosclerótica y, a su vez, destacan las estatinas, que se dice que son fármacos que actúan inhibiendo la síntesis hepática de LDL-colesterol-3-hidroxi-3-metilglutaril-CoenzimaA reductasa (HMG-CoA-reductasa), que influyen en la biosíntesis del colesterol. Se sabe que la reducción de los niveles de colesterol intrahepático desencadena un aumento en la reiteración de los receptores de LDL en los hepatocitos, pudiendo reducir los niveles de colesterol LDL y triglicéridos, elevando los niveles de colesterol HDL (1,12,13).
Las estatinas se consideran los únicos agentes farmacológicos que han demostrado de manera realista efectos antiateroscleróticos que se pueden dividir en dos grupos, a saber: 1) relacionados con la reducción de los niveles de colesterol LDL; 2) efectos pleiotrópicos, aquellos que son independientes de la reducción del colesterol, como efectos antiinflamatorios, antidiabéticos, mejoría de la enfermedad de Alzheimer, mejoría de la disfunción endotelial, antioxidantes, entre otros. La disminución de los niveles de lípidos séricos atribuible al uso de estatinas genera una estabilización significativa de la placa aterosclerótica, pero los efectos pleiotrópicos han sido de gran valor, ya que demuestran: mejora de la función endotelial, disminución del estrés oxidativo y de la inflamación, aumento de la estabilización de la placa, inhibición de la respuesta trombogénica y promoción de la regresión de la placa (1,13).
Cabe mencionar los diferentes tipos de estatinas disponibles, destacando el principal factor diferenciador que es la capacidad de reducir los niveles de colesterol LDL. Actualmente las ideales son Atorvastatina y Rosuvastatina. Clasificando los tipos de estatinas según su intensidad alta (reducción >50% del c-LDL), intensidad moderada (reducción del c-LDL del 30-50%) y baja intensidad (<30% de reducción de c-LDL), respectivamente: Atorvastatina 4080 mg y Rosuvastatina 20-40 mg, pertenecientes a la primera clasificación; Atorvastatina 1020 mg, Rosuvastatina 5-10 mg, Simvastatina 20-40 mg, Pravastatina 20-80 mg, Lovastatina 40 mg, Fluvastatina 40 mg y Pitavastatina 2-4 mg, pertenecientes a la segunda clasificación; y, no menos importante, Simvastatina 10 mg, Pravastatina 10-20 mg; Lovastatina 20 mg, Fluvastatina 20-40 mg y Pitavastatina 1 mg, pertenecientes a la tercera clasificación (1).
Esta clase de fármacos generalmente se tolera bien, siendo la miopatía el efecto adverso clínicamente más relevante. Aunque aproximadamente entre el 5% y el 10% de los pacientes que reciben tratamiento con estatinas reportan mialgia, la mayoría de los casos no se deben a las estatinas. El riesgo de miopatía se puede minimizar evitando las interacciones medicamentosas. La rabdomiólisis es un efecto secundario extremadamente raro. Otros efectos para considerar se producen a nivel de la homeostasis de la glucosa, siendo posible un aumento de los niveles de glucosa en sangre y de HbA1c en la fase inicial del tratamiento. Estos efectos dependen de la dosis y están asociados con un posible ligero aumento de peso. Aun así, el beneficio terapéutico de las estatinas supera los riesgos para la mayoría de los pacientes. Teniendo en cuenta que las estatinas son medicamentos de larga duración, se debe prestar especial atención a posibles interacciones farmacológicas (3).
Un factor importante para destacar es la interacción farmacológica, y el subtipo de estatina que presenta menor riesgo, destacando así la pravastatina, ya que los principales metabolitos se obtienen mediante degradación química en el estómago y no a través del metabolismo hepático dependiente del citocromo P450 (1).
Siendo así, un enfoque multidisciplinario para la prevención y el tratamiento de las ECV es esencial para brindar atención integral y personalizada a los pacientes. La colaboración entre profesionales sanitarios de diferentes especialidades, incluidos cardiólogos, médicos generales, enfermeras, nutricionistas y fisioterapeutas, permite una evaluación completa de los factores de riesgo, la individualización del plan de tratamiento y el apoyo continuo al paciente durante todo el curso de la enfermedad. A pesar de los avances significativos en la prevención y el tratamiento de la EA, persisten desafíos en la implementación efectiva de estrategias de prevención primaria y secundaria. Barreras como el acceso limitado a la atención médica, las disparidades socioeconómicas y la falta de adherencia de los pacientes pueden afectar negativamente los resultados clínicos y la eficacia de las intervenciones preventivas (12).
Además, es crucial promover políticas de salud pública que fomenten la prevención primaria y secundaria de la EA, incluida la implementación de programas de detección temprana, el acceso equitativo a los servicios de salud y el apoyo financiero para intervenciones preventivas. La participación de múltiples sectores de la sociedad, incluidos gobiernos, organizaciones no gubernamentales, profesionales de la salud y la comunidad en general, es esencial para abordar los complejos desafíos asociados con la EA y promover la salud cardiovascular a escala global (12).
4 RESULTADOS Y DISCUSION
Durante años, las percepciones sobre las enfermedades cardiovasculares han sido idealizadas por el grado de estenosis vascular, que se relaciona con la presencia de lesiones cardiovasculares de alto riesgo y también con la caída de los niveles de colesterol, lo que reduce el tamaño y, en consecuencia, aumenta la luz, mejorando la circulación. Hoy en día, cada vez hay más evidencia sobre la acción de las estatinas sobre la placa aterosclerótica, que es integral y no se limita a reducir el volumen de colesterol en la placa, sino a través de la reducción de los niveles de colesterol circulante, sino que implica la estabilización de la placa, y en consecuencia, su regresión (14).
En especto a los efectos pleiotrópicos de las estatinas destaca la actividad antiinflamatoria y la mejora de la función endotelial, además de la disminución de la actividad colagenolítica y del potencial trombótico. Sin embargo, el papel que demuestran estos efectos, independientemente de la reducción de los niveles de lípidos, aún no está del todo claro. Ante esto, es plausible afirmar que hoy en día las estatinas son consideradas los únicos agentes farmacológicos que han demostrado verdaderos efectos antiateroscleróticos. La terapia con estatinas, en dosis altas y por un período prolongado, puede establecer la regresión de la placa de ateroma, ya que la disminución de volumen ocurrió junto con la reducción de los niveles de lípidos (14).
Según Silva y Vieira (15), el uso de estatinas proporciona una estabilización de la placa aterosclerótica, provocando una reducción de su tamaño, además de una reducción del riesgo de rotura. Además, el uso de estatinas tiene como objetivo la formación de calcificaciones en la placa de aterosclerosis, independientemente de la dosis utilizada, comprobando el tiempo y el grado de calcificación. Según Valada (16), el tratamiento con estatinas aumenta el grado de calcificación en la placa aterosclerótica, reduciendo así el tamaño del núcleo lipídico, generando inhibición de la progresión de componentes considerados vulnerables en la placa, predisponiendo un estímulo a la transición de la placa aterosclerótica vulnerable a una más estable, especialmente cuando se utilizan estatinas en dosis altas para el tratamiento (15,16).
Un recurso conocido como Tomografía de Coherencia Óptica (OCT) muestra que la terapia con estatinas en dosis consideradas altas se asocia con un aumento en el espesor de la capa fibrosa de la placa ateroscleótica, lo que puede correlacionarse con una reducción en el número de macrófagos que se infiltran en la pared arterial, la oxidación de partículas de lipoproteínas, shPCR, el nivel sérico de colesterol LDL y también metaloproteinasa-9, lo que demuestra una marcada disminución en el grado de inflamación en la región vascular donde se establece la placa aterosclerótica (17).
Recientemente se ha propuesto la resonancia magnética de alta resolución para evaluar la vulnerabilidad de la placa aterosclerótica. La resonancia magnética puede ilustrar en detalle los componentes de la placa aterosclerótica, la pared arterial y los tejidos blandos circundantes. En particular, puede cuantificar adecuadamente las características clave de la placa vulnerable, la ulceración, el núcleo necrótico rico en lípidos (LRNC), la calcificación, la neovascularización intraplaca (IPN) y la inflamación. Una revisión sistemática reciente incluyó siete estudios prospectivos (un total de 36,1 pacientes con enfermedad aterosclerótica carotídea) y examinó los cambios en los volúmenes del LRNC y los volúmenes de la luz después del tratamiento con estatinas durante al menos un año. La gran mayoría de los estudios prospectivos informaron una reducción significativa en los volúmenes de LRNC sin ningún cambio significativo en la carga de placa. La regresión de los lípidos centrales puede ser un mecanismo representativo de la estabilización de la placa inducida por estatinas. Por lo tanto, este estudio que utilizó imágenes por resonancia magnética confirmó la reducción inducida por las estatinas en el porcentaje y el volumen de lípidos dentro de la placa carotídea después de una terapia intensiva con estatinas (18,19).
En el estudio de Stasinopoulou et al. (19), se evaluó el efecto del tratamiento con atorvastatina sobre la progresión de la lesión aterosclerótica midiendo la estenosis luminal a nivel de la válvula aórtica en ratones sometidos a un modelo animal aterosclerótico (ApoE −/−). Los cambios en la estabilidad de la placa se evaluaron midiendo las concentraciones de colágeno y tejido conectivo dentro de las placas ateroscleróticas. El grado de estenosis luminal fue significativamente menor en el grupo tratado con atorvastatina (ATF) a largo plazo (13,90 ± 1,08%) en comparación con su grupo de control (CO-12W) (21,95% ± 2,40% en CO-12W, P <0,001). En particular, la interrupción a largo plazo de la atorvastatina (6 semanas) casi revirtió este efecto beneficioso de la atorvastatina (ATW-6W vs ATL, P = 0,051).
Los autores concluyeron que la administración ininterrumpida de atorvastatina atenuó la progresión de la aterosclerosis y aumentó la estabilidad de la placa al suprimir el potencial inflamatorio dentro de las lesiones ateroscleróticas aórticas de ratones ApoE -/- hipercolesterolémicos. Cuando se interrumpió repentinamente el tratamiento con atorvastatina, su efecto ateroprotector pareció anularse rápidamente, lo que provocó una desestabilización aguda de la placa, independientemente de los cambios en los niveles de colesterol. La liberación aguda de mediadores inflamatorios dentro de las placas ateroscleróticas después de la interrupción de las estatinas puede explicar mecánicamente los cambios exagerados y desfavorables en la estabilidad de la placa a corto plazo. Después de la respuesta de rebote inicial, estos efectos se suavizaron ligeramente a partir de entonces, lo que eventualmente condujo a una desestabilización sostenida de la placa a largo plazo. Los hallazgos son de importancia clínica y describen el riesgo de eventos adversos en pacientes ateroscleróticos que no cumplen con el tratamiento continuo con estatinas (19).
Un ensayo randomizado reciente que estudió el efecto de la rosuvastatina en comparación con la atorvastatina sobre la estabilización de la placa coronaria concluyó que la terapia con rosuvastatina resultó en una mayor estabilización de la placa según lo evaluado por el espesor de la capa fibrosa, la prevalencia del fibroateroma de capa delgada, los macrófagos y la densidad de los microvasos. Una de las razones plausibles de esto es que la rosuvastatina redujo la actividad de las metaloproteinasas de la matriz derivadas del endotelio y los monocitos. Se postula que esto reduce el adelgazamiento de la capa fibrosa y eventualmente estabiliza las placas coronarias (20).
Otro estudio reciente también mostró una activación reducida de los monocitos con rosuvastatina, que puede desempeñar un papel importante en la reducción de las placas ateroscleróticas coronarias. Este estudio también demostró una reducción del volumen total de ateroma y del volumen total de ateroma normalizado. Corroborando con un estudio que demostró que la rosuvastatina, en comparación con la atorvastatina, normalizó el colesterol de membrana, la proteína del factor tisular y la actividad procoagulante dependiente del factor tisular en pacientes hipercolesterolémicos, lo que puede ser otra razón plausible para mejores resultados con rosuvastatina (21,22).
Por tanto, la terapia con estatinas provoca una mayor estabilización de la placa aterosclerótica mediante cambios inducidos en su composición. Cabe destacar los efectos que producen las estatinas sobre los niveles séricos de colesterol HDL, que son inversamente proporcionales al riesgo de eventos cardiovasculares propiamente dichos, estrechamente ligados al proceso aterosclerótico (1).
Según datos de Barros (5), el efecto protector de niveles moderados/altos de colesterol HDL se correlaciona con propiedades antioxidantes, antitrombóticas/fibrinolíticas, antiinflamatorias y, sobre todo, promueve la función endotelial y la salida de colesterol con los macrófagos de tejidos periféricos al hígado.
Otro estudio, evidenciado por Candido et al. (22), predispone entre la asociación de los niveles séricos de colesterol HDL y el espesor de la capa fibrosa, pudiendo así considerar el colesterol HDL como una diana terapéutica que proporciona estabilización de la placa. Finalmente, el tratamiento con estatinas aumenta el grado de calcificación de la placa aterosclerótica, reduciendo el diámetro del núcleo lipídico, inhibiendo así la progresión de los componentes vulnerables de la placa, además de estimular la transición de una placa aterosclerótica vulnerable a una más estable, especialmente cuando se utilizan dosis altas de estatinas.
5 CONSIDERACIONES FINALES
Al analizar diferentes estudios, efectivamente tenemos información sobre el uso de medicamentos y la influencia positiva del proceso aterosclerótico, destacando los factores de riesgo que afectan la placa. Además, el tipo de fármaco que tiene el potencial de estabilizar la placa aterosclerótica mediante cambios inducidos en su composición son las estatinas.
Por tanto, está claro que las estatinas favorecen la regresión y estabilización de la placa de ateroma. Del momento en que se infiere el uso de terapia que involucra el uso de estatinas en dosis altas, se asocia con un aumento significativo en el espesor de la capa fibrosa de la placa aterosclerótica, teniendo así una correlación entre el aumento de esta y la reducción del número de macrófagos que se establecen en la pared arterial, en el nivel sérico de colesterol LDL y en la oxidación de las partículas de lipoproteínas.
Sin embargo, está claro que las prácticas no farmacológicas actúan de manera muy significativa en la vida de las personas que padecen enfermedad coronaria, destacándose también la práctica de actividad física y una dieta regulada. Se dice que estos son factores predisponentes beneficiosos para la vida del individuo independientemente de factores como: edad, sexo, raza/etnia. Al analizar esta revisión se puede confirmar el objetivo del presente trabajo, en el que los componentes contenidos en el medicamento mencionado, aunque existan efectos adversos, predisponen positivamente a la situación comentada.
REFERÊNCIAS
1. Ferreira G, Ferreira M. Influência do uso de fármacos na regressão da placa aterosclerótica. Revista Eletrônica Acervo Saúde. 2023 May 18;23(5):e12682–2. Disponible en: https://ubibliorum.ubi.pt/bitstream/10400.6/8795/1/6899_14700.pdf
2. Reis SC. Uma revisão bibliográfica sobre aterosclerose | Revista Eletrônica Acervo Científico. acervomaiscombr [Internet]. 2019 Feb 4;3. Disponible en: https://acervomais.com.br/index.php/cientifico/article/view/444
3. Paquito BNC. Doença Aterosclerótica – Prevenção e terapêutica [disertación]. Lisboa: Faculdade de Farmácia, Universidade de Lisboa. 2023. 71p.
4. Miranda ALA, Ramos FR de O, Cavalcante LS. A utilização de estatinas na prevenção primária de doenças cardiovasculares: revisão bibliográfica. Brazilian Journal of Health Review. 2024 May 2;7(3):e69375. Disponible en: https://ojs.brazilianjournals.com.br/ojs/index.php/BJHR/article/view/69375#:~:text=Em%20conclus%C3%A3o%2C%20as%20estatinas%20s%C3%A3o,avaliar%20cuidadosamente%20o%20tratamento%20individualizado.
5. Barros MS. Relação do Colesterol e Estatinas com o Síndrome Coronário Agudo: uma revisão [disertación]. Lisboa: Instituto de Ciências Biomédicas Abel Salazar, Universidade do Porto; 2019. 34p
6. Abdallah A, Souza LFA de, Colacite J. O uso de estatinas no tratamento de dislipidemia: Revisão bibliográfica. Research, Society and Development [Internet]. 2023 Oct 29;12(11):e82121143679–e82121143679. Disponible en: https://rsdjournal.org/index.php/rsd/article/view/43679/35153
7. Gonçalves JR. Como escrever um artigo de revisão de literatura | Revista JRG de Estudos Acadêmicos. [Internet]. 2022 Abr 13 [citado 2024 Abr 23]; Disponible en: https://www.revistajrg.com/index.php/jrg/article/view/122/201
8. González G, Fernández F, Ávalos D, Ortellado J, Adorno M, Galeano J, et al. Registro Nacional de Síndrome Coronario Agudo en Paraguay (RENASCA-PY). Archivos de Cardiología de México. 2022 Mar 16;92(2). Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9005167/
9. Santos VP dos, Pozzan G, Castelli Júnior V, Caffaro RA. Arteriosclerose, aterosclerose, arteriolosclerose e esclerose calcificante da média de Monckeberg: qual a diferença? Jornal Vascular Brasileiro [Internet]. 2021;20. Disponible en: https://www.scielo.br/j/jvb/a/Fw3v7WMNjm5mDJdWRd6rJLH/?lang=pt&format=pdf
10. Seidman MA, Mitchell RN, Stone JR. Pathophysiology of Atherosclerosis. Cellular and Molecular Pathobiology of Cardiovascular Disease; 2020; 55, 221 237.
11. Pérez Sorí Y, Herrera Moya VA, Puig Reyes I, Moreno-Martínez FL, Bermúdez Alemán R, Rodríguez Millares T, et al. Histología de la placa de ateroma en arterias coronarias de fallecidos después de una revascularización miocárdica quirúrgica. Clínica e Investigación en Arteriosclerosis. 2019 Mar;31(2):63–72.
12. Benfica I, Silva, Melina Rodrigues Rocha, Flavia A, Marina. Importância da prevenção primária e secundária na doença arterial coronariana. Brazilian Journal of Health Review. 2024 Apr 9;7(2):e68756–6. Disponible en: https://ojs.brazilianjournals.com.br/ojs/index.php/BJHR/article/view/68756
13. Sainz JI, Mercè Brunet Serra. Influencia de la farmacogenética en la diversidad de respuesta a las estatinas asociada a las reacciones… [Internet]. ResearchGate. Walter de Gruyter; 2023 [citado 2024 Oct 2]. Disponible en: https://www.researchgate.net/publication/374493759_Influencia_de_la_farmacogenetica_en_la_diversidad_de_respuesta_a_las_estatinas_asociada_a_las_reacciones_adversas
14. Valente LJM. Influência do uso de estatinas sobre a regressão/estabilização da placa de ateroma. Tese de Doutorado. Universidade da Beira Interior, Covilhã, Portugal, 2019.
15. Silva S. Uso de estatinas e suplementação com coenzima Q10: uma revisão narrativa. Monografia do curso de Farmácia, Centro Universitário AGES, Paripiranga – Brasil, 2021.
16. Valada IRG. Aterosclerose: a hipercolesterolémia e a importância dos microRNAs. Tese de Doutorado. Universidade de Coimbra, Coimbra, Portugal, 2019.
17. Nikolaos PE Kadoglou, Khattab E, Nikolaos Velidakis, Nikolaos Patsourakos, Vaia Lambadiari. A new approach of statin therapy in carotid atherosclerosis: Targeting indices of plaque vulnerability on the top of lipid-lowering. A narrative review. Kardiologia Polska [Internet]. 2022 Sep [citado 2024 Oct 2];80(9):880–90. Disponible en: https://journals.viamedica.pl/polish_heart_journal/article/view/90477
18. Rasmussen P, Yandrapalli S, Aronow W. Statin therapy for primary cardiovascular prevention in older adults over 75 years. Kardiologia Polska. 2021. Disponible en: https://www.tctmd.com/news/statins-effective-primary-prevention-old-and-veryold#:~:text=The%20incidence%20of%20CVD%20events%20was%205.0%25%20lower%20in%20statin,12.5%25%20lower%20in%20statin%20users.
19. Stasinopoulou M, Nikolaos P.E. Kadoglou, Christodoulou E, Efthymios Paronis, Nikolaos Kostomitsopoulos, Valsami G, et al. Statins’ Withdrawal Induces Atherosclerotic Plaque Destabilization in Animal Model—A “Rebound” Stimulation of Inflammation. Journal of Cardiovascular Pharmacology and Therapeutics. 2019 Mar 24;24(4):377–86.
20. Kumar A, Shariff M, Doshi R. Impact of rosuvastatin versus atorvastatin on coronary atherosclerotic plaque volume – a systematic review and meta-analysis with trial sequential analysis of randomized control trials. European Journal of Preventive Cardiology. 2020 Dec 1;27(19):2138–41.
21. Sarraju A, Nissen SE. Atherosclerotic plaque stabilization and regression: a review of clinical evidence. Nature Reviews Cardiology [Internet]. 2024 Jan 4;1–11. Disponible en: https://www.nature.com/articles/s41569-023-00979-8?fromPaywallRec=false
22. Barros MS. Relação do colesterol e estatinas com síndrome coronário agudo: uma revisão. Mestrado em Medicina. Instituto de Ciências Biomédicas Abel Salazar, Universidade de Porto, Porto – Portugal, 2019.
23. Caroline Bezerra Candido, Neto S, Camili Vitória Lucian, Clara, Corredeira F, Gabrielle J, et al. Repercussões da dislipidemia na população infanto-juvenil: uma revisão de literatura. Recima21 – Revista Científica Multidisciplinar – ISSN 2675-6218 [Internet]. 2022 Ago 22 [citado 2024 Oct 2];3(8):e381741–1. Disponible en: https://recima21.com.br/index.php/recima21/article/view/1741
1 Discente do Curso Superior de Medicina da Universidade Brasil (UB) Campus Fernandópolis e-mail: ouvidoria@universidadebrasil.edu.br
2 Discente do Curso Superior de Medicina da Universidad Central del Paraguay (UCP) Campus Ciudad del Este e-mail: institucional@central.edu.py
3 Discente do Curso Superior de Medicina da Universidad Privada del Este (UPE) Campus Ciudad del Este email: info@upecde.edu.py

