COMPUTATIONAL STUDY OF THE ANTIFUNGAL ACTIVITY OF ESSENTIAL OILS AGAINST OROPHARYNGEAL CANDIDIASIS
REGISTRO DOI: 10.69849/revistaft/th10249231707
Thyago Silva Martins1
Lorrany Kalliny Cardoso Queiroz2
Gunar Vingre da Silva Mota3
Fabio Luiz Paranhos Costa4
Rômulo Gomes de Oliveira Cabral5
Sarah Mossolini Lewe6
Camila Cristina Daluia Calegari7
Leandro Francisco Ribeiro8
Dayane Sousa Morais Borges9
Mayara Carvalho Borges10
Giovana Camila Paleari Prado¹¹
Resumo: Neste estudo de ancoragem molecular (usou-se o programa Autodocking Vina) foi investigado o potencial fungicida dos óleos essenciais de: Ocimum basilicum, Cymnopogon martinii, Thymus vulgaris e Cinnamomum cassia. Assim, selecionou-se metabólitos secundários majoritários (carvacrol, aldeído cinâmico, eucaliptol, geraniol, acetato de geraniol, linalool e p-Cimeno, Timol) foram testados como ligantes contra a proteína SAP2 (esta proteína de funciona como uma enzima hidrolítica, apresentando ampla especificidade de substrato, e é expressa abundantemente no cultivo de C. albicans)
Palavras-chave:candidíase orofaríngea; ancoragem molecular; SAP2.
Abstract: In this molecular docking study (the Autodocking Vina program was used) the fungicidal potential of the essential oils of: Ocimum basilicum, Cymnopogon martinii, Thymus vulgaris and Cinnamomum cassia was investigated. Thus, major secondary metabolites (carvacrol, cinnamic aldehyde, elcaliptol, geraniol, geraniol acetate,linalool and p-cymene, thymol) were tested as ligands against the SAP2 protein (this protein works as a hydrolytic enzyme, presenting a wide substrate specificity, and is abundantly expressed in C. albicans culture.
Keywords: oropharyngeal candidiasis; molecular anchoring; SAP2.
INTRODUÇÃO
As infecções fúngicas causadas pela Candida albicans (C.A) podem desencadear manifestações clínicas em diversas partes do corpo, tais como as membranas mucosas, a pele, e em casos específicos até mesmo orgãos internos2. A candidíase oral, por sua vez, pode gerar grandes danos e imenso desconforto na cavidade oral, e se manifesta geralmente em pacientes com um sistema imunológico enfraquecido, uso de antibióticos, próteses dentárias desadaptadas e uma higiene oral deficiente, fatores estes que podem levar à multiplicação descontrolada do fungo1.
A candidíase orofaríngea, é muito prevalente em bebês, idosos que usam próteses totais e pacientes em tratamento com antibacterianos, essa afecção, pode se ter manifestações clínicas mais severas em pacientes com HIV/AIDS, haja visto risco de proliferação excessiva de C.A para outros tecidos do corpo3.
Com base nisso, tem se buscado intensamente medicamentos alternativos aos antifúngicos já existentes, na tentativa de contornar os casos de resistência e de se otimizar os resultados da terapêutica, por meio de fármacos que possuam menos efeitos colaterais para o tratamento da candidíase orofaríngea2. Nesse contexto, este estudo se propôs a pesquisar o potencial fungicida dos óleos essenciais de Ocimum basilicum, Cymnopogon martinii, Thymus vulgaris e Cinnamomum cassia, compostos fitoterápicos que se mostram muito promissores, através de técnicas de ancoragem molecular, por meio do programa Autodocking Vina. Foram selecionados metabólitos secundários majoritários desses óleos essenciais, como carvacrol, aldeído cinâmico, eucaliptol, geraniol, linalool, timol e p-Cimeno e testamos como ligantes contra a proteína SAP2, que desempenha um papel importante no metabolismo do fungo e é amplamente expressa em culturas de Cândida albicans.
Neste estudo, as estruturas moleculares dos metabólitos secundários e da proteína SAP2 foram preparadas como ligantes, e foram realizados cálculos de propriedades ADMET (absorção, distribuição, metabolismo, excreção e toxicidade) e eficiência de ligação utilizando o software Discovery Studio. Os resultados foram comparados com os obtidos para o fármaco fluconazol, amplamente utilizado no tratamento de infecções fúngicas, e para o inibidor pepstatina A.
O método de ancoragem molecular permite um melhor entendimento das interações proteína-ligante, oferecendo insights valiosos sobre os mecanismos moleculares subjacentes à inibição da proteína SAP2. Essas informações são muito importantes para possibilitar o desenvolvimento de compostos cada vez mais potentes e seletivos, a fim de se obter um tratamento mais eficaz contra a candidíase orofaríngea 1 .
METODOLOGIA
Foram utilizados para a obtenção da identificação da proteína, bem como suas propriedades o banco de dados virtuais Protein Data Bank, no qual foi possível verificar as respectivas características cristalográficas e informações pertinentes ao ligante natural como referência para o preparo dos compostos. Foi utilizado também o PubChem para a pesquisa de possíveis ligantes e identificação de suas características físico-químicas. Foram realizadas simulações computacionais utilizando o software AutoDock Vina, a fim de se obter por meio de predições in silico o melhor encaixe do complexo proteína-ligante caracterizado pelas ligações com a menor energia de ligação possível para a efetividade da ligação, podendo por meio de seu algoritmo determinar os compostos mais promissores e capazes de inibir a atuação da SAP 2. Aplicação do Softwares Open Babel para conversão de arquivos e de visualização gráfica Discovery Studio. O Open Babel é um software contendo ferramentas de arquivos de vários formatos e que realiza a conversão de diversos formatos a fim de atender as mais diversas especificidades dos programas empregados na química computacional. O Discovery Studio foi o software de eleição para a obtenção de imagens pois o principal propósito é propiciar uma melhor visualização das interações químicas a nível molecular entre estruturas protéicas e possíveis fármacos, sendo uma ferramenta útil na demonstração gráfica do encaixe molecular, conformação de macromoléculas, modelagem de fármacos e simulações de otimização. Já as informações pertinentes às características farmacológicas de absorção, distribuição, metabolismo, excreção e toxicidade foram obtidas através SwissAdme.
RESULTADOS E DISCUSSÃO
Com o intuito de avaliar a eficácia de ligação, é aplicada uma normalização da afinidade em relação ao número de átomos na molécula, excluindo átomos de hidrogênio. O cálculo envolve a divisão da energia de ligação dos compostos (ΔG) pelo número de átomos não relacionados ao hidrogênio no ligante (n ou NAH). Para determinar a qualidade dos ligantes, são realizados ajustes que se aproximam de 1,0 ou superam esse valor, indicando uma ligação quase ideal, enquanto pontuações de ajuste mais baixas sugerem uma ligação subótima. Geralmente, um ligante com valores de EL ≥ 0,30 kcal/mol/átomo é considerado promissor, com um valor mínimo de 0,26 como referência5.
É fundamental analisar a energia de interação e os aminoácidos envolvidos nas interações no sítio ativo da SAP2 quando se trata dos fármacos listados na tabela 1, como o fluconazol, a anfotericina B, o cetoconazol, a terbinafina, a flucitosina e a Terbinafina, em comparação com a pepstatina A, o inibidor cocristalizado da SAP2. Além disso, é necessário avaliar produtos naturais para identificar possíveis inibidores da SAP2. O critério a ser considerado deve ser baseado em aspectos energéticos e nos aminoácidos do sítio ativo. Tomando a pepstatina A como referência, que apresenta uma energia de interação de -7,9 kcal/mol e interações de hidrogênio com cinco aminoácidos (ASP 86, THR 222, TYR 225, THR 221, GLY 34), consideramos um ligante “eficaz” aquele com energia de interação superior a -5,0 kcal/mol e compartilhando pelo menos três aminoácidos em comum com os mencionados (ILE 82, ALA 133, ASN 131, SER 36, LEU 216, ILE 305, GLU 193, ASN 301, ILE 123, ILE 119, SER 35, ASP 218, ASP 32, GLY 220, ILE 223, VAL 12, GLN 121, GLU 10, THR 13). Analisando os resultados do docking molecular e da tabela de eficiência de ligação (EL), pode-se destacar alguns constituintes majoritários dos óleos essenciais estudados como potenciais inibidores da SAP2. O carvacrol apresentou uma boa energia de ligação de -5,5 kcal/mol, estabelecendo interações de van der Waals com resíduos do sítio ativo como ASP86, ILE30, SER88 e ILE119. Além disso, obteve um EL de 0,50, superior ao padrão de 0,30, indicando uma relação favorável entre energia de ligação e tamanho molecular. O eucaliptol (elcaliptol) também obteve energia de ligação de -5,5 kcal/mol, interagindo com resíduos como THR221, ASP86, GLY220 e ILE123. Seu EL foi de 0,50, igual ao do carvacrol. O p-cimeno, apesar de ter o mesmo valor de energia de ligação (-5,5 kcal/mol), estabeleceu interações de van der Waals com menos resíduos do que o carvacrol e o eucaliptol. Porém, seu EL foi o maior dentre os compostos testados (0,55), indicando alta eficiência de ligação por átomo não hidrogênio. O timol também apresentou energia de ligação de -5,3 kcal/mol e EL de 0,48, além de interagir com resíduos importantes como ASP86, SER88 e ILE119. Portanto, com base nos critérios energéticos e de eficiência de ligação, o carvacrol, eucaliptol, p-cimeno e timol se destacam como os constituintes com maior potencial inibitório contra a SAP2 dentre os analisados neste estudo. Estes resultados abrem perspectivas para investigação experimental da atividade antifúngica destes compostos.
CONSIDERAÇÕES FINAIS
O carvacrol e o eucaliptol apresentaram energias de ligação de -5,5 kcal/mol, o que é considerado um valor favorável para inibição enzimática. Ambos os compostos também apresentaram EL de 0,50, indicando uma relação favorável entre energia de ligação e tamanho molecular. O p-cimeno apresentou energia de ligação de -5,5 kcal/mol, o mesmo valor do carvacrol e do eucaliptol, mas estabeleceu interações de van der Waals com menos resíduos do que estes. Porém, seu EL foi o maior dentre os compostos testados (0,55), indicando alta eficiência de ligação por átomo não hidrogênio. O timol também apresentou energia de ligação de -5,3 kcal/mol, um valor ligeiramente inferior ao do carvacrol e do eucaliptol, mas ainda considerado favorável para inibição enzimática. O timol também apresentou EL de 0,48, além de interagir com resíduos importantes como ASP86, SER88 e ILE119. Assim, de acordo com o presente estudo, o carvacrol, eucaliptol, p-cimeno e timol são os constituintes majoritários dos óleos essenciais estudados com maior potencial inibitório contra a SAP2. Estes resultados abrem perspectivas para investigação experimental da atividade antifúngica destes compostos. Estudos in vitro e in vivo são necessários para confirmar a atividade inibitória destes compostos contra a SAP2 e avaliar o seu potencial como agentes antifúngicos.
REFERÊNCIA BIBLIOGRÁFICA
1. Lima, I. O. Rev. Bras. Farmg. 2006, 197, 201.
2. Almeida, L. F.Dissertação. UFP, 2011, 89.
3. Wingeter, M. A. Soc. Bras. Rev. 2007, 272, 276.
4. Biovia Discovery Studio – BIOVIA. Dassault Systèmes®
5.Reynolds, C. H.; Tounge, B. A.; Bembenek, S. D. J. Med. Chem. 2008, 51, 2432.

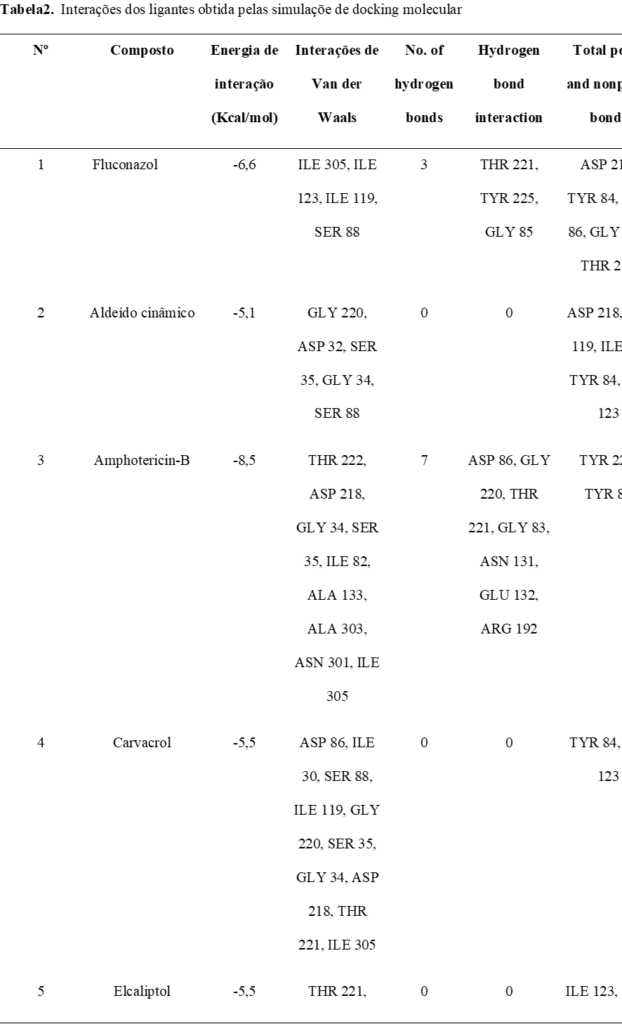
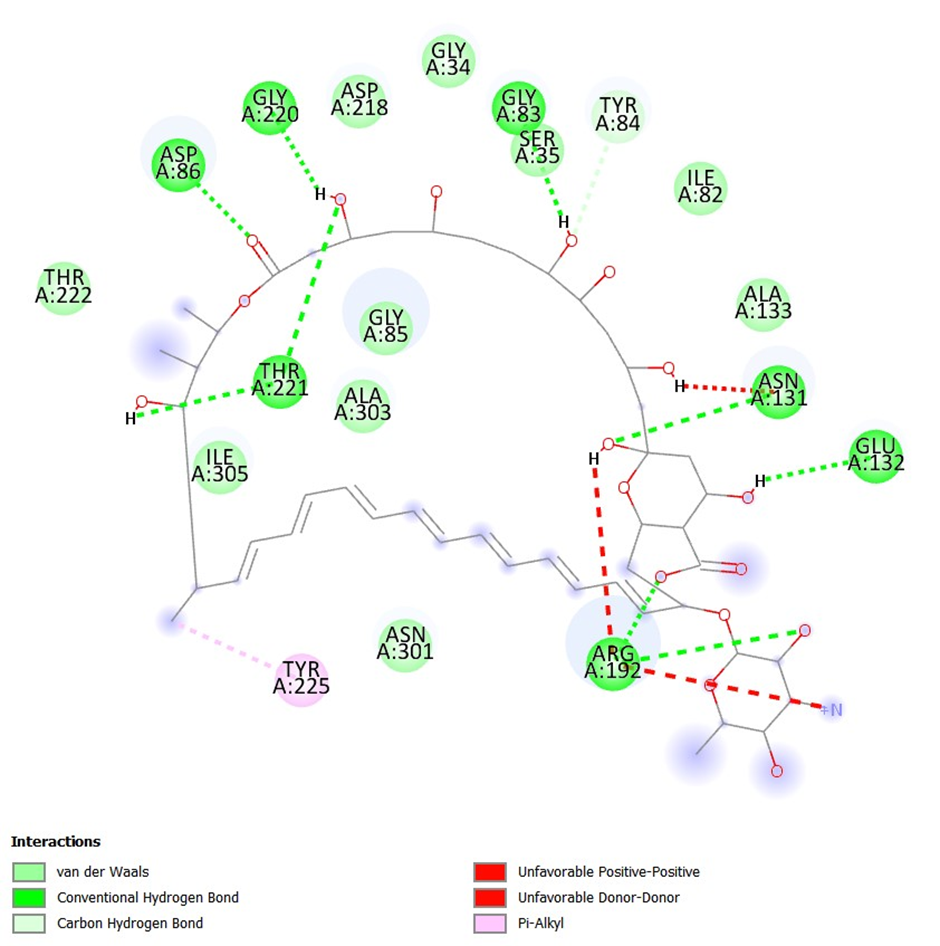
Imagem 1: Interação entre a pepstatina A e a proteina SAP 2
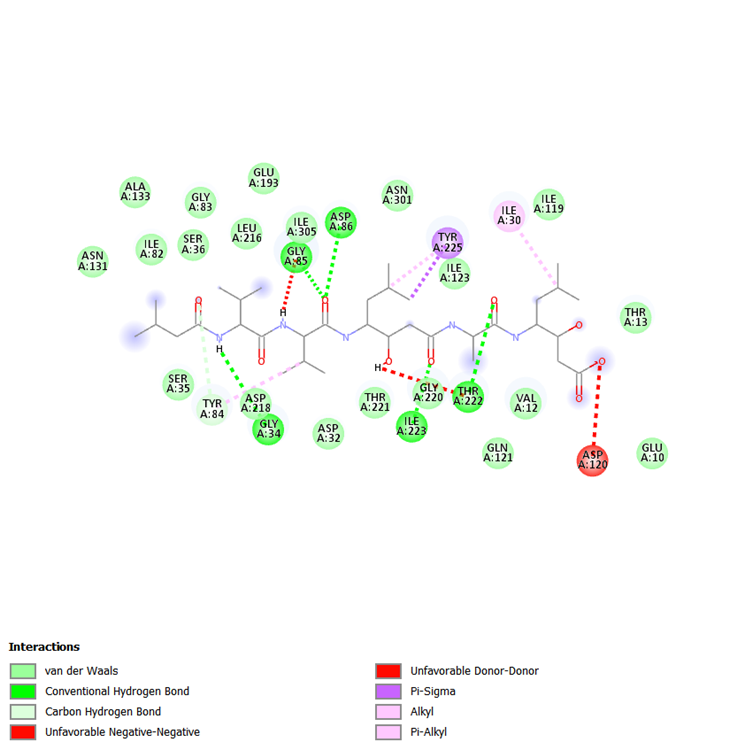
Imagem 2: Interação entre o linalool e a proteina SAP 2
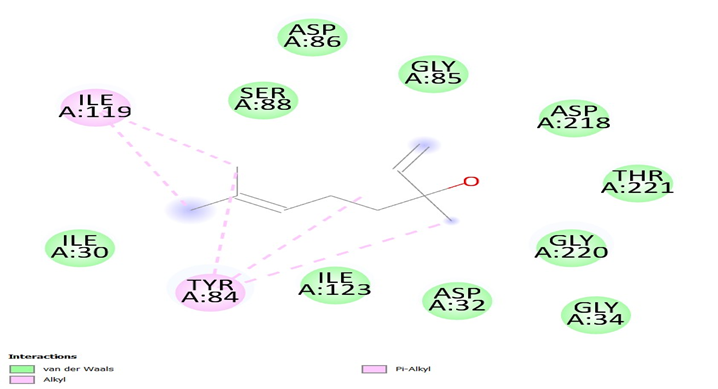
Imagem 3: interação entre o cetoconazol e a proteína SAP2
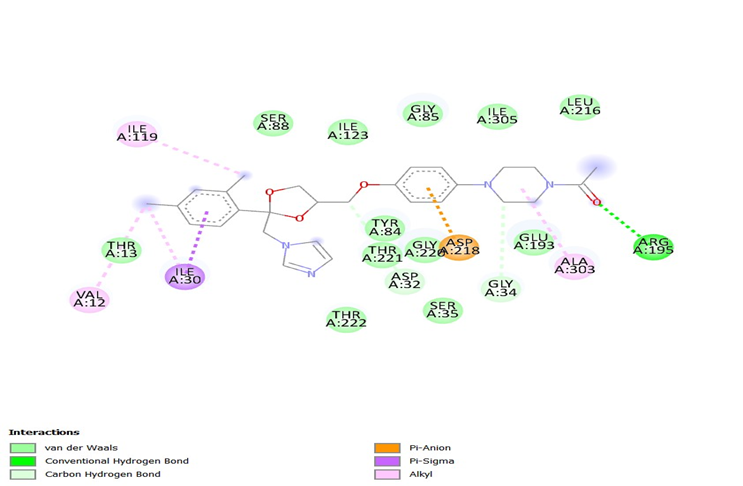
Imagem 4: interação entre a anfotericina B e a proteína SAP2
1Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (62) 993051093 e e-mail: thyagomartins@discente.ufj.edu.br).
2Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (66) 9212-6488 e e-mail: lorranykalliny@discente.ufj.edu.br).
3Afiliações (Docente da Universidade Federal do Pará (UFPA), Telefone: (91) 8325-2703 e e-mail: gunar@ufpa.br).
4Afiliações (Docente da Universidade Federal de Jataí (UFJ), Telefone: (64) 99996-7947 e e-mail: flpcosta@ufj.edu.br).
5Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (62) 993051093 e e-mail: romulogomes@discente.ufj.edu.br).
6Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (64) 993405508 e-mail: sarahlewe@hotmail.com.
7Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (64) 984230663 e-mail: camiladaluia@hotmail.com.
8Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (41) 989040741 e-mail: leandro.ribeiro@discente.ufj.edu.br).
9Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (64) 996715703 e-mail: dayaneborges@discente.ufj.edu.br).
10Afiliações (Discente da Universidade Federal de Jataí (UFJ), Telefone: (64) 996559127 e-mail:mayara.borges@discente.ufj.edu.br
11Afiliação (Docente Faculdade Morgana Potrich), Telefone: (14) 991374533 e-mail: gipaleari@yahoo.com.br
