REGISTRO DOI: 10.5281/zenodo.10929673
Thiago Bento Ribeiro
RESUMO
Introdução: Em dezembro de 2019 uma nova patologia epidêmica aparece no Mercado Atacadista de Frutos do Mar de Wuhan, província de Hubei, com pacientes apresentando pneumonia viral provocada por um agente microbiano desconhecido. Em 11 de março de 2020 a OMS a classifica oficialmente como uma pandemia. Até o momento, mais de 45 milhões de pessoas já foram infectadas e mais de 1 milhão de casos de mortes foram reportados à OMS. O TMO já foi utilizado durante a pandemia do vírus da influenza em 1918-1920 e também foi recomendado por médicos e cientistas contra a gripe aviária H5N1 em 2007. Estudos sugerem que o TMO tem potencial para desempenhar um papel significativo em ajudar a reduzir a morbidade, mortalidade, o tempo de internação e a necessidade de um paciente para a ventilação mecânica.
Objetivo: O presente estudo visa verificar se o uso do TMO quando associado ao tratamento padrão em pacientes hospitalizados com COVID-19, diminui os dias de internação e minimiza os efeitos deletérios funcionais comparando o emprego desse tipo de terapêutica a aplicação apenas do protocolo padrão.
Material e Métodos: Neste estudo multicêntrico (5 unidades de referência de tratamento de COVID-19, um em cada região do Brasil), randomizado e controlado, serão recrutados 406 indivíduos, de ambos os sexos, com idade igual ou superior a 50 anos que tenham sido hospitalizados com diagnóstico médico de COVID-19, confirmado por exame laboratorial e/ou de imagem. Os indivíduos serão randomizados e alocados em 3 grupos: grupo intervenção (GI), estes submetidos ao tratamento manipulativo osteopático em conjunto à terapêutica padrão, grupo controle (GC), estes submetidos à manipulação simulada adjuvante ao tratamento padrão e grupo protocolo padrão (GPP), estes submetidos ao tratamento padrão utilizado na atualidade. A avaliação inicial se dará pelos médicos responsáveis pela triagem de pacientes nas unidades hospitalares, que farão o diagnóstico clínico baseado nos sinais e sintomas dos mesmos e confirmado através de exame laboratorial e/ou de imagem. Farão uma anamnese e exame clínico preliminar, administrando também dois questionários que servirão de follow up para a recuperação sintomática e funcional dos pacientes. Os tratamentos manipulativos serão realizados por 5 osteopatas (um em cada unidade hospitalar) e se iniciarão dentro de 24 horas após admissão, sendo realizados 2 vezes ao dia com intervalo de pelo menos 6 horas entre um atendimento e outro durante aproximadamente 15 minutos. O tratamento osteopático será contínuo até a cessação de tratamento medicamentoso, insuficiência respiratória ou morte. Os dados serão coletados pelas equipes de profissionais de cuidados médicos dos pacientes e repassados ao responsável da pesquisa para análise através do pacote estatístico SPSS 2.0 (Statistical Package for Social Sciences).
Palavras chave: TMO. Tratamento Manipulativo Osteopático. COVID-19. Coronavírus. SARS-CoV-2.
ABSTRACT
Introduction: In December 2019 a new epidemic pathology appeared in the Wholesale Seafood Market in Wuhan, Hubei province, with patients experiencing viral pneumonia caused by an unknown microbial agent. On March 11, 2020, WHO officially classified it as a pandemic. So far, more than 45 million people have been infected and more than 1 million death cases have been reported to WHO. OMT was already used during the influenza virus pandemic in 1918-1920 and was also recommended by doctors and scientists against H5N1 avian influenza in 2007. Studies suggest that OMT has the potential to play a significant role in helping to reduce morbidity, mortality, length of hospitalization and the need for mechanical ventilation.
Objective: The present study aims to verify whether the use of OMT when associated with standard treatment in patients hospitalized with COVID-19, reduces the days of hospitalization and minimizes the harmful functional effects by comparing the use of this type of therapy to the single application of the standard protocol.
Material e Methods: In this multicenter study (5 reference units of COVID-19 treatment, one in each region of Brazil), randomized and controlled, 406 individuals, of both sexes, aged 50 years or over who have been hospitalized with medical diagnosis of COVID-19, confirmed by laboratory and / or imaging exam, will be recruited. The individuals will be randomized and allocated into 3 groups: intervention group (IG), submitted to manipulative osteopathic treatment together with standard therapy, control group (CG), submitted to simulated manipulation adjuvant to standard treatment. and standard protocol group (SPG), submitted to the standard treatment used today. The initial assessment will be made by doctors responsible for screening patients in hospital units, who will make the clinical diagnosis based on their signs and symptoms and confirmed through laboratory and/or imaging tests. They will carry out an anamnesis and preliminary clinical examination, also administering two questionnaires that will serve as a follow up for the symptomatic and functional recovery of patients. The manipulative treatments will be performed by 5 osteopaths (one in each hospital unit) and will start within 24 hours after admission, being performed twice a day with an interval of at least 6 hours between one appointment and another for approximately 15 minutes. Osteopathic treatment will be continuous until drug treatment ceases, respiratory failure or death. The data will be collected by the patients’ teams of medical care professionals and passed on to the professional in charge of the research for analysis through the statistical package SPSS 2.0 (Statistical Package for Social Sciences).
Palavras chave: OMT. Osteopathic Manipulative Treatment. COVID-19. Coronavírus. SARS-CoV-2.
1. INTRODUÇÃO
A COVID-19 é a doença provocada pelo agente etiológico SARS-CoV-2, ou, síndrome respiratória aguda grave coronavírus 2 (Roujian et al., 2020). Em 11 de março de 2020 a OMS a classifica oficialmente como uma pandemia. Até o momento, mais de 64 milhões de pessoas já foram infectadas e mais de 1 milhão e quinhentas mil mortes foram reportados à OMS (WHO, 2020); e os impactos não só sócio econômicos (Nicola et al., 2020) como também no bem estar mental da população (Alradhawi, 2020) foram e ainda continuam sendo devastadores. Sua patogênese ainda é muito duvidosa e controversa , porém uma base de estudos anteriores com a SARS-CoV nos permite traçar um provável curso de eventos clínicos e dividir a COVID-19 em três fases que correspondem a diferentes estágios clínicos da doença (Mason RJ., 2020). A primeira é a fase assintomática nos dias 1-2 da infecção; a segunda fase é a resposta das vias aéreas condutoras superiores que acontece nos dias subsequentes e na terceira fase temos a hipóxia, infiltrações de vidro fosco no parênquima pulmonar e a Síndrome do Desconforto Respiratório Agudo (SDRA).
Como não existem medicamentos eficazes para combater esse vírus até agora, ganhar tempo para o paciente entre o início dos sintomas e a necessidade de ventilação mecânica pode diminuir a taxa de mortalidade devido à SDRA. Segundo Domingo et al. (2020), a implicação do vírus e os mecanismos dependentes do hospedeiro na patogênese da COVID-19 sugere que qualquer estratégia terapêutica deve combinar drogas antivirais e terapias coadjuvantes para modular as respostas no hospedeiro.
Em um estudo de importância histórica, onde o TMO foi utilizado durante a pandemia do vírus da influenza (1918-1920), as taxas de morbidade e mortalidade dos pacientes foram reduzidas utilizando-se técnicas de tratamento linfático (Smith, 1920 em um estudo observacional / republicada na JAOA em 2000).
O TMO também já foi recomendado por médicos e cientistas contra a gripe aviária H5N1 em 2007 (Patterson MM. 2005 e Hruby RJ. e Hoffman KN. 2007). Em 2010, em um ensaio clínico randomizado controlado, Noll et. al utilizaram Tratamento Manipulativo Osteopático (TMO), através de um protocolo previamente publicado (Noll et. al. 2008), como tratamento adjuvante em pacientes hospitalizados com pneumonia, demonstrando um potencial efeito na duração do tempo de internação que tendeu a ser menor, redução de antibióticos intravenosos ministrados, assim como a incidência de insuficiência respiratória e morte no grupo que recebeu o tratamento proposto. Em 2016, Noll. et. al fizeram uma análise dos subgrupos do ensaio de 2010, para elucidar melhor as características dos pacientes que eram mais propensos a se beneficiarem do TMO. Assim, idade, índice de gravidade de pneumonia e tipo de pneumonia foram avaliados nos grupos do estudo. A presente análise sugeriu que o TMO coadjuvante ao trabalho medicamentoso reduziu o tempo de internação em participantes com idade entre 50 e 74 anos de idade e reduziu as taxas de mortalidade hospitalar nos pacientes acima de 75 anos, parecendo ser benéfico também para os participantes com maior gravidade da doença, reduzindo o tempo de permanência hospitalar em PSI classe IV e reduzindo as taxas de mortalidade em PSI classe V se comparado ao grupo que fez apenas o trabalho medicamentoso.
Os estudos, apesar de sugerirem que o TMO tem potencial para desempenhar um papel significativo em ajudar a reduzir a morbidade, mortalidade, o tempo de internação e a necessidade de um paciente para a ventilação mecânica, ainda apresentam falhas em seus métodos que podem ser corrigidas em pesquisas futuras a fim de se comprovar tal potencial. Adaptações quanto ao tamanho da amostra, melhores critérios para inclusão e exclusão de pacientes e a introdução de mais técnicas de âmbito linfático ao protocolo utilizado em 2010 podem potencializar os resultados já encontrados.
O presente projeto de estudo se propõe a realizar tais adaptações, a fim de engrandecer e fomentar os resultados já encontrados previamente.
2. FUNDAMENTAÇÃO TEÓRICA
2.1 Conceito
Em dezembro de 2019 uma nova patologia epidêmica aparece no Mercado Atacadista de Frutos do Mar de Wuhan, província de Hubei na China, com pacientes apresentando pneumonia viral provocada por um agente microbiano desconhecido. O mercado foi fechado em 01 de janeiro de 2020 e em 11 e 12 de janeiro de 2020 a OMS recebeu informações detalhadas sobre o surto, onde 41 casos foram diagnosticados e reportados (WHO, 2020).
Após sequenciamento genético através de amostras de lavagem broncoalveolar obtida dos núcleos dos pacientes de Wuhan, verificou-se que o agente microbiano ainda não identificado na época estava intimamente relacionado ao coronavírus responsável pelo surto da Síndrome Respiratória Aguda Grave (SARS) em 2003 (Ren et al., 2020).
Em 11 de fevereiro de 2020, o Comitê Internacional de Taxonomia de Vírus (ICTV) anuncia “síndrome respiratória aguda grave coronavírus 2 (SARS-CoV-2)” como o nome do novo vírus e a Organização Mundial de Saúde (OMS) seguindo diretrizes previamente desenvolvidas com a Organização Mundial de Saúde Animal (OIE) e a Organização das Nações Unidas para Agricultura e Alimentação (FAO) anuncia o nome da doença como “”COVID-19” (WHO, 2020).
2.2 Aspectos Epidemiológicos
2.2.1 Número de Casos e Óbitos
Até o momento, segundo a Organização Mundial de Saúde, temos cerca de 64.603.428 casos confirmados e 1.500.614 de mortes por COVID-19 a nível mundial. As Américas avançam como o continente com maior número de casos com mais de 26 milhões de pessoas infectadas. Se analisarmos as estatísticas por país, o Brasil é o terceiro país com maior número de casos (6.436.650) e o segundo em número de mortes (174.415), perdendo apenas para EUA em número de mortes e EUA e Índia em número de casos (Painel da WHO).
A nível Brasil, segundo dados do Ministério da Saúde, a região sudeste é a região com maior número de casos e número de mortes, com 2.257.142 e 80.062, respectivamente. O maior índice de mortalidade é encontrado na região centro-oeste, com 99,9/100 mil habitantes (Painel do Ministério da Saúde).
2.2.2 Hospitalizações
Em um estudo, Niquini RP. et al. descreveram as características demográficas e comorbidades dos pacientes hospitalizados por Síndrome Respiratória Aguda Grave (SRAG) em decorrência de COVID-19 no Brasil comparando-os com SRAG causado pelo vírus da Influenza e com a população geral. Segundo o estudo, até a 21º semana epidemiológica (período em que o estudo se baseou), foram identificadas as seguintes situações:
– 94.807 casos de SRAG, onde 31,7% desse total (n= 31.918) eram decorrentes de COVID-19.
– A região sudeste representou 2/3 das hospitalizações.
– Ao avaliar a distribuição por sexo, percebeu-se uma predominância de pacientes do sexo masculino (60%).
– No que diz respeito à faixa etária, foi encontrada uma média de idade de 57 anos (HQ: 44-70) dentre os hospitalizados.
– Indivíduos que se autodeclararam brancos foram maioria entre os hospitalizados, porém o preenchimento dessa variável não foi realizado em 34,5% dos hospitalizados, não podendo, tal informação, ser levada em consideração.
– Dentre as comorbidades, diabetes mellitus, doença renal crônica (DRC), doenças cardiovasculares (DCV) e pneumopatias crônicas foram predominantes em pacientes hospitalizados por SRAG decorrente da COVID-19.
– A hospitalização de gestantes ou puérperas foi significativamente maior do que a estimada para a população geral em todas as faixas etárias. Realizando uma comparação dos achados desse estudo com achados a nível mundial, percebe-se que a média de idade observada em pacientes hospitalizados no Brasil foi semelhante à calculada entre pacientes hospitalizados em Wuhan, na China (56, HQ: 46-67) em estudo de coorte retrospectivo realizado (Zhou F. et al., 2020), porém menor à obtida em pacientes hospitalizados nos EUA (63, HQ: 52-75) e na Itália (63, HQ: 56-70) em estudos realizados nessas regiões (Richardson S. et al., 2020 e Grasselli G. et al., 2020 respectivamente). Quando comparamos o sexo, percebemos uma semelhança na predominância de homens hospitalizados, mencionados em todos esses estudos. Em relação às comorbidades, quando falamos de diabetes mellitus, DRC e pneumopatias crônicas a prevalência de hospitalizações a nível Brasil se mostraram superiores (25% para diabetes, 4% para DRC e 4% para pneumopatias) às da China (19% para diabetes, 1% para DRC e 3% para pneumopatias) e Itália (17% para diabetes, 3% para DRC e 4% para pneumopatias) e inferior à dos EUA (34% para diabetes, 5% para DRC e 5% para pneumopatias). Já quando falamos de DCV, Brasil tem nível de prevalência maior (41%) que China (38%) e menor que Itália (49%) e EUA (57%).
2.2.3 Custos
Até o momento, no Brasil, já foram gastos pela União com combate à COVID 19 488,9 bilhões, com a expectativa de chegar a 587,7 bilhões (Painel de Transparência do Tesouro Nacional).
Os custos assistenciais hospitalares ainda são incertos, porém, uma empresa privada de soluções em gestão de saúde realizou um estudo em 12 hospitais brasileiros (entre públicos, privados e filantrópicos) que disponibilizaram suas unidades para atendimento à pacientes de COVID-19, no período de abril a maio. A metodologia de custeio foi padronizada, a qual se considerou que todos os custos de produção fossem alocados ao custo da diária, incluindo custos diretos e indiretos, ou seja, todos os custos necessários para operação de um leito hospitalar, como custos com equipes médica e enfermagem, materiais, medicamentos, EPIs (Equipamentos de Proteção Individual), serviços de apoio e administrativo, entre outros. Nesse estudo o custo médio de diária em unidade de internação não crítica com paciente COVID-19 foi R$ 1.400,00, com taxa de ocupação média de 50%; enquanto em unidades de internação crítica adulto (UTI), o custo médio foi R$ 2.452,00 com taxa de ocupação média de 67%.
Rees EM. et al., em uma revisão sistemática, verificou que a média de dias de internação hospitalar por COVID-19 dentro da China era de 14 dias (IQR: 11-19) e fora dela 5 dias (IQR: 3-9). Para a UTI a média de dias de internação foram de 8 dias (IQR:5-13) na China e 7 dias (IQR:4-11) fora dela.
2.3 Sequelas da COVID-19
Como parte do processo fisiopatológico da COVID-19, é gerada uma intensa resposta inflamatória que atinge primeiro o trato respiratório, principalmente os pulmões. No entanto, diversos estudos sugerem que as sequelas dessa infecção não se limitam apenas ao sistema respiratório. Podemos ver tais sequelas no sistema cardiovascular, sistema nervoso central e periférico (Vindegaard N. e Benros ME. 2020) e até mesmo sequelas psiquiátricas e psicológicas.
2.3.1 Sequelas no Sistema Respiratório
Durante a fase aguda da infecção por SARS-CoV-2, o dano pulmonar causa edema, liberação alveolar de células epiteliais e deposição de material hialino nas membranas alveolares. Na fase seguinte da infecção, que geralmente ocorre entre a segunda e a quinta semana, os pulmões apresentam sinais de fibrose, com deposição de fibrina e infiltrado de células inflamatórias e fibroblastos próximos às células epiteliais nos espaços alveolares. Durante o estágio final, entre a sexta e a oitava semana, o tecido pulmonar torna-se fibrótico. Além disso, há vários relatos de lesões bilaterais com predomínio do lobo inferior (Delpino MV. e Quarleri J. 2020; Gentile F. et al. 2020 e Sohail S. 2020).
2.3.2 Sequelas no Sistema Cardiovascular
Foi documentado que os pacientes com formas graves de COVID-19 apresentaram lesões miocárdicas significativas, incluindo miocardite relacionada à infecção, com redução da função sistólica e arritmias. Essas lesões podem ser secundárias a danos pulmonares graves. Infelizmente, pouco se sabe sobre os mecanismos responsáveis por essas sequelas. Preliminarmente, presume-se que a enzima conversora de angiotensina 2 (ECA2) estaria envolvida, o que permite que o vírus entre nas células e facilite a replicação viral. Níveis significativamente elevados de ECA2 foram encontrados no tecido cardíaco (cardiomiócitos e pericitos), principalmente em pacientes com doenças cardiovasculares preexistentes (Bose R. e McCarthy JR., 2020). Foi relatada lesão miocárdica, que pode ser decorrente de dano direto aos cardiomiócitos, inflamação sistêmica, fibrose intersticial miocárdica e hipóxia (Babapoor-Farrokhran S. et al. 2020). Devido às lesões miocárdicas significativas em pacientes com manifestações clínicas graves de COVID-19, a morbidade e letalidade da doença podem ser altas, especialmente em pacientes com doenças cardiovasculares preexistentes (Aggarwal G. et al. 2020; Clerkin KJ. et al. 2020 e Bansal M. 2020).
2.3.3 Sequelas Neuropsiquiátricas
Em casos graves de COVID-19, a resposta hiperinflamatória sistêmica pode causar declínio cognitivo a longo prazo, como deficiências de memória, atenção, velocidade de processamento e funcionamento, juntamente com perda neuronal difusa (Cothran TP. et al., 2020). Além disso, foi documentado que processos inflamatórios sistêmicos em pessoas de meia-idade podem levar a um declínio cognitivo décadas mais tarde. No entanto, são necessárias mais evidências para avaliar os efeitos independentes e sinérgicos das sequelas da COVID-19 nas funções cognitivas de curto e longo prazo. Portanto, será necessária uma avaliação em longo prazo dessas características e sinais nos pacientes recuperados de COVID-19.
Além disso, há relatos de que o SARS-CoV-2 pode atingir os sistemas nervoso central e periférico, com disseminação hematogênica ou disseminação neural direta através do trato respiratório por possíveis mecanismos de neurotropismo viral. O receptor da ECA2 desempenharia um papel no mecanismo pelo qual o vírus SARS-CoV-2 entraria nas células centrais. Também foram observados vários tipos de manifestações clínicas neuropsiquiátricas, como encefalopatia aguda, alterações de humor, psicose, disfunção neuromuscular ou processos desmielinizantes, que podem acompanhar uma infecção viral aguda ou podem ocorrer após uma infecção em pacientes recuperados após semanas, meses ou anos até.
Portanto, o acompanhamento neuropsiquiátrico prospectivo de indivíduos expostos ao SARS-CoV-2, bem como a avaliação de seu estado neuroimunológico, é crucial para compreendermos completamente o impacto de longo prazo das manifestações neuropsiquiátricas da COVID-19 (Rogers JP. et al. 2020; Polak SB. et al. 2020 e Troyer EA. et al. 2020).
Faz-se necessária uma avaliação mais aprofundada das consequências neuropsiquiátricas diretas e dos efeitos indiretos da COVID-19 na saúde mental dos pacientes recuperados, a fim de traçar um melhor planejamento dos cuidados de saúde mental dos mesmos.
2.3.4 Sequelas Psicológicas
A disseminação da COVID-19 globalmente resultou em esforços para garantir o distanciamento social, o que poderia levar a efeitos psicológicos negativos devido ao isolamento social.
Todas as faixas etárias — crianças, adolescentes, adultos jovens e idosos – correm o risco de sofrer consequências psicológicas devido às medidas de saúde pública implementadas durante a pandemia (Imran N. et al. 2020 e Beam CR. e Kim AJ. 2020), bem como grupos específicos, tais como profissionais de saúde, que podem vir a sofrer repercussões da doença em sua saúde mental (Kisely S. et al. 2020 e Salazar de Pablo G. et al. 2020).
2.4 TMO na COVID-19
Em uma revisão de literatura, Marin T. et al. 2020, realizaram uma pesquisa bibliográfica para encontrar todo o material necessário que pudesse fomentar a potencial influência que o TMO tem em todos os aspectos pertinentes à COVID-19, tanto no âmbito curativo como também nos âmbitos preventivo e paliativo. Todos os materiais encontrados sugerem que o TMO quando administrado pode contribuir para modular a imunidade, os processos inflamatórios e a proliferação de fibroblastos que resultam de uma infecção como a SARS. A literatura também permitiu identificar os elementos-chave do TMO que poderiam influenciar os processos fisiopatológicos da COVID-19, aliviando os sintomas e as afecções sistêmicas encontradas nos seguintes sistemas: sistema respiratório, sistema digestivo, cardiovascular, renal e nervoso.
3. PROBLEMA DE PESQUISA
O uso do TMO como tratamento adjuvante ao tratamento padrão em pacientes hospitalizados com COVID-19 diminui o tempo de internação e os efeitos deletérios funcionais desses pacientes, se comparado a utilização apenas de protocolo padrão?
4. HIPÓTESES DA PESQUISA
H° – O uso do TMO como tratamento adjuvante ao tratamento padrão em pacientes hospitalizados com COVID-19 não diminui o tempo de internação e os efeitos deletérios funcionais nestes pacientes se comparado a utilização apenas de protocolo padrão.
H¹ – O uso do TMO como tratamento adjuvante ao tratamento padrão em pacientes hospitalizados com COVID-19 diminui o tempo de internação e os efeitos deletérios funcionais nestes pacientes se comparado a utilização apenas de protocolo padrão.
5. OBJETIVOS
5.1 Objetivos Gerais
Verificar se o uso do TMO quando associado ao tratamento padrão em pacientes hospitalizados com COVID-19, diminui os dias de internação e minimiza os efeitos deletérios funcionais comparando o emprego desse tipo de terapêutica com a aplicação apenas do protocolo padrão.
5.2 Objetivos Específicos
Comparar o tempo de internação hospitalar entre os indivíduos alocados nos grupos intervenção (GI), estes submetidos ao tratamento manipulativo osteopático em conjunto à terapêutica padrão, grupo controle (GC), estes submetidos à manipulação simulada adjuvante ao tratamento padrão e grupo protocolo padrão (GPP), estes submetidos ao tratamento padrão utilizado na atualidade.
Comparar o tempo de utilização de medicação ministrada entre os grupos GI, GC e GPP.
Comparar a incidência de insuficiência respiratória entre os grupos GI, GC e GPP.
Comparar as taxas de morbidade e mortalidade nos grupos GI, GC e GPP. Comparar a recuperação e qualidade de vida funcional dos indivíduos dos grupos após a alta hospitalar.
6. DESFECHOS DE INTERESSE
6.1 Desfechos Primários
Os desfechos primários serão: tempo de internação, tempo para estabilidade clínica e uma pontuação de recuperação sintomática e funcional.
VARIÁVEL DEFINIÇÃO INSTRUMENTO Tempo de Internação Definido pela data e hora do pedido de admissão até a alta. Registro em prontuário médico e repassado ao responsável pela pesquisa. Tempo Para Estabilidade Clínica Definido como dia do calendário do hospital quando todos os sete parâmetros clínicos primeiro atenderam aos critérios de estabilidade (P.A. sistólica ≥ 90 mmHg; frequência cardíaca ≤ 100 bpm; frequência respiratória ≤ 24 irpm; temperatura ≤ 38º; saturação de oxigênio ≥ 90%; capacidade de alimentação pela boca ou tubo e estado mental de volta à linha de base pré-doença – Halm, EA. et al., 1998) Dados registrados diariamente em prontuário e repassados ao responsável pela pesquisa. Recuperação Sintomática e Funcional “follow up” Definido como recuperação dos sintomas e da funcionalidade de atividades de vida diária nos aspectos físicos e mentais. 2 questionários: um abordando 5 sintomas (tosse, dispneia, produção de expectoração, dor torácica de origem pleural e fadiga – Metley JP. et al., 1997) e outro abordando 8 componentes (capacidade funcional, aspectos físicos, dor, saúde geral, vitalidade, aspectos sociais, emocionais e de saúde mental – Laguardia, et al., 2013) administrados na admissão e nos dias 14, 30, 60 e 90.
6.2 Desfechos Secundários
Os desfechos secundários serão: a duração da administração de medicamentos e o final do tratamento seja para alta, insuficiência respiratória ou morte, todos mensurados através de dados registrados em prontuário e repassados ao responsável pela pesquisa.
7. MATERIAIS E MÉTODOS
7.1 Delineamento do Estudo
Ensaio clínico multicêntrico, randomizado, controlado, duplo cego (pacientes e avaliadores), com pacientes divididos em três grupos: Grupo Intervenção (GI), Grupo Controle (GC) e Grupo Protocolo Padrão (GPP).
7.2 Amostra
A amostra do estudo será composta de indivíduos de ambos os sexos, com faixa etária igual ou acima de 50 anos de idade recém hospitalizados que apresentam diagnóstico médico de COVID-19, os quais serão alocados em três grupos: GI no qual será realizado um protocolo de TMO associado ao tratamento convencional, GC no qual será realizado um tratamento simulado em combinação com o tratamento convencional e GPP onde será realizado o tratamento convencional padrão para pacientes hospitalizados com COVID-19.
O tamanho da amostra foi baseado no estudo de Noll et. al, que utilizou um tempo médio de internação de 7,5 dias e para tal foram utilizados 406 indivíduos. O recrutamento será feito em 5 hospitais de referência para tratamento de pacientes com COVID-19, um em cada região do Brasil (sul, sudeste, centro-oeste, norte e nordeste).
7.3 Critérios de Elegibilidade
Os critérios de inclusão são: participantes de ambos os sexos, com idade igual ou acima de 50 anos, hospitalizados, admitidos com diagnóstico clínico de COVID-19 confirmado através de exame clínico, diagnóstico laboratorial e/ou imagem que concordarem em participar do estudo.
Os critérios de exclusão são: participantes que tenham sinais e sintomas clínicos de COVID-19, porém não tenham diagnóstico fechado através de exames laboratoriais e/ou imagem, indivíduos com qualquer condição que contra indique os tratamentos e/ou as técnicas propostas (neoplasias e/ou metástases, doenças ósseas de origem metabólicas não controladas, fratura de costela ou vértebra e hipertensão arterial), pacientes com insuficiência respiratória entubados e pacientes que não concordarem em participar do estudo.
7.4 Randomização
A randomização estratificada, através do software Random Allocation, será utilizada em cada local de estudo para alocar todos os 406 indivíduos a um dos três grupos: GI (n= 136), GC (n= 135) e GPP (n= 135) A alocação será ocultada em envelopes opacos, selados, que serão abertos somente após a admissão do indivíduo no estudo.
7.5 Cegamento
Nesse estudo todos os pacientes, médicos que ministrarão os protocolos de tratamentos convencionais em todos os grupos e os responsáveis pelas coletas dos dados da pesquisa que serão a equipe de cuidados de saúde daqueles respectivos pacientes estão cegados quanto a alocação e o tratamento que cada indivíduo receberá. Somente os 5 Osteopatas responsáveis pelo tratamento nos grupos GI e GC terão conhecimento da alocação e do tratamento dos respectivos indivíduos. Um responsável pela coleta de dados aplicará um questionário 24 horas após a alta do estudo para avaliar a eficácia do cegamento dos pacientes.
7.6 Intervenção
Grupo Intervenção (GI):
Nesse grupo os indivíduos serão avaliados e receberão um protocolo de tratamento de TMO, em decúbito dorsal, dividido em 2 componentes: um componente de TMO padronizado utilizando-se 9 técnicas durante aproximadamente 10 minutos (esta padronização com o objetivo de se ter uma reprodutilidade científica) e um componente de TMO não padronizado durante aproximadamente 5 minutos, permitindo assim o tratamento de achados estruturais exclusivos de cada indivíduo e suas disfunções somáticas (fazendo com que a abordagem reflita a aplicação clínica atual do TMO) + tratamento convencional realizado como protocolo atual para pacientes internados com COVID-19.
Grupo Controle (GC):
Nesse grupo os indivíduos receberão o mesmo protocolo de tratamento de TMO em dois componentes em decúbito dorsal, porém de maneira simulada. Durante os 10 minutos do componente padronizado algumas diretrizes serão seguidas, para minimizar o potencial efeito e não intencional do toque no sistema neuromusculoesquelético, tais como: evitar o toque prolongado em qualquer área do corpo, movendo as mãos aproximadamente a cada 5 segundos para evitar que o tecido responda a forças mecânicas de tempo prolongado; sempre que possível, entrar em contato com os locais adjacentes, mas não diretamente com os locais envolvidos durante o protocolo, especialmente a coluna vertebral; usar os princípios de fulcro, direcionando mais a força no colchão da cama, minimizando a força aplicada ao tecido e achatar e amolecer a superfície das mãos de tratamento para minimizar as áreas focais de força. Para o tempo do componente não padronizado (5 minutos aproximadamente) o osteopata fará a ausculta do pulso carotídeo bilateralmente, ausculta cardíaca e pulmonar do paciente. Associado ao protocolo simulado de TMO o paciente também receberá o tratamento convencional dado aos pacientes com COVID-19.
Grupo Protocolo Padrão (GPP):
Nesse grupo os pacientes receberão apenas o protocolo padrão de tratamento dado aos pacientes com diagnóstico médico de COVID-19.
7.6.1 Considerações sobre as Intervenções
Os tratamentos de TMO do GI e GC serão realizados por 5 osteopatas (um em cada unidade hospitalar) com mais de 5 anos de experiência, que terão conhecimento sobre a alocação e os respectivos tratamentos a serem realizados nos sujeitos da pesquisa, porém não terão conhecimento dos dados que serão coletados. Os atendimentos com TMO serão iniciados dentro de 24 horas após a admissão do indivíduo e serão realizados por aproximadamente 15 minutos (não menos de 13 e não mais que 17 minutos), 2 (duas) vezes ao dia com um intervalo de pelo menos 6 horas entre um atendimento e outro e somente serão interrompidos em casos de cessação de tratamento medicamentoso, insuficiência respiratória ou morte. Os atendimentos com TMO serão continuados mesmo após alta hospitalar naqueles que ainda se utilizarem de medicamentos de tratamento convencional de forma domiciliar. Esses atendimentos serão realizados em ambulatórios montados provisoriamente dentro dos hospitais.
Como ainda não se tem um consenso de um protocolo a ser seguido em âmbito nacional, em termos de medicamentos principalmente, os protocolos padrões utilizados nos respectivos grupos será o adotado em cada unidade hospitalar para aquela região.
O contato entre os participantes será evitado e os atendimentos serão individualizados.
7.6.2 Protocolo de Técnicas do Tratamento Manipulativo Osteopático
As técnicas de manipulação do TMO do primeiro componente de atendimento (10 minutos) serão ministradas na seguinte sequência:
1) Soft Tissue To The Thoracic And Upper Lumbar Paraspinal Muscles (técnicas de tecidos moles da região torácica e região lombar alta): o osteopata senta-se ou fica de pé ao lado da cama e aplica uma técnica de liberação dos músculos paravertebrais torácicos do paciente. Mais atenção pode ser dada às áreas de rigidez ou espasmo muscular. O osteopata pode usar a inibição nessas áreas, mas toda a área paravertebral torácica é tratada. A duração aproximada é de 1 minuto.
2) Rib Raising (elevação das costelas): o osteopata se senta ou fica de pé ao lado da cama e coloca as mãos sob o tórax do paciente, fazendo contato com os ângulos das costelas com as pontas dos dedos. Com os dedos flexionados, o prático aplica tração lateral ao ângulo da costela. Enquanto a tração é mantida, os punhos do mesmo permanecem retos enquanto suas mãos se movem em direção ao lado anterior do corpo do paciente, aumentando o ângulo costal do paciente. O braço do prático é usado como alavanca e a lateral da cama como ponto de apoio fixo para produzir elevações e abaixamentos suaves e constantes da caixa torácica. Este movimento é repetido várias vezes. As mãos do terapeuta são então movidas para cima na caixa torácica e o procedimento é repetido até que todas as costelas sejam tratadas. As áreas restritas são tratadas com mais intensidade para promover o movimento normal. A técnica é repetida do outro lado. A duração aproximada é de 2 minutos.
3) Indirect Myofascial Technique To Dome The Diaphragm or Improve Diaphragmatic Motion (técnica miofascial indireta para as cúpulas diafragmáticas ou para aumentar a mobilidade diafragmática): do lado da cama, o osteopata coloca uma mão sob o paciente na parte onde os músculos diafragmáticos se prendem às costelas e vértebras inferiores e coloca a outra mão na área epigástrica abdominal. As mãos do terapeuta são giradas em direções opostas para determinar a direção de maior liberdade de movimento. Os tecidos são então movidos na direção de maior liberdade para um ponto de equilíbrio e mantidos lá até que uma liberação da tensão do tecido seja palpada. A duração aproximada é de 1 minuto.
4) Soft Tissue To The Cervical Spine (tecidos moles da coluna cervical): da cabeceira da cama, o osteopata coloca suas mãos nos músculos paravertebrais cervicais do paciente para promover uma liberação e alongamento de todos os tecidos moles. A duração aproximada é de 1 minuto.
5) Suboccipital Inhibition (inibição suboccipital): da cabeceira da cama, o osteopata coloca as pontas dos dedos nos músculos suboccipitais na base do crânio do paciente. Uma tração externa e cefálica constante e suave é aplicada para conseguir um relaxamento da tensão desses tecidos. A duração aproximada é de 1 minuto.
6) Myofascial Release To The Thoracic Inlet (liberação miofascial do orifício superior do tórax): da cabeceira da cama, o osteopata coloca as mãos com os polegares apoiados sobre os processos transversos do primeiro segmento torácico posteriormente e os dedos nas clavículas e duas primeiras costelas anteriormente. O teste de movimento passivo é usado para determinar a direção na qual os tecidos se movem mais livremente. Os tecidos são mantidos em posição indireta (direção de fluidez) até que a liberação seja palpada. Se uma restrição de tecido ainda for palpada, os tecidos são levados para uma posição direta (direção de restrição) até que uma liberação seja palpada. A duração aproximada é de 1 minuto.
7) Thoracic Lymphatic Pump With Activation (bomba linfática torácica com ativação): na cabeceira da cama, o osteopata coloca as mãos na parede torácica anterior do paciente com as eminências tenares de cada mão sobre os músculos peitorais, logo abaixo das clavículas. Os dedos ficarão abertos e angulados em direção às laterais do corpo do paciente. O mesmo é instruído a respirar fundo e expirar. Durante a expiração, o prático aplica pressões rápidas e alternadas a uma taxa de aproximadamente 120 compressões e relaxamentos por minuto na parede torácica, o que induz uma ação de bombeamento rítmico. No final da expiração, alguma pressão será mantida na parede torácica. Este procedimento é repetido duas ou três vezes. A pressão da parede torácica do paciente aumenta a cada expiração sucessivamente e é sustentada com a inspiração subsequente. Na terceira ou quarta inspiração, durante o primeiro terço dela, as mãos do terapeuta são rapidamente removidas da parede torácica. Esse movimento causa uma liberação repentina da pressão acumulada na caixa torácica e faz com que a mesma se expanda rapidamente, criando um aumento repentino na pressão intratorácica negativa e fazendo com que o ar entre nos pulmões. Este ciclo é então repetido. A duração aproximada é de 2 minutos.
8) Abdominal Lymphatic Pump (bomba linfática abdominal – Grande Manobra Abdominal): o osteopata estará de pé na altura da cabeça do paciente que estará, se possível em posição de declive (caso não seja possível, colocar almofadas embaixo da bacia do mesmo). O terapeuta posiciona suas mãos em concha sobre a região mais baixa do abdômen do paciente (as pontas dos dedos tocam a sínfise púbica do paciente). Prático pede respiração ampla do paciente, realizando durante as expirações uma leve supinação com as duas mãos enganchando o mais profundo os tecidos e vísceras para puxá-las na sua direção. Nas fases inspiratórias o prático permite uma leve pronação de suas mãos permitindo que as mesmas desçam em direção ao púbis do paciente novamente. Realiza essa sequência por 4 ou 5 ciclos respiratórios, e no último ciclo aproveitando-se da última expiração realiza uma vibração com suas mãos. Deixa o paciente respirar e realizar essa técnica por 2 ou 3 séries. A duração é de aproximadamente 2 minutos.
9) Pedal Lymphatic Pump (bomba linfática podal): o osteopata fica ao pé da cama e realiza o movimento de dorsiflexão suave e ritmada dos pés do paciente, fazendo com que o conteúdo abdominal bata intermitentemente contra o diafragma abdominal. No caso de um paciente com amputação de membro inferior, o prático colocará suas mãos na porção mais distal do membro inferior. A duração aproximada é de 1 minuto.
As técnicas teciduais promoverão um relaxamento muscular reduzindo a tensão nos respectivos tecidos. A técnica de elevação das costelas (rib raising) tem o propósito de melhorar a movimentação da caixa torácica, assim como estimular os gânglios da cadeia simpática. As técnicas de liberação do diafragma e liberação do orifício superior do tórax são usadas para melhorar a mobilidade do diafragma e o fluxo da drenagem linfática. A inibição suboccipital considera a liberação das restrições ao redor dos nervos vagos, melhorando assim, a função nervosa. Por fim, as técnicas de bombas linfáticas torácica, abdominal e podal são realizadas para estimular e melhorar a circulação linfática, visando um aumento do sistema imunológico.
7.7 Locais de Pesquisa
Instituições que se disponibilizarem ao estudo.
7.8 Considerações Éticas
O presente estudo obedecerá a todas as regras básicas da resolução 466/12 do Conselho Nacional de Saúde (CNS) em relação à ética em pesquisa com seres humanos. O mesmo não oferece risco à saúde dos participantes, porém a qualquer sinal de intercorrência ou piora dos sintomas os médicos assistentes serão acionados e o tratamento reavaliado e/ou interrompido.
Serão entregues duas cópias do termo de consentimento livre e esclarecido (TCLE) para cada participante do estudo assine, segundo a mesma resolução. Uma ficará com o participante e a outra com a equipe de pesquisa (ANEXO A).
A identidade dos indivíduos será mantida em sigilo, mas os resultados da presente pesquisa serão divulgados em eventos e publicações científicas para contribuição com o conhecimento da profissão e benefício da comunidade.
8. PROCEDIMENTO PARA COLETA DE DADOS
8.1 Avaliação Inicial
A avaliação inicial será feita pelo médico responsável pela triagem dos pacientes nas respectivas unidades hospitalares, que fará o diagnóstico clínico baseado nos sinais e sintomas do paciente e confirmado através de exames laboratoriais e/ou de imagem. A anamnese realizada pelo mesmo incluirá identificação completa do paciente contendo sexo, idade, etnia, índice de massa corporal, histórico médico completo pregresso e atual, principais comorbidades para identificação de fatores de risco, hábitos de vida relacionados a histórico de tabagismo, uso atual de álcool, prática de atividade física e hábitos alimentares. Ao exame físico deverá constar a pressão arterial, frequência cardíaca e respiratória, verificação da temperatura e saturação de oxigênio presente no corpo. Na admissão serão aplicados ainda dois questionários para posterior avaliação da recuperação dos sintomas e recuperação funcional durante follow up.
8.2 Tempo de Internação, Tempo para Estabilidade Clínica e Duração de Administração de Medicamentos
Os dados serão coletados pelas equipes de profissionais de cuidados médicos responsáveis pelos pacientes nas respectivas unidades hospitalares, que estão cegados quanto à alocação e ao tratamento a que cada indivíduo será submetido, registrados em prontuário e repassados para o responsável do estudo.
8.3 Recuperação Sintomática e Funcional (Follow Up)
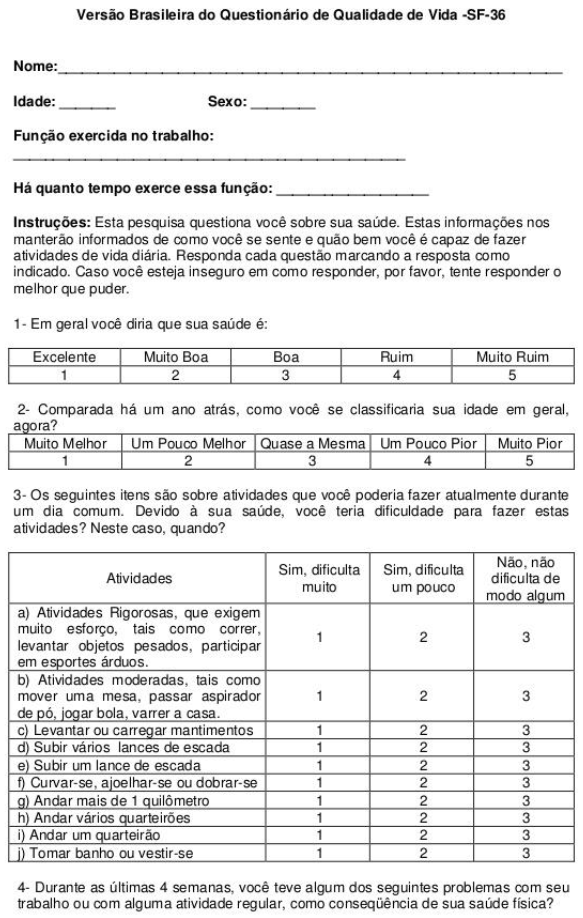
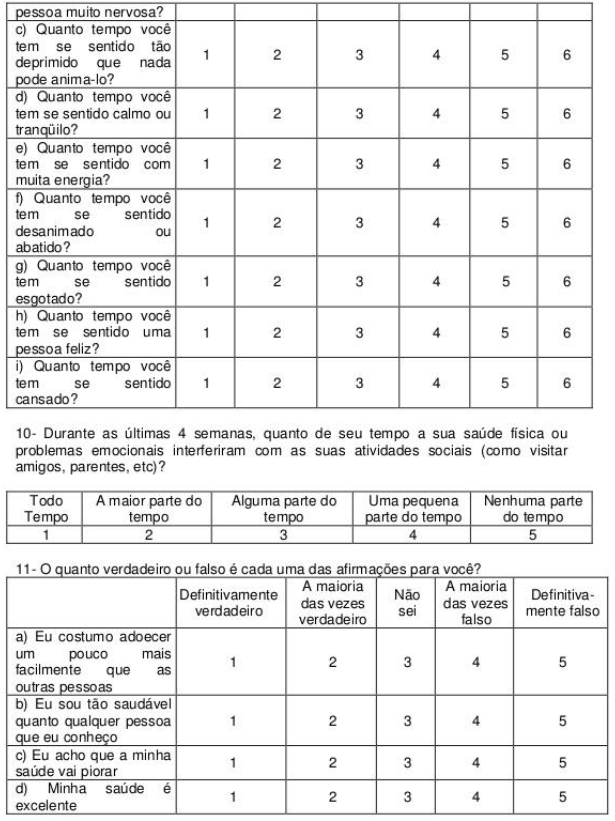
Dois questionários serão aplicados para avaliação desta variável. Um questionário validado específico para pneumonia abordando 5 sintomas (tosse, dispneia, produção de expectoração, dor torácica de origem pleural e fadiga). Pontuações altas indicam mais sintomas nesse questionário. E outro questionário genérico de qualidade de vida, abordando 8 componentes (capacidade funcional, aspectos físicos, dor, saúde geral, vitalidade, aspectos sociais, emocionais e de saúde mental). Nesse questionário, pontuações baixas indicam piores resultados para qualidade de vida e saúde (ANEXO B).
Os questionários serão administrados durante a avaliação inicial (admissão), nos dias 14, 30, 60 e 90.
Detalhes do desenho do estudo podem ser vistos a seguir na figura 1.
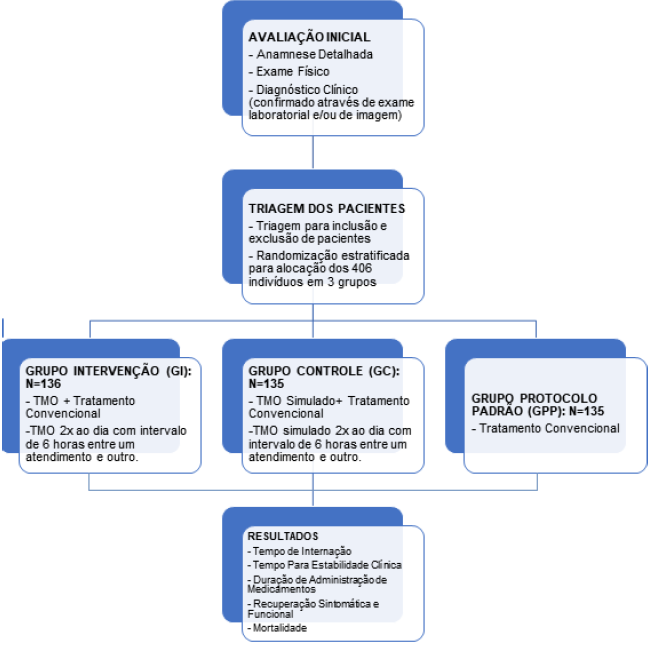
Figura 1: Desenho do Estudo
9. PROCEDIMENTO ESTATÍSTICO
Após a avaliação e admissão, os participantes receberão um código numérico com três dígitos para sua localização durante o estudo (tal código iniciará a partir de 100). Este código numérico será colocado em todos os prontuários. Uma listagem contendo o nome dos participantes com o respectivo código ficará sob a responsabilidade apenas do responsável pelo projeto.
Os dados coletados serão armazenados em uma tabela do Programa Microsoft Excel, após serão transferidos e analisados utilizando o pacote estatístico SPSS 2.0 (Statistical Package for Social Sciences).
Valores de média e desvio padrão serão calculados para cada variável do estudo e o princípio da intenção de tratar também será utilizado (Hollis S, Campbell F., 1999).
LISTA DE ABREVIATURAS E SIGLAS
BPM – Batimentos Por Minuto
CNS – Conselho Nacional de Saúde
DRC – Doença Renal Crônica
DCV – Doenças Cardiovasculares
ECA2 – Enzima Conversora de Angiotensina 2
EPIs – Equipamentos de Proteção Individual
FAO – Organização das Nações Unidas para Agricultura e Alimentação GI – Grupo Intervenção
GC – Grupo Controle
GPP – Grupo Protocolo Padrão
ICTV – Comitê Internacional de Taxonomia de Vírus
IRPM – Incursões Respiratórias Por Minuto
OMS – Organização Mundial de Saúde
TMO – Tratamento Manipulativo Osteopático
OIE – Organização Mundial de Saúde Animal
PA – Pressão Arterial
PSI – Índice de Gravidade de Pneumonia
SARS-CoV-2 – Síndrome Respiratória Aguda Grave Coronavírus 2 SDRA – Síndrome do Desconforto Respiratório Agudo TCLE – Termo de Consentimento Livre e Esclarecido
UTI – Unidade de Terapia Intensiva
10. REFERÊNCIAS BIBLIOGRÁFICAS
1. ROUJIAN L. et al. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for vírus origins and receptor binding. The Lancet 2020; 395: 565-574.
2. COVID-19 WEEKLY EPIDEMIOLOGICAL UPDATE IN 04 DECEMBER 2020 Disponível em: https://www.who.int/emergencies/diseases/novel-coronavirus 2019/situation-reports/ . Acesso em: 04 de dezembro de 2020.
3. NICOLA M. et al. The socio-economic implications of the coronavirus and COVID-19 pandemic: a review, International Journal of Surgery 2020; 78: 185– 193.
4. ALRADHAWI M. Effects of the COVID-19 pandemic on mental well-being amongst individuals in society- A letter to the editor on “The socio-economic implications of the coronavirus and COVID-19 pandemic: A review”. International Journal of Surgery 2020; 78: 147–148.
5. MASON RJ. Pathogenesis of COVID-19 from a cell biologic perspective. European Respiratory Journal 2020; in press (https://doi.org/10.1183/13993003.00607-2020).
6. DOMINGO P., et al. The four horsemen of a viral Apocalypse: The pathogenesis of SARS-CoV-2 infection (COVID-19). EBioMedicine 2020; 58: 102887.
7. NOLL DR. et al. Clinical and research protocol for osteopathic manipulative treatment of elderly patients with pneumonia The Journal of the American Osteopathic Association 2008;108(9):508-516.
8. SMITH RK. One hundred thousand cases of influenza with a death rate of one fortieth of that officially reported under conventional medical treatment. The Journal of the American Osteopathic Association 1920; 20: 172-175. Reprinted in: The Journal of the American Osteopathic 2000; 100: 320-323.
9. PATTERSON MM. The coming influenza pandemic: Lessons from the past for the future. The Journal of the American Osteopathic Association 2005; 105 (11): pp. 498-500.
10.HRUBY RJ., HOFFMAN KN. Avian influenza: An osteopathic component to treatment. Osteopath Med Prim Care 2007; 1: pp. 1-19.
11.NOLL DR. et al. Efficacy of osteopathic manipulation as an adjunctive treatment for hospitalized patients with pneumonia: a randomized controlled trial. Osteopath Medicine and Primary Care 2010; 4: 2.
12.NOLL DR. et al. Multicenter osteopathic pneumonia study in the elderly: subgroup analysis on hospital length of stay, ventilator-dependent respiratory failure rate, and in-hospital mortality rate. The Journal of the American Osteopathic Association 2016; Vol. 116: No. 9.
13.NOVEL CORONAVIRUS – CHINA; WORLD HEALTH ORGANIZATION WEBSITE. Disponível em: https://www.who.int/csr/don/12-january-2020-novel coronavirus-china/en/ . Acesso em: 04 de outubro de 2020.
14.REN LL. et al. Identification of a novel coronavirus causing severe pneumonia in human: a descriptive study. Chinese Medical Journal 2020; 133(9):1015-24.
15.NAMING THE CORONAVIRUS DISEASE (COVID-19) AND THE VIRUS THAT CAUSES IT; WORLD HEALTH ORGANIZATION WEBSITE. Disponível em: https://www.who.int/emergencies/diseases/novel-coronavirus-2019/technical guidance/naming-the-coronavirus-disease-(covid-2019)-and-the-virus-that causes-it . Acesso em: 04 de outubro de 2020.
16.COVID-19 WEEKLY EPIDEMIOLOGICAL UPDATE IN 03 NOVEMBER 2020 Disponível em: https://www.who.int/emergencies/diseases/novel-coronavirus 2019/situation-reports/ . Acesso em: 09 de novembro de 2020.
17.WHO CORONAVIRUS DISEASE (COVID-19) DASHBOARD WEBSITE. Disponível em: https://covid19.who.int/ . Acesso em: 09 de novembro de 2020.
18.PAINEL CORONAVÍRUS NO BRASIL WEBSITE. Disponível em: https://covid.saude.gov.br/ . Acesso em: 04 de dezembro de 2020.
19.NIQUINI RP. et al. SRAG por COVID-19 no Brasil: descrição e comparação de características demográficas e comorbidades com SRAG por influenza e com a população geral. Cad. Saúde Pública 2020; 36 (Julho): e00149420
20.ZHOU F. et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet 2020; 395: 1054-62.
21.GRASSELLI G. et al. Baseline characteristics and outcomes of 1591 patients infected with SARS-CoV-2 admitted to ICUs of the Lombardy Region, Italy. JAMA 2020; 323: 1574-81.
22.RICHARDSON S. et al. Presenting characteristics, comorbidities, and outcomes among 5700 patients hospitalized with COVID-19 in the New York City area. JAMA 2020; 323: 2052-59.
23.MONITORAMENTO DE GASTOS DA UNIÃO COM COMBATE À COVID-19 WEBSITE. Disponível em: https://www.tesourotransparente.gov.br/visualizacao/painel-de monitoramentos-dos-gastos-com-covid-19 . Acesso em: 04 de dezembro de 2020.
24.CUSTO HOSPITALAR DA COVID-19 PARA CADA 1,37 MI DE INFECTADOS É CERCA DE 3,1 BI. WEBSITE. Disponível em: https://portalhospitaisbrasil.com.br/custo-hospitalar-da-covid-19-para-cada 137-mi-de-infectados-e-de-cerca-de-r-31-bi/ . Acesso em: 01 de novembro de 2020.
25.REES EM. et al. Covid-19 length of hospital stay: a systematic review and data synthesis. . BMC Medicine 2020; 18: 270.
26.VINDEGAARD N, BENROS ME. COVID-19 pandemic and mental health consequences: Systematic review of the current evidence. Brain Behav Immun. 2020; S0889 1591(20)30954-5. Publicação online antecipada.
27.DELPINO MV. & QUARLERI J. SARS-CoV-2 Pathogenesis: Imbalance in the Renin-Angiotensin System Favors Lung Fibrosis. Frontiers in Cellular and Infection Microbiology 2020; 10: 340.
28.GENTILE F. et al. COVID-19 and risk of pulmonary fibrosis: the importance of planning ahead. European Journal of Preventive Cardiology 2020; 2047487320932695. Publicação online antecipada.
29.SOHAIL S. Radiology of COVID-19 – Imaging the pulmonary damage. The Journal of the Pakistan Medical Association 2020; 70 (Suppl 3) (5): S60–S63.
30.BOSE R. E MCCARTHY JR. Direct SARS-CoV-2 infection of the heart potentiates the cardiovascular sequelae of COVID-19. Drug Discovery Today 2020 S1359-6446(20)30249-X. Publicação on-line antecipada.
31.BABAPOOR-FARROKHRAN S. et.al Myocardial injury and COVID-19: Possible mechanisms. Life Sciences 2020; 253: 117723.
32.AGGARWAL G. et al. Association of Cardiovascular Disease with Coronavirus Disease 2019 (COVID-19) Severity: A Meta-Analysis. Current Problems in Cardiology 2020; 45 (8): 100617.
33.CLERKIN KJ. et al. COVID-19 and Cardiovascular Disease. Circulation 2020; 141: 1648–1655.
34.BANSAL M. Cardiovascular disease and COVID-19. Diabetes and metabolic syndrome 2020; 14: 247–250.
35.COTHRAN TP. et al. A brewing storm: The neuropsychological sequelae of hyperinflammation due to COVID-19. Brain, Behavior, and Immunity 2020; S0889-1591(20)31209-5. Publicação on-line antecipada.
36.ROGERS JP. et al. Psychiatric and neuropsychiatric presentations associated with severe coronavirus infections: a systematic review and meta-analysis with comparison to the COVID-19 pandemic. The Lancet Psychiatry 2020; 7(7): 611-627.
37.POLAK SB. et al. A systematic review of pathological findings in COVID-19: a pathophysiological timeline and possible mechanisms of disease progression. Modern Pathology: an 35ficial jornal of the United States and Canadian Academy of Pathology, Inc, 2020; 1–11. Publicação on-line antecipada.
38.TROYER EA. et al. Are we facing a crashing wave of neuropsychiatric sequelae of COVID-19? Neuropsychiatric symptoms and potential immunologic mechanisms. Brain, Behavior, and Immunity 2020; 87: 34–39.
39.IMRAN N. et al. Psychological burden of quarantine in children and adolescents: A rapid systematic review and proposed solutions. Pakistan Journal of Medical Sciences 2020; 36(5): 1106–1116.
40.BEAM CR. AND KIM AJ. Psychological sequelae of social isolation and loneliness might be a larger problem in young adults than older adults. Psychological Trauma: Theory, Research, Practice, and Policy, 10.1037/tra0000774. Publicação on-line antecipada.
41.KISELY S. et al. Occurrence, prevention, and management of the psychological effects of emerging virus outbreaks on healthcare workers: rapid review and meta-analysis. BMJ 2020; 369: m1642.
42.SALAZAR DE PABLO G.et al. Impact of coronavirus syndromes on physical and mental health of health care workers: Systematic review and meta analysis. Journal of Affective Disorders 2020; 275: 48–57.
43.MARIN T. et al. Evidence-based assessment of potential therapeutic effects of adjunct osteopathic medicine for multidisciplinary care of acute and convalescent COVID-19 patients. Review article. Explore 2020; S1550- 8307(20)30306-2
44.HALM EA. et al. Time to clinical stability in patients hospitalized with community acquired pneumonia: implications for practice guidelines. JAMA 1998; 279:1452-1457.
45.METLAY JP. et al. Measuring symptomatic and functional recovery in patients with community-acquired pneumonia. Journal of General Internal Medicine 1997; 12: 423-430.
46.LAGUARDIA, J. et al. Brazilian normative data for the Short Form 36. Revista Brasileira de Epidemiologia volume.16 nº.4 São Paulo Dec. 2013.
47.HOLLIS SCF. What is meant by intention to treat analysis? Survey of published randomised controlled trials. BMJ. 1999 Sep 2011; 319(7211): 670-4.
12. ANEXOS
ANEXO A
TERMO DE CONSENTIMENTO LIVRE E ESCLARECIDO
Você está sendo convidado(a) a participar do projeto de pesquisa intitulado “Uso do TMO como tratamento adjuvante em pacientes hospitalizados com COVID-19 para diminuição de dias de internação e efeitos deletérios funcionais se comparado a utilização apenas de protocolo padrão. Um ensaio multicêntrico, randomizado e controlado.”, sob responsabilidade de Thiago Bento Ribeiro.
Este projeto tem como objetivo, verificar se o uso do TMO (Tratamento Manipulativo Osteopático) quando associado ao tratamento padrão em pacientes hospitalizados com COVID-19, diminui os dias de internação e minimiza os efeitos deletérios funcionais comparando o emprego desse tipo de terapêutica a aplicação apenas do protocolo padrão. Os participantes serão divididos, por sorteio, em três grupos. O(A) participante poderá ser selecionado para o grupo que será feito a intervenção do TMO associado ao tratamento padrão, para o grupo que irá receber uma intervenção simulada associado ao tratamento padrão, ou seja, que não terá os mesmos gestos manipulativos ou para o grupo que irá receber apenas o tratamento padrão. Abaixo seguem informações relacionadas aos procedimentos que serão realizadas neste projeto assim como informações adicionais:
1. A avaliação inicial será feita pelo médico responsável pela triagem dos pacientes. Nela será feito algumas perguntas e alguns exames clínicos para que seja feito o seu diagnóstico. Durante essa avaliação também será feito algumas perguntas para o preenchimento de dois formulários.
2. Após a distribuição dos pacientes, os que caírem no grupo que receberá o Tratamento Manipulativo receberão uma sequência de técnicas de terapia manual e associada à esse tratamento o mesmo receberá o tratamento convencional dado aos pacientes hospitalizados com COVID-19.
3. Os que caírem no grupo denominado controle receberão a mesma sequência de técnicas, porém de uma maneira simulada. Esses participantes também receberão o tratamento convencional.
4. Os participantes que caírem no terceiro grupo somente receberão o tratamento convencional dado aos pacientes de COVID-19.
5. Essa pesquisa auxiliará o entendimento sobre o potencial de ajuda que o Tratamento Manipulativo Osteopático poderá ter às complicações e nos efeitos deletérios funcionais desta doença tão pouco conhecida ainda.
6. Quaisquer dúvidas ou questionamentos poderão ser esclarecidos com o autor da pesquisa a qualquer momento.
7. A participação é voluntária, sem nenhum tipo de remuneração pela participação e você tem a liberdade de deixar o estudo a qualquer momento sem qualquer ônus.
8. A identidade e dados dos participantes serão mantidos em sigilo em relação a publicações futuras e armazenado em banco de dados sob a guarda do pesquisador responsável.
9. Os pacientes poderão se beneficiar com a diminuição do tempo de internação e dos efeitos deletérios deixados pela doença.
Ao assinar abaixo, você confirma que leu as afirmações contidas neste termo de consentimento, que foram explicados os procedimentos do estudo, que teve a oportunidade de fazer perguntas, que está satisfeito(a) com as explicações fornecidas e que autoriza sua participação voluntária neste estudo. Mesmo assim, novos esclarecimentos podem ser solicitados a qualquer momento, e sempre será possível retirar o seu consentimento em qualquer etapa da pesquisa, sem qualquer ônus.
Para quaisquer esclarecimentos pode ser feito contato com Thiago Bento Ribeiro, pelo e-mail: thiago.ribeiro@kynesis.com.br, ou pelo telefone (21) 98630-8476.
Este documento consiste em duas vias, sendo uma que fica com o pesquisador e a outra com o(a) participante.
Eu, ______________________________, declaro ter sido informado e concordo com a minha participação, como voluntária, no projeto de pesquisa acima descrito.
Rio de Janeiro, ____ de _______________ de ______.
ANEXO B