ANALYSIS OF ANTIMICROBIALS AND THE MICROBIOLOGICAL PROFILE OF PATIENTS HOSPITALIZED FOR COVID-19 IN AN INTENSIVE CARE UNIT
REGISTRO DOI: 10.5281/zenodo.10801148
Arenice Lucas Ramires1, Nixon Matheus de Carvalho Silva1, Rayllan Cezar da Silva Moreira1, Rosiane Morais de Souza2, Milthes Viana Guedes2, José de Oliveira da Silva3, Francisca Maria da Silva4, Francisco de Oliveira da Silva5, Cleonice de Macedo Lopes Silva6, Wendryus Willian de Lima7
RESUMO:
Em outubro de 2019, houve um grande quantitativo de infecções na cidade de Wuhan na China, levando a quadros de insuficiência respiratória, no início tratada como Influenza, logo percebeu-se que era de fácil contágio, afetando todo o mundo, o que levou em março de 2020 a declaração de pandemia mundial. A atual pandemia é causada pelo Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2), sua principal
característica é o acometimento respiratório pulmonar, infecções agudas ou severas, dependendo da gravidade o paciente pode apresentar, febre, coriza, sensação de aperto no peito, cansaço, fadiga e quadros de pneumonia, o que está relacionado diretamente às altas taxas de mortalidade. O que levou o mundo a viver um completo estado de isolamento, pois as taxas de contágios e mortalidade são muito altas. Com isso o uso de antibióticos
tornou-se opção, por ser uma doença desconhecida no mundo, não sabendo ao certo qual era o tratamento adequado para o contágio com rápida proliferação. O que levou a um questionamento, ” até quando o uso de antibióticos é um benefício à saúde, e a partir de qual momento seu uso exacerbado se torna um problema de saúde pública?”. Objetivo: Analisar o consumo de antimicrobianos utilizados por pacientes COVID-19 internados em umas unidades de terapia intensiva e inferir microrganismos prevalentes. Metodologia: Foi realizado um estudo de coorte observacional, retrospectivo e quantitativo, onde foi analisado os registros do consumo de antimicrobianos utilizados durante dois anos da COVID – 19, em pacientes adultos em uma unidade de terapia intensiva, correlacionando com os microrganismos identificados através de cultura microbiológica, em um período de março de 2020 a março de 2022.As buscas foram realizadas nas seguintes bases de dados para o
levantamento teórico da pesquisa: Scielo, PubMed. Para as buscas foram utilizadas diferentes combinações: “antimicrobianos”, “pandemia”, “insuficiência respiratória”, “antibióticos”, “Covid-19”. Resultados: Durante o período de estudo, foram identificados 28.979 antimicrobianos na qual 12.638 usados no ano de 2020, 12.621 em 2021 e 3.548 no ano de 2022, foram utilizados 42 antimicrobianos diferentes durante o período em estudo no
hospital. Considerações Finais: Os resultados obtidos são importantes, porque mostram que o uso indiscriminado de medicamentos pode levar a sérios problemas de saúde pública. Dessa forma espera-se que novos estudos sejam realizados para que haja conscientização quanto ao uso racional desses medicamentos, e a reeducação da saúde pública.
Palavras-chaves: COVID-19; Pandemia; Insuficiência Respiratória; Antibióticos; Saúde Pública.
ABSTRACT: In October 2019, there was a large number of infections in the city of Wuhan in China, leading to respiratory failure, at first treated as Influenza, it was soon realized that it was easily contagious, affecting the whole world, which led in March 2020 to the declaration of a global pandemic.The current pandemic is caused by the Severe Acute Respiratory Syndrome Coronavirus 2 ( SARS-CoV-2), its main characteristic is pulmonary respiratory involvement, acute or severe infections, depending on the severity the patient may present, fever, runny nose, feeling of tightness in the chest, tiredness, fatigue and pneumonia, which is directly related to high mortality rates.This has led the world to live in a complete state of isolation, as the rates of contagion and mortality are very high. With this, the use of antibiotics became an option, because it is an unknown disease in the world, not knowing for sure what was the appropriate treatment for the contagion with rapid proliferation.Which led to a question, “how long is the use of antibiotics a health benefit, and from what moment does their exacerbated use become a public health problem?”. Objective: To analyze the consumption of antimicrobials used by COVID-19 patients admitted to intensive care units and infer prevalent microorganisms. Methodology: An observational, retrospective and quantitative cohort study was conducted, where we analyzed the records of the consumption of antimicrobials used during two years of COVID-19, in adult patients in an intensive care unit, correlating with the microorganisms identified through microbiological culture, in a period from March 2020 to March 2022.The searches were performed in the following databases for the theoretical survey of the research: Scielo, PubMed. For the searches, different combinations were used: “antimicrobials”, “pandemic”, “respiratory failure”, “antibiotics”, “Covid-19”. Results: During the study period, 28,979 antimicrobials were identified in which 12,638 used in the year 2020 , 12,621 in 2021 and 3,548 in the year 2022 , were used 42 different antimicrobials during the period under study in the hospital. Final Considerations: The results obtained are important because they show that the indiscriminate use of medicines can lead to serious public health problems. Thus, it is expected that further studies will be conducted so that there is awareness about the rational use of these drugs, and the re-education of public health.
Keywords: COVID-19; Pandemic; Respiratory Failure; Antibiotics; Public health.
INTRODUÇÃO
O mundo vivenciou a primeira epidemia viral do século XXI quando um novo vírus respiratório, pertencente à família Coronaviridae , deixou de infectar apenas animais e passou a ter o ser humano como hospedeiro. [1] Os Coronavírus são vírus que causam infecções respiratórias em animais, incluindo aves e mamíferos. Contudo, apenas sete patógenos são conhecidos por infectar humanos. Os coronavírus sazonais na maioria das vezes estão relacionados a síndromes gripais. Nas últimas duas décadas, duas classes (Síndrome respiratória Aguda Grave – SARS e Síndrome Respiratória do Oriente Médio – MERS) dos Coronavírus foram diretamente relacionadas e os protagonistas das epidemias mais virulentas de síndrome respiratória aguda grave (SRAG), até então conhecidas e registradas. A epidemia de SARS que teve início em Hong Kong (China), em 2003, com letalidade de aproximadamente 10% e a MERS que teve surgimento na Arábia Saudita em 2012 com letalidade de cerca de 30 %. Esses vírus fazem parte da lista de doenças prioritárias para pesquisa no contexto de emergência. (2) A doença do Coronavírus 2019 ( COVID-19) causada pelo SARS-CoV-2 é considerada uma ameaça à saúde global com a capacidade de afetar a vida dos seres humanos em todos os âmbitos de sua existência. (3) Em outubro de 2019 , houve um grande quantitativo de infecções na cidade de Wuhan na China, levando a quadros de insuficiência respiratória, no início tratada como Influenza, logo percebeu-se que era de fácil contágio, afetando todo o mundo, o que levou em março de 2020 a declaração de pandemia mundial. A atual pandemia é causada pelo Severe Acute
Respiratory Syndrome Coronavirus 2 (SARS-CoV-2), sua principal característica é o acometimento respiratório pulmonar, infecções agudas ou severas, dependendo da gravidade o paciente pode apresentar, febre, coriza, sensação de aperto no peito, cansaço, fadiga e quadros de pneumonia, o que está relacionado diretamente às altas taxas de mortalidade. O que levou o mundo a viver um completo estado de isolamento, pois as taxas de contágios e mortalidade são muito altas. Com isso o uso de antibióticos tornou-se opção, por ser uma doença desconhecida no mundo, não sabendo ao certo qual era o tratamento adequado para o contágio com rápida proliferação. O que levou a um questionamento, ” até quando o uso de antibióticos é um benefício à saúde, e a partir de qual momento seu uso exacerbado se torna um problema de saúde pública?” Neste contexto, o presente estudo tem como objetivo avaliar e quantificar o uso de antimicrobianos, e comparar os resultados obtidos com os microrganismos combatidos com o número elevado de antibióticos usados durante o período do estudo em pacientes hospitalizados com COVID-19 em um hospital privado na cidade de Manaus-AM, que foi um epicentro da COVID-19 no Brasil. É uma pesquisa de um estudo de coorte observacional, retrospectivo e quantitativo, onde será analisado os registros de informações em prontuário eletrônico (MV – Sistemas) sobre o uso de antibióticos de pacientes graves a críticos com COVID-19, avaliando o quantitativo utilizados e correlacionando os microrganismos identificados e combatidos nesse período, onde será feito um comparativo durante a pandemia com o uso de antibióticos. Para assim poder alcançar dados sobre o seu uso em quadros de COVID-19, contribuindo assim para o uso racional de medicamentos, uma das maiores preocupações dos dias atuais.
O SARS-CoV é o agente causador de um quadro de pandemia a nível mundial desde o ano de 2020. É um vírus transmitido pelo ar, capaz de infectar diversas pessoas e causar sintomas de leves a graves em pacientes, com alta taxa de mortalidade. Com base nos relatos disponíveis e nos dados científicos relatados pela China, Itália e pelos Estados Unidos. (4). No dia 26 de fevereiro de 2020 registrou-se no Estado de São Paulo primeiro caso importado confirmado do Covid- 19, tratou-se de uma pessoa do sexo masculino, com 61 anos que havia realizado uma viagem à Itália. No dia 22 de março, todas as Capitais já haviam notificado casos confirmados do Covid19, 56 dias após o registro do 1000º caso, o número de infecções já havia aumentado 200 vezes mais, atingindo exatamente 233.143 casos. O primeiro registro de óbito no Brasil ocorreu apenas 20 dias após a confirmação do primeiro caso, no dia 17 de março de 2020. Ao passarem 29 dias quase todas as UFS já haviam registrado mortes, o último estado a registrar foi o Estado de Tocantins. No dia 20 de março foi decretado no país a transmissão comunitária, que teve como epicentro o Estado do Amazonas, com 2 picos elevados de pandemia (4.746,6/1 milhões) de casos confirmados. (5) A região Norte exibiu uma das maiores taxas de incidências. O Estado do Amazonas foi o epicentro brasileiro durante a pandemia, tendo o índice de casos, confirmados e suspeitos elevadíssimos, durante a primeira e segunda onda pandêmica, assim denominado pela OMS, onde houve um colapso no sistema de saúde do Estado, e uma crise no sistema funerário da capital, gerando, falhas no sistema de saúde, bem como o item de suma importância que foi a escassez de oxigênio. Uma das maiores dificuldades encontrada tanto pelo sistema de saúde como pelo 5 governo, foi a aceitação populacional quanto ao isolamento voluntário, a rigidez da população em isolar-se acarretou ainda mais o sistema de saúde, onde houve superlotação dos hospitais tanto públicos quanto particulares. As UTIs ficaram com excesso de lotação, filas de espera por leitos e atendimento básico deixou o Estado com colapso total. (5) A Resistência a Antimicrobianos (denominada, AMR, da sigla em inglês) na atualidade é considerada um dos grandes problemas sem solução prévia para a saúde pública mundial. A estimativa é que aproximadamente quatro milhões de pessoas são acometidas, anualmente, por infecções, tendo associação direta a cuidados de saúde na União Europeia (UE), e que cerca de 37.000 indivíduos em decorrência venham a óbito ocasionada diretamente às infecções resistentes adquiridas dentro dos ambientes hospitalares. Cerca 67,6% dessas mortes são provocadas por bactérias multirresistentes a antibióticos. Segundo a Organização Mundial da Saúde ( OMS), a definição de AMR é caracterizada quando os micro-organismos têm a capacidade (bactérias, fungos, vírus e parasitas) de sofrer mutação quando expostos a antimicrobianos, gerando variantes, logo criando resistência a esses medicamentos, tornando-os ineficazes. Contudo, muitas vezes o termo em questão é exemplificado pelo caso dos antibióticos utilizados em infecções bacterianas.(6) Às doenças infecciosas são combatidas com a utilização de antimicrobianos, sendo o seu uso adequado uma das principais preocupações mundiais.(4) Contudo, vale ressaltar que, os antimicrobianos têm apresentado papel importante na gestão da pandemia, apesar de que, Covid-19 e RAM podem colidir um ao outro, pois há um impulso para recorrer aos antimicrobianos existentes em pacientes com Covid-19 gravemente enfermos na ausência de tratamentos específicos, enquanto as tentativas de controlar a disseminação de Covid19 também podem levar a uma redução da resistência antimicrobiana.(7) No entanto, a falta de evidências de alta qualidade para essa situação e o ritmo constante de novas informações e conflitos têm sido um desafio geral para todas as especialidades médicas, inclusive a terapia intensiva. O uso exacerbado dos antibióticos leva a sérios danos à saúde do paciente, quanto à resistência de antimicrobianos em microrganismos, tendo em vista que uma grande preocupação é a saúde pública. A descoberta dos antimicrobianos na década de 30 e a sua posterior utilização em larga escala no combate às doenças infecciosas geraram no início uma euforia na comunidade científica, que acreditava ter encontrado a solução contra as infecções bacterianas. Os medicamentos ocupam um importante papel nos sistemas de saúde, pois podem aumentar a expectativa de vida, erradicar certas doenças e trazer benefícios sociais e econômicos. (8). Verificou-se desde o início da pandemia que o uso de antimicrobianos foi feito sem critérios precisos, vale ressaltar que já existem a mais de cinco décadas, estudos comparativos comprovando o uso indiscriminado desses tratamentos. Sabendo que, utilização sem os devidos critérios de qualquer medicamento, podem vir a ter sérias consequências até mesmo irreversíveis, 6 como podemos exemplificar, o efeito terapêutico sem a devida eficácia esperada, reações adversas, dependência farmacológicas, resistência bacteriana, a qualidade de vida dos pacientes e familiares é afetada diretamente sendo reduzida drasticamente, o aumento da morbidade, da mortalidade e consequentemente, dos custos da atenção à saúde, até mesmo podendo levar em caso extremo ao óbito desse paciente em tratamento.(8) Os hospitais sendo a porta de entrada e saída de pacientes com uma grande diversidade de microrganismos contaminantes, torna-se um dos locais mais propícios para a seleção e disseminação de cepas microbianas resistentes, tornando-se dentre muitos um dos locais mais propício existente, se pararmos para realizar uma análise minuciosa na maioria das vezes há mais de um agente antimicrobiano, sendo disseminado de uma única só vez em um mesmo ambiente hospitalar, especialmente nas Unidades de Terapia Intensiva ( UTI), onde é um local propício para essa troca de agentes etiológicos entre os pacientes. Tal fato se dá por uma combinação de fatores pré-existentes como é o caso de pacientes imunocomprometidos, o uso contínuo de antimicrobianos e ocorrência de infecções e reinfecções hospitalares por bactérias patogênicas altamente resistentes. (8)
OBJETIVOS
1 .Geral
– Analisar o consumo de antimicrobianos utilizados por pacientes COVID-19 internados em umas unidades de terapia intensiva e inferir microrganismos prevalentes.
2 .Específico
– Avaliar o uso de antimicrobianos em pacientes com COVID-19.
– Descrever fatores associados ao aumento do consumo de antimicrobianos em UTI durante a pandemia.
-Levantar microrganismos correlacionados aos antimicrobianos de maior consumo.
METODOLOGIA
1. Delineamento experimental
Foi realizado um estudo de coorte observacional, retrospectivo e quantitativo, onde foi analisado os registros do consumo de antimicrobianos utilizados durante dois anos da COVID – 19, em pacientes adultos em uma unidade de terapia intensiva, correlacionando com os microrganismos identificados através de cultura microbiológica, em um período de março de 2020 a março de 2022.
As buscas foram realizadas nas seguintes bases de dados para o levantamento teórico da pesquisa: Scielo, PubMed. Para as buscas foram utilizadas diferentes combinações: “antimicrobianos”, “pandemia”, “insuficiência respiratória”, “antibióticos”, “Covid-19”.
2 . Critérios de inclusão e exclusão
Para seleção do material analisado foi considerado pacientes maiores de 18 anos internados com COVID- 19 de grave a crítico, com confirmação por RT-PCR ou teste sorológico específico, com terapia antimicrobiana; sendo excluídos: Pacientes com tempo de permanência no hospital menor que 24 horas não configurando necessidade de internação hospitalar, paciente transferido para outra unidade impossibilitando seguimento intra hospitalar, insuficiência de dados no prontuário que não permitam a avaliação completa.
3. Aspectos éticos
Este estudo compõe o projeto FOLLOW COVID-19 que foi submetido ao comitê de ética em pesquisa CAAE: 52104121.9.0000.0042, número parecer: 5.112.830 2 em pesquisa de seres humanos da Faculdade Adventista da Bahia – FADBA, e também foi submetido a anuência ao Núcleo de Ensino e Pesquisa em Saúde ( NEPS) – do Hospital Adventista de Manaus – HAM e aprovado para pesquisa na instituição.
4 . Procedimento metodológico
O material selecionado foi analisado inicialmente a partir de títulos e resumos em artigos científicos para embasamento teórico, após aprovação do NEPS foi feita uma análise em formato de planilhas de antimicrobianos utilizados durante os anos de estudos. Na qual foi analisado o uso de antimicrobianos utilizados para pacientes internados diagnosticados com COVID-19 em UTI e correlacionando com as culturas dos microrganismos identificados.
5 . Análise de dados
Os dados analisados em abril de 2023 pelo GPAF do HAM responsável pela análise terapêutica, e os pesquisadores juntamente com a responsável farmacêutica Rosiane Moraes de Souza e Milthes Viana Guedes, mediante consulta ao consumo de antimicrobianos no período de março de 2020 a março de 2022. Onde foi avaliado em prontuário eletrônico dos pacientes as culturas positivas quando existentes. Posteriormente, foi feita a checagem dos critérios de inclusão e exclusão.
Foi utilizado uma planilha no programa Excel, a saber: dados sociodemográficos do paciente ( sexo, idade, IMC), variáveis da hospitalização ( dias de internação, dias de doença na internação, dias livres de ventilação mecânica, alta hospitalar, reinternação) antecedentes e/ou condições clínicas (fatores de risco relacionados a comorbidades Cardiopatia/ Asma/ doença pulmonar obstrutiva crônica ( DPOC) / Hipertensão/ Diabetes/ Obesidade), medicamentos, cultura positiva.
RESULTADOS E DISCUSSÃO
Durante o período de estudo através das análises de prontuários selecionamos de março de 2020 a março de 2022, foram identificados 28.979 antimicrobianos na qual 12.638 usados no ano de 2020, 12.621 em 2021 e 3.548 no ano de 2022. Com o quantitativo de 42 antimicrobianos diferentes utilizados durante o período em estudo no hospital, conforme mostra a figura 1.
Figura 1: Gráfico geral dos antimicrobianos dos anos de 2020 a 2022.
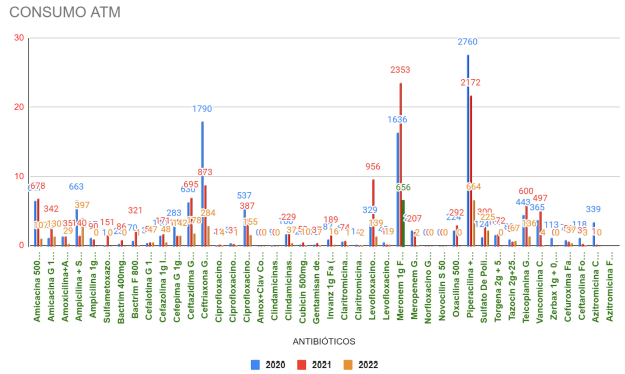
Fonte: Autores, 2023
A utilização de antimicrobianos
Segundo Nieuw Laat, durante o período pandêmico pela Covid-19 a utilização em grande escala de antimicrobianos pode ter sido responsável pelo aumento de resistência antimicrobiana (RAM). Contudo, de acordo com Organização Mundial da Saúde (2021), muito antes da pandemia de COVID-19, a resistência aos antimicrobianos (RAM) já era reconhecida como uma importante emergência mundial, responsável por cerca de 700.000 mortes a cada ano.
Ainda de acordo com a OMS (2021), há previsão de que ocorra 10 milhões de mortes por ano até 2050 devido à RAM.
Esse cenário preocupante da pandemia só foi possível, devido a busca desordenada e desenfreada por tratamentos e profilaxias contra a coronavírus em questão, onde houve um aumento considerável na utilização de tratamentos que não apresentaram efetividade comprovada cientificamente ou possuem indicação farmacológica descrita. (9)
O uso irracional da farmacoterapia durante o COVID-19
Contudo, vale ressaltar que, os antimicrobianos têm apresentado papel importante na gestão da pandemia, apesar de que, Covid-19 e RAM podem colidir um ao outro, pois há um impulso para recorrer aos antimicrobianos existentes em pacientes com Covid-19 gravemente enfermos na ausência de tratamentos específicos, enquanto as tentativas de controlar a disseminação de Covid-19 também podem levar a uma redução da resistência antimicrobiana (7).
Conforme Marinho et al. (10) , nas unidades de tratamento intensivo, é onde se detém a maior densidade de consumo de antimicrobianos, estimando-se que em 50% das vezes a prescrição é desnecessária ou incorreta. Esta situação afeta não só o paciente, mas também interfere na ecologia microbiana de todo o ambiente hospitalar e limita as opções terapêuticas, uma vez que o consumo abusivo de antimicrobianos induz uma pressão seletiva e consequente seleção de microrganismos resistentes. O uso exacerbado de antimicrobianos pela população tem sido um dos maiores desafios para o uso racional e controle da RAM, e provavelmente uma boa parte dessa responsabilidade possa recair sobre a dificuldade de entendimento e seguimento das prescrições médicas pelos usuários (11). Na tabela 1 demonstra o uso de antimicrobianos para cada ano de estudo. No ano de 2020 dentre os números de antimicrobianos o mais utilizado foi a piperacilina + tazobactam com 2.760 na qual é indicada para o tratamento de algumas infecções bacterianas, sendo elas: Infecção do aparelho respiratório inferior (pneumonias). Infecções das vias urinárias, infecções generalizadas bacterianas ( sepse) dentre outras. No ano de 2021 temos um grande avanço na utilização do Meropenem 1g com 2.353 na qual é indicado para o tratamento de infecções causadas por uma única ou múltiplas bactérias. No entanto, até março de 2022 voltamos a ter a piperacilina + tazobactam como a com mais crescente uso com 664 neste ano, conforme a figura 2.
Figura 2: Consumo dos antimicrobianos mais usados no período de estudo.
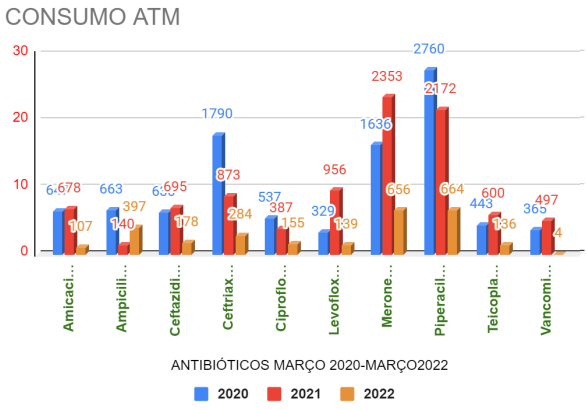
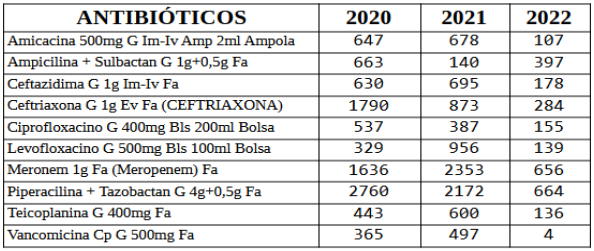
Tabela 1: Consumo de antimicrobiano utilizado por ano.
O Perfil microbiológico dos antimicrobianos.
Durante o estudo dos antimicrobianos mais utilizados observou-se que a piperacilina por sua vez teve uma utilização mais elevada durante o período de março de 2020 a março de 2022. É indicada para o tratamento de infecções bacterianas sistêmicas ou locais, causadas por microrganismos gram-positivos e gram-negativos aeróbios e anaeróbios sensíveis à esses antibióticos, ela exerce sua atividade bactericida pela inibição da formação do septo e da síntese da parede celular, qual tem seu metabolismo parcialmente hepático. A piperacilina é transformada no metabólito desetil com atividade microbiológica pequena. O tazobactam é metabolizado em um único metabólito microbiologicamente inativo. Essa combinação é altamente ativa contra microorganismos das bactérias Gram-negativas: Cepas produtoras e não produtoras de beta-lactamase de: Escherichia coli, Citrobacter spp.
O meropenem, por sua vez, foi o segundo mais prescrito e é um carbapenêmico de amplo espectro, prescrito e usado nas terapias de infecções graves de pacientes adultos internados nas unidades da UTI, causadas por patógenos Gram-negativos susceptíveis. O meropeném tem ação bactericida interferindo com a síntese da parede celular bacteriana. A facilidade com que penetra nas células bacterianas, seu alto nível de estabilidade à maioria das serinas betalactamases e sua grande afinidade pelas múltiplas Proteínas Ligantes de Penicilina ( PBPs) o que faz com que seja uma potente atividade bactericida de meropeném contra um amplo espectro de bactérias aeróbicas e anaeróbicas.
O antibiótico Sulbactam sódico + ampicilina é indicado em infecções causadas por microrganismos suscetíveis, tendo a combater tanto os patógenos gram positivos quanto as gram negativas.
Ceftazidima pode ser prescrito, quando se suspeita da presença de Bacterioides fragilis. Por causa de seu amplo espectro de ação, especialmente contra agentes gram-negativos, está também indicado nas infecções resistentes a outros antibióticos , incluindo aminoglicosídeos e cefalosporinas diversas.
A ceftriaxona é um tipo de antibiótico capaz de eliminar grandes microorganismos/bactérias gram negativas responsáveis por vários tipos de infecções, durante todo o tratamento deve sempre ficar sendo verificado as reações durante a administração do medicamento.
O ciprofloxacino, componente ativo de Cipro, para o tratamento de infecções complicadas e não complicadas causadas por microrganismos sensíveis a este antibióticos, as infecções causadas por bactérias gram negativas. As bactérias gram-negativas, Acinetobacter baumannii , Pseudomonas aeruginosa, Escherichia coli e Klebsiella pneumoniae estão associadas a infecções nosocomiais, incluindo infecções do trato urinário, infecções da corrente sanguínea, infecções associadas a cateter e pneumonia associada à ventilação mecânica.
Levofloxacino é eficaz contra uma série de bactérias Gram-positivas e Gram-negativas, como: Staphylococci, Streptococci incluindo Pneumococci, Enterobacteriaceae, Haemophilus influenzae, bactérias Gram-negativas não fermentativas e micro-organismos atípicos. Devido a seu amplo espectro de ação, a levofloxacina é prescrita para uma ampla gama de infecções onde o agente causal é desconhecido.
Sulfato de Amicacina é indicado para o tratamento a curto prazo de infecções graves causadas por cepas sensíveis de bactérias Gram negativas, como por exemplo: Pseudomonas sp., Escherichia coli, Proteus sp. indol-positivo e indol-negativo, Providencia sp., Klebsiella sp.,Enterobacter sp., Serratia sp. e Acinetobacter sp. (que era chamada anteriormente de Mima-Herelle ).Também é indicada para bacteremia e septicemia em infecções graves do trato respiratório, ossos e articulações, sistema nervoso central (incluindo meningite), pele e tecidos moles, infecções intra-abdominais ( incluindo peritonite), queimaduras e infecções pós-operatórias ( incluindo pós-cirurgia vascular).Eficaz também contra infecções recorrentes complicadas e graves do trato urinário causadas por estas bactérias. Pode vir a ser introduzido como terapia de suspeita de infecção por Gram-negativos como também é eficaz contra cepas de Gram-negativos resistentes a gentamicina e/ou tobramicina, particularmente Proteus rettgeri, Providencia stuartii, Serratia marcescens e Pseudomonas aeruginosa.
A teicoplanina é indicada contra infecções causadas por bactérias gram-positivas sensíveis, incluindo aquelas resistentes a outros antibióticos tais como meticilina e as cefalosporinas: endocardite, septicemia, infecções osteoarticulares, infecções do trato respiratório inferior, infecções de pele e tecidos moles, infecções urinárias e peritonite associada à diálise peritoneal crônica ambulatorial. Indicada ao tratamento de infecciosos em pacientes alérgicos às penicilinas ou cefalosporinas. Pode ser usada contra colite pseudomembranosa causada por Clostridium difficile .
A vancomicina é um medicamento antibacteriano da classe dos glicopeptídeos tricíclicos. Em doses adequadas promove a morte das bactérias. A vancomicina é indicada para o tratamento de infecções graves causadas pela bactéria Staphylococcus aureus resistente a antibióticos betalactâmicos (ex.: penicilinas ou cefalosporinas). Indicada para tratar infecções causadas por outras bactérias suscetíveis em pacientes alérgicos a antibióticos beta lactâmicos ( ex.: penicilinas ou cefalosporinas) ou que não responderam a outros tratamentos. A vancomicina é indicada para o tratamento de infecção óssea, septicemia ( infecção no sangue), infecção do trato respiratório inferior ( pneumonia), infecção na pele e estruturas da pele. É indicada também para o tratamento e prevenção de endocardite ( infecção das válvulas do coração).
O aumento da resistência a vários antibióticos leva a condições graves de risco de vida e resulta a um grande desafio no tratamento de infecções bacterianas Gram-negativas. Além disso, o surgimento de bactérias Gram-negativas multirresistentes ( MDR) aumenta o índice de desafios do tratamento e aumenta ainda mais a morbidade e a mortalidade de pacientes internados.(12) A maior parte das bactérias é inofensiva e até residem no corpo humano e contribui de forma positiva para a sobrevivência, pois realizam algumas funções importantes para o corpo como a produção de enzimas, degradação de produtos tóxicos e atuam na modulação do sistema imune do hospedeiro. Contudo algumas espécies são patogênicas e causam muitos prejuízos (13). As bactérias resistentes mais frequentes são: Escherichia coli, Staphylococcus aureus e Streptococcus pneumoniae (7). Durante o estudo foi possível observar a proliferação das bactérias gram-negativas como Enterobacteriaceae, Pseudomonas com até mesmo Staphylococcus aureus, dentro outras. Os órgãos mais acometidos foram os pulmões, trato urinário, como também acometimentos cutâneos, conforme a tabela 2.
Tabela 2: Quadro de antibióticos e seus patógenos combatentes.
ANTIBIÓTICOS Gram+ Gram- PATÓGENOS Amicacina x Pseudomonas sp., Escherichia Coli, Proteus sp. Providencia spp., Klebsiella-Enterobacter- Serratia sp., Acinetobacter sp. Ampicilina + Sulbactam x x Gram-positivas; Staphylococcus (aureus, epidermidis s saprophyticus),Streptococcus (pneumoniae e pyogenes) e Enterococcus faecalis; gram-negativas como Haemophilus influenzae, Moraxella catarrhalis, Escherichia coli, Klebsiella, Proteus mirabilis, Acinetobacter, Enterobacter, Neisseria gonorrhoeae. ANTIBIÓTICOS Gram+ Gram- PATÓGENOS Ceftazidima x pseudomonas aeruginosa, Pseudomonas sp., Klebsiella pneumoniae, Klebsiella sp., Proteus mirabilis, Proteus vulgaris, Morganella morganii ( Proteus morganii), Proteus rettgeri, Providencia sp., Escherichia coli, Enterobacter sp., Citrobacter sp., Serratia sp., Salmonella sp., Yersinia enterocolitica, Pasteurella multocida, Acinetobacter sp., Neisseria gonorrhoeae, Neisseria meningitidis, Haemophilus influenzae ( incluindo cepas resistentes à ampicilina) e Haemophilus parainfluenzae. Ceftriaxona x Haemophilus influenzae, Moraxella catarrhalis, a maioria das Escherichia coli, Klebsiella pneumoniae, Morganella, Neisseria, Proteus, Enterobacter sp., Serratia marcescens e Acinetobacter sp. Streptococcus pneumoniae. O Staphylococcus epidermidis, outros estafilococos coagulase-negativos, Staphylococcus aureus. Ciprofloxacino x Klebsiella, Enterobacter, Proteus, E. coli, Pseudomonas, Haemophilus, Moraxella, Legionella e Staphylococcus Levofloxacino x x Staphylococci, Streptococci incluindo Pneumococci, Enterobacteriaceae, Haemophilus influenzae, bactérias Gram-negativas não fermentativas e micro-organismos atípicos. Meropenem x Escherichia coli, klebsiella sp, Proteus sp. piperacilina + Tazobactam x x Gram-negativas: Escherichia coli, Citrobacter spp. ( incluindo C. freundii, C. diversus), Klebsiella spp. ( incluindo K. oxitoca, K. pneumoniae), Enterobacter spp. ( incluindo E. cloacae, E. aerogenes), Proteus vulgaris, Proteus mirabilis, Providencia rettgeri, Providencia stuartii, Plesiomonas shigelloides, Morganella morganii, Serratia spp . ( incluindo S. marcescens, S. liquefaciens), Salmonella spp., Shigella spp., Pseudomonas aeruginosa e outras Pseudomonas spp. ( incluindo P. cepacia, P. fluorescens), Xanthomonas maltophilia, Neisseria gonorrhoeae, Neisseria meningitidis, Moraxella spp. ( incluindo Branhamella catarrhalis), Acinetobacter spp., Haemophilus influenzae, H. parainfluenzae, Pasteurella multocida, Yersinia spp., Campylobacter spp., Gardnerella vaginalis. Gram-positivas: Cepas produtoras e não produtoras de beta-lactamase de: estreptococos (S. pneumoniae, S. pyogenes, S. bovis, S. agalactiae, S. viridans, Grupo C, Grupo G), enterococos ( E. faecalis, E. faecium), Staphylococcus aureus (S. aureus não resistente à meticilina), S. saprophyticus, S. epidermidis (estafilococos coagulase-negativo), Corynebacteria, Listeria monocytogenes, Nocardia spp. Teicoplanina x Staphylococcu s, Clostridium difficile Vancomicina x Staphylococcus aureus, Enterococcus faecalis, Streptococcus pneumoniae.
Fonte: Autores, 2023
CONCLUSÃO
O presente estudo identificou um aumento de administração de antibióticos quando comparado aos períodos anteriores à pandemia COVID -19 , houve um aumento de prescrição considerável durante o período em questão. Pode-se observar que a falta de conhecimento do patógeno e o desespero e o peso de uma pandemia, ocasionou esse uso exacerbado.
Houve a falta de cautela do parte do prescritor, que mesmo antes de saber qual patógeno o paciente foi acometido, já prescrevia, em uma tentativa de evitar uma reinfecção, ou até mesmo a piora desse paciente. Até porque o COVID-19 alterava todo o sistema imunológico do paciente levando à uma verdadeira confusão
para um diagnostico preciso. Com isso estima-se que esse uso descontrolado de antibióticos poderá
trazer sérios problemas à saúde pública a curto ou longo prazo, visto que muitas bactérias que antes estavam
adormecidas, foram e estão sendo ativadas por não haver antibióticos com tanta eficácia como antes no
sistema de saúde. Com isso a propagação de doenças que antes eram tratadas com antibioticoterapia, esses mesmos antibióticos não possuem mais a mesma sensibilidade a qual se é esperada.
Os resultados obtidos são importantes, porque mostram que o uso indiscriminado de medicamentos pode levar a sérios problemas de saúde pública. Dessa forma espera-se que novos estudos sejam realizados para que haja conscientização quanto ao uso racional desses medicamentos, e a reeducação da saúde pública.
REFERÊNCIAS
1. Souza Layse Costa de. SARS-CoV, MERS-CoV e SARS-CoV-2: uma revisão narrativa dos principais Coronavírus do século. SARS-CoV, MERS-CoV e SARS-CoV-2: a narrativa review of the main Coronaviruses of the century. 2021
Jan 14;
2. Lana, R. M. et al. Emergência do novo coronavírus (SARS-CoV-2) e o papel de uma vigilância nacional em saúde oportuna e efetiva. Cadernos de Saúde Pública, v. 36, n.3, p. 19-20, 1 abri. 2020.
3. Cespedes, M. S.; Souza, J. C. R. P. Coronavírus: a clínica update of Covid-19. Revista da Associação Médica Brasileira (1992), v. 66, n. 2, p. 116-123, 7 mai. 2020.
4. Rodrigues, F. d’A.; Bertoldi, A. D. Perfil da utilização de antimicrobianos em um hospital privado. Ciência e Saúde coletiva, v.15, p. 1239-1247, 2 jun. 2008.
5. Cavalcante João Roberto, et al. COVID-19 no Brasil: evolução da epidemia até a semana Revista epidemiológica 20 de 2020. Científica Multidisciplinar, , COVID-19 no Brasil: evolução da epidemia até a semana epidemiológica 20 de 2020. 20 Apr 29;
6. Silva, R. A. et al. Resistência a Antimicrobianos: a formulação da resposta no âmbito da saúde global. Saúde em Debate, v. 44, n. 126, p. 607-623, 12 fev. 2020.
7. Mesquita, R.F.; et al. Uso racional de antimicrobianos e impacto no perfil de resistência microbiológica em tempos de pandemia pela Covid-19. Research, Society and Development, v. 11, n. 1, p.111, 6 mar. 2022
8. Souza, F. C. Baroni, M. M. F. Rosene, F. M. Perfil da utilização de antimicrobianos na unidade de terapia intensiva de um hospital público. Revista Brasileira de Farmácia Hospitalar e Serviços de Saúde, v. 8, n. 4, p. 37-44, 12 nov. 2017.
9. MARINHO, L.S.S.; PAZ, F.A.N. Consequências do uso indiscriminado de medicamentos como prevenção do COVID-19: revisão integrativa. Revista Científica Multidisciplinar, v. 2, n. 10, p. 886-887,5 jun. 2021.
10. Marinho, M.G.; et al. Estudo de consumo de antimicrobianos do Centro de Terapia Intensiva de um hospital universitário da Região Norte. Research, Society and Development, v. 11, n. 5, p.115, 3 jan. 2022.
11. MACHADO, O. V. O. et al. Antimicrobianos: revisão geral para graduandos e generalistas. EdUnichristus,[s.l.]. 2 nov. 2019.
12. Wu Xiuji, et al. Temporal association between antibiotic use and resistance in Gram-negative
bacteria. Associação temporal entre o uso de antibióticos e resistência em bactérias gram-negativas. 2021 Jan 01;
13. BAPTISTA, M. G. F. M. Mecanismos de resistência aos antibióticos. Dissertação (Mestrado em Ciências Farmacêuticas) – Universidade Lusófona de Humanidades e Tecnologia, Lisboa. p. 51. 2013.
1Biomédico(a) pelo Centro Universitário do Norte – UNINORTE.
2Farmacêutica no Hospital Adventista de Manaus-AM.
3Doutorando em Música e Educação pela Integralização de Crédito na Integralize – Santa Catarina.
4Doutoranda em Neuropedagogia pela Integralização de Crédito na Integralize – Santa Catarina.
5Doutorando em Psicologia pela Integralização de Crédito na Integralize – Santa Catarina.
6Graduanda em Enfermagem-Centro Universitário Tabosa de Almeida. Caruaru-PE.
7Acadêmico de Medicina – ULBRA
