REGISTRO DOI: 10.5281/zenodo.10570217
Paulo André Freire Magalhães1; Layanne Damasceno Silva Veloso1; Thaynara Cavalcanti Lima1; Lucas de Oliveira Silva1; Roberto Robe Gomes Santos1; Gustavo Alves Silva1; Esther Miranda Cardoso1; Héllen Vivianny Barros da Silva Sá1; Anne Karoline de Carvalho Nunes1; Isla Vargas Viana Santana1; Liz Romão2
RESUMO
Introdução: O uso de naltrexona em baixas doses (LDN) como terapia integrativa para pacientes com câncer vem sendo discutido com hipótese de possibilidade de prolongar a vida de pacientes oncológicos. Objetivo: Mapear na literatura corrente, evidências sobre o uso da LDN em pacientes oncológicos. Métodos: Esta revisão de escopo foi desenvolvida com base nas recomendações do guia internacional Preferred Reporting Items for Systematic reviews and Meta-Analyses extension for Scoping Reviews (PRISMA-ScR). Buscas de artigos abordando o uso de LDN em paciente oncológicos foram realizadas entre setembro e outubro de 2023. A busca da produção científica foi feita nas bases de dados MEDLINE (via PubMed), LILACS (via Biblioteca Virtual em Saúde) e google scholar. Resultados: 5 artigos do tipo relatos de caso foram incluídos nessa revisão. Nenhum estudo com delineamento mais robusto (ex.: prospectivos, longitudinais e ensaios clínicos) foram identificados. A idade dos pacientes variou de 46 a 80 anos, totalizando sete pacientes, sendo cinco do sexo masculino. Os diagnósticos de câncer diferiram entre os casos, a maioria apresentou metástase em alguma região do corpo e prognóstico restrito. A dose de LDN utilizada dos estudos variou de 3 a 4,5 mg dia, administrada via oral, com posologia diária ou 2 vezes por semana, com uso isolado ou como parte de um protocolo integrativo. Nenhum efeito tóxico foi relatado e todos os autores relataram aumento da sobrevida dos pacientes habitualmente considerados terminais. Conclusão: A terapia integrativa com LDN parece ser promissora para o tratamento de pacientes oncológicos, dada a sua falta de toxicidade, a sua pronta disponibilidade e o seu efeito nos pacientes relatados. Sua eficácia, no entanto, merece investigação mais aprofundada em ensaios controlados.
Palavras-chave: sintomas cancerínicos, antineoplásicos, protocolos de tratamento de câncer, naltrexona.
INTRODUÇÃO
A Naltrexona é um análogo sintético da oximorfona e antagonista não seletivo opioide. Foi produzida pela primeira vez no ano de 1962 e é utilizada originalmente no tratamento de dependência ao álcool e opioides. A Administração de Alimentos e Medicamentos (FDA) dos Estados Unidos liberou seu uso em doses diárias de 50 mg a 100 mg para essa finalidade, mas a partir do ao de 1980, diversos estudos foram desenvolvidos sobre o medicamento e os efeitos da Naltrexona em baixas doses (LDN), que se refere ao seu uso em doses abaixo de 10mg, no tratamento do câncer e na replicação celular com resultados promissores. Contudo, o FDA não reconhece oficialmente o uso da naltrexona em doses reduzidas para essas condições, tornando a prescrição desse tratamento “off-label”, que significa em doses não previstas na bula do medicamento, baseando-se no estudo e na experiência do médico. (GUIMARÃES, et al, 2023).
O câncer representa um dos maiores desafios em termos de saúde pública mundial, sendo uma das principais causas de morte e um obstáculo significativo para o aumento da expectativa de vida. O impacto do câncer, tanto em termos de novos casos, quanto de óbitos, cresce em todo o mundo e isso se deve principalmente às transições demográficas e epidemiológicas presentes na sociedade. (SUNG, et al, 2021).
Nesse contexto, o processo de envelhecimento da população, as mudanças nos hábitos de vida e no ambiente, incluindo transformações estruturais que afetam a mobilidade, o lazer, a alimentação e a exposição a poluentes ambientais, contribuem para o aumento da sua ocorrência. Do ano de 2013 a 2023, houve um aumento de 20% na sua incidência e espera-se que, para 2030, ocorram mais de 25 milhões de novos casos no Brasil. Para o triênio 2023-2025, estima-se 704 mil casos novos. (SANTOS, et al, 2023).
Diante disso, descobertas a respeito do câncer, principalmente relacionadas à resposta imunológica do paciente contra células cancerosas, têm servido como base para novos tratamentos envolvendo a imunomodulação. O sistema imunológico atua não só na prevenção da doença, ao destruir células anômalas precursoras do câncer, mas também como barreira para a sua progressão e disseminação. (ROCHA, 2014).
Evidências mostram que terapias que atuam direta ou indiretamente na regulação do sistema imune podem auxiliar no tratamento da doença. Uma dessas terapias é com a utilização do LDN, que é a sigla para Low Dose Naltrexone, que se refere ao uso dessa medicação a níveis abaixo de 10 mg por dia (baixas doses). Contudo, sua prescrição é feita fora da bula (off-label), haja vista, a administração demonstrou possíveis benefícios em pacientes com diferentes condições de saúde (GUIMARÃES, et al, 2023).
A Naltrexona é um antagonista opióide ativo, com propriedades primordiais no tratamento de dependência à álcool e opióides, entretanto, têm ganhado visibilidade por suas promissoras propriedades anti-inflamatórias e no tratamento de câncer, justificadas por seu mecanismo imunomodulador e anticancerígeno. (BERKSON; RUBIN, 2007) Estudos têm evidenciado que a LDN aumenta o número e densidade de receptores opiáceos em membranas tumorais, contribuindo para indução de apoptose destas células, além disso, seu uso em baixas doses mostrou aumento e densidade de células de grande importância para o controle da carcinogênese, como células T, e Natural killer (NK), além de barrar a angiogênese. (BERKSON; RUBIN, 2007)
Em experimento realizado em humano, por Berkson e cols. (2006) mostrou reversão de sinais e de linfoma de células B apenas com uso de LDN em baixas doses, bem como, o aumento da sobrevivência a longo prazo, de um paciente com câncer de pâncreas com metástase hepática, via administração intravenosa. (BERKSON; RUBIN, 2010)
Dado que o receptor opioide é considerado um fator de risco para carcinogênese e metástase, sua inibição com uso de Naltrexona, conhecida também como nalmefeno, indicaram consistência na redução da potencialidade do câncer colorretal como através da inibição da viabilidade e migração das células CT26 e regulação negativa da expressão da calmodulina, de CaMK II, inibindo assim a via AKT-GSK-3β e a glicólise das células CT26. (WU et al., 2018)
Outro dado que reforça a potencialidade do uso da Naltrexona em baixas doses, também nomeada como metilnaltrexona, foi o aumento da sobrevida em pacientes com câncer avançado, em ensaios randomizados. Assim como, estabilização da progressão em pacientes com de câncer de próstata. (DALGLEISH; LIU, 2022)
São diversos os tipos de cânceres tratados, com desfechos exitosos após o uso de naltrexona em baixas doses, resultados como esses, trazem à luz, a necessidade de explorar, compreender e compilar sua potencialidade bem como, suas aplicabilidades. Esse estudo teve como objetivo mapear na literatura corrente, evidências sobre o uso da LDN em pacientes oncológicos.
MÉTODOS:
Trata-se de uma revisão de escopo que consiste em sintetizar as evidências de pesquisas, para mapear a literatura existente de determinado assunto e identificar os principais conceitos, teorias, fontes e lacunas de conhecimento, através de uma abordagem sistemática (Tricco et al. 2018). Esta revisão teve o protocolo de pesquisa registrado no Open Science Framework no dia 09 de outubro de 2023 (https://osf.io/6mshp/) e foi desenvolvida com base nas recomendações do guia internacional Preferred Reporting Items for Systematic reviews and Meta-Analyses extension for Scoping Reviews (PRISMA-ScR) (Tricco et al. 2018), utilizando-se as nove etapas do método proposto pelo Instituto Joanna Briggs (JBI) (JBI, 2014).
Para orientar a formulação da questão norteadora, adotou-se a estratégia População, Conceito e Contexto (PCC) com a seguinte pergunta: quais as evidências científicas sobre o efeito da naltrexona em baixas doses (LDN) associado ao tratamento convencional na imunomodulação em pacientes oncológicos? Assim, foram definidos com base na questão norteadora: População – adultos com diagnóstico de câncer; Conceito – uso de LDN associado ao tratamento oncológico convencional; e Contexto – centros de tratamento de câncer no mundo.
Critério de elegibilidade dos estudos
Foram incluídos na revisão estudos primários quantitativos ou qualitativos. Consideraram-se também teses, dissertações, livros, documentos técnicos e governamentais, e não houve limite temporal para a seleção. Incluíram-se publicações em inglês, espanhol e português que continham os seguintes descritores ou palavras-chave e seus análogos: naltrexona, naltrexona em dose baixa, câncer, humanos, adultos, imunomodulação e resposta imune.
Excluíram-se aqueles que não tiveram como objetivo principal o efeito da LDN em pacientes oncológicos, que abordaram o uso de LDN em outras condições de saúde (ex.: fibromialgia, doenças reumatológicas), uso em crianças ou animais, bem como revisões narrativas e integrativas, editoriais, protocolos de pesquisa, instrumentos de validação, textos da Internet, editoriais, ensaios e artigos não disponibilizados na íntegra nas bases de dados.
Fontes de informação e estratégia de busca
Realizaram-se as buscas entre setembro e outubro de 2023. A busca da produção científica foi feita nas bases de dados MEDLINE (via PubMed), LILACS (via Biblioteca Virtual em Saúde) e google scholar.
As referências dos artigos selecionados foram verificadas para identificar novos estudos não localizados nas buscas anteriores, observados os critérios de inclusão previamente estabelecidos.
Considerando os critérios de inclusão, elaborou-se a estratégia de busca no PubMed, a partir do Medical Subject Headings (MeSH) e acrescidos das palavras-chave a saber: “naltrexone” OR “low-dose naltrexone” AND “cancer” AND “humans” OR “adults” AND “immunomodulation” OR “Immunity” [MeSH Terms] NOT “rheumatological diseases” [MeSH Terms] OR “children” [MeSH Terms] OR “animals” OR “fibromyalgia”.
Essa estratégia foi adaptada conforme as especificidades de cada base utilizada. Em todas as bases de dados realizou-se a busca considerando-se a data de publicação até o dia 12 de outubro de 2023.
Para construção da estratégia de busca desta revisão realizou-se um estudo preliminar na base PubMed com descritores que fazem parte do Decs e Mesh conforme apresentado no Quadro 1.
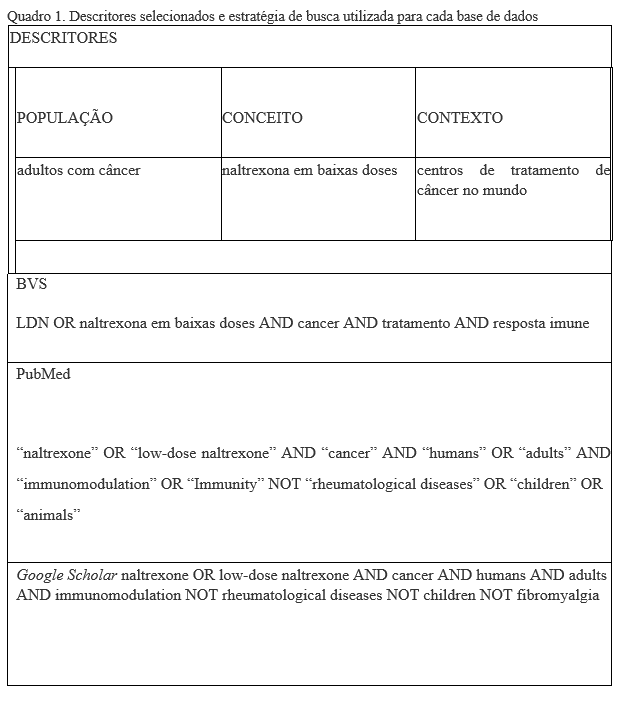
Seleção de fontes de evidência
Dois revisores fizeram a triagem independente dos estudos e os selecionaram com base nos títulos e resumo. Posteriormente, os revisores leram independentemente na íntegra os artigos pré-selecionados, identificando com precisão a sua relevância para a pesquisa e se os critérios de inclusão estavam contemplados. As divergências entre os revisores foram resolvidas por discussão e em colaboração com um terceiro revisor, para alcançar o consenso entre todos.
O software RAYYAN® foi utilizado para organizar a leitura e seleção dos artigos pelos pesquisadores colaboradores envolvidos, que agiliza a triagem inicial de resumos e títulos, usando um processo de semi-automação, e incorpora um alto nível de usabilidade neste processo (Ouzzani et al., 2016).
Processo de coleta dos dados e síntese dos resultados
A extração e sintetização dos elementos essenciais encontrados em cada publicação foram realizadas por dois revisores independentes, a partir de um instrumento estruturado, elaborado para este estudo, e utilizou-se o Microsoft Excel (https://products.office.com/) para a tabulação dos dados.
Os dados extraídos incluíram detalhes sobre a autoria, ano das publicações, tipo, objetivos, desenho, local, população, tipo de câncer, tratamento, dosagem de naltrexona e as principais descobertas relevantes para o objetivo desta revisão (efeitos do uso de LDN em pacientes oncológicos, com foco nas respostas imunológicas). Os dados se encontram apresentados em gráficos e tabelas, e a discussão apoiada na literatura disponível.
RESULTADOS
A busca inicial identificou um total de cinco artigos. Destes, cinco foram selecionados para compor essa revisão, pois atenderam aos critérios de inclusão. A figura 1 apresenta um fluxograma com o processo de busca e seleção dos artigos.
Figura 1. Fluxograma de seleção dos artigos incluídos na revisão de escopo
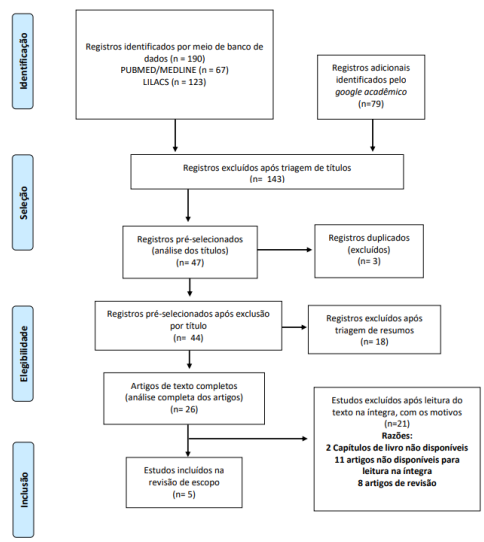
Os artigos que compuseram essa revisão são relatos de casos. Nenhum estudo com delineamento mais robusto (ex.: prospectivos, longitudinais e ensaios clínicos) foram encontrados relacionado ao uso da LDN em pacientes oncológicos. A idade dos pacientes variou de 46 a 80 anos, totalizando sete pacientes, sendo cinco do sexo masculino e dois do sexo feminino. Os diagnósticos de câncer diferiram entre os casos, a maioria apresentou metástase em alguma região do corpo e prognóstico restrito.
A dose de LDN utilizada dos estudos variou de 3 a 4,5 mg dia, administrada via oral, com posologia diária ou 2 vezes por semana. Apenas dois estudos usaram o LDN de forma isolada (Berkson B.M. et al., 2007; Jeffrey A. Miskoff et al., 2018), os demais utilizaram a LDN como parte de um protocolo integrativo individualizado, elaborado pelos autores que incluía outras medicações, dietas controladas e mudança de hábitos de vida. As características gerais dos estudos incluídos nessa revisão, bem como os principais resultados, encontram-se descritos na tabela 1.
Tabela 1. Principais características dos estudos incluídos, população, desfechos e principais resultados dos estudos incluídos na revisão de escopo.
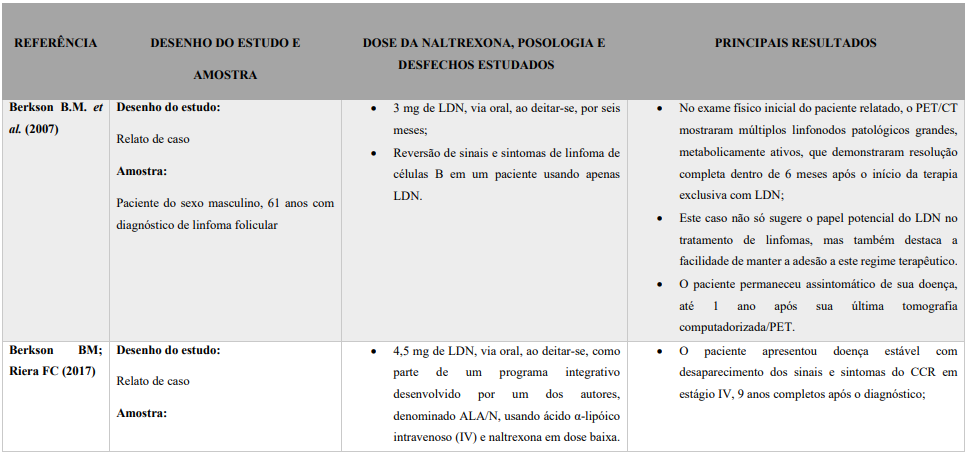



DISCUSSÃO
Esta revisão de escopo identificou na literatura corrente, cinco artigos, do tipo relato de caso, que utilizaram LDN de forma exclusiva ou como parte do tratamento de pacientes com câncer. Todos os estudos demonstraram benefícios do uso de LDN em pacientes com câncer, incluindo resolução completa de linfonodos patológicos após o início da terapia exclusiva com LDN (Berkson, 2007). Nenhum efeito tóxico foi relatado pelos autores.
Um estudo de caso realizado por Berkson e cols (2006), no Centro Médico Universitário em oncologia, de 2002 a 2006, em um paciente de 46 anos, com câncer de pâncreas com metástase hepática, em associação de ácido Lipóico (ALA) intravenoso, e Naltrexona em baixas doses, respectivamente, 300-600mg, 2 dias, por semana, e 4,5 mg, ao deitar, revelaram aumento da sobrevida, bem como, ausência de sintomas e progressão da doença, sem efeitos tóxicos, além da melhora subjetiva da disposição, em paciente considerado terminal e com tratamentos convencionais considerados esgotados, reforçando uma opção animadora no manejo de cânceres agressivos, como o de pâncreas.
Além disso, outro relato de caso reforça a potencialidade da Naltrexona em baixas doses em um câncer potencialmente fatal, como o de pulmão metastático. O referido trabalho foi realizado por Miskoff et al. (2018), na Neptune City, EUA, de 2014 a 2018, em um paciente de 50 anos, com doses de Naltrexona de 4,5 mg, corroboraram com umas das salutares propriedades da LDN, a inibição da atividade anticarcinogênica, haja vista, a ausência de recorrência da doença neste paciente durante o seu uso.
Em 2006, um estudo de caso realizado no Centro Médico Integrativo do Novo México, por Berkson et al, acompanhou o caso de um paciente do sexo masculino, de 61 anos, diagnosticado com linfoma folicular de células β. Em 2004, o paciente havia recusado o tratamento convencional de quimioterapia devido aos efeitos colaterais. Após 17 meses, ele procurou tratamento alternativo e aceitou a terapia com Naltrexona em baixas doses (LDN), com administração de 3 mg todas as noites ao deitar-se, por praticamente não apresentar efeitos colaterais. Ele também recebeu uma dieta específica e suplementos, mas não seguiu as recomendações dietéticas nem continuou com os suplementos alimentares, continuou somente com o LDN. Apesar disso, após apenas uma semana de tratamento, o paciente apresentou melhora dos sintomas, incluindo a diminuição do tamanho dos gânglios linfáticos. Após 6 meses, seus nódulos desapareceram, e uma nova tomografia mostrou melhora significativa. Embora os autores tenham considerado a possibilidade de remissão espontânea, eles atribuíram a remissão clínica e radiológica ao tratamento com LDN e sugerem que o medicamento merece investigação adicional devido à rapidez da melhora de pacientes oncológicos que fizeram seu uso na dose correta, devido ao seu baixo custo, facilidade de administração e potencial eficácia.
Outro relato de caso, realizado por Berkson et al em 2018 no Centro Médico Integrativo do Novo México, descreve a história de um paciente de 64 anos, do sexo masculino, diagnosticado em 2008 com câncer de células renais, metastático, em estágio IV, que foi acompanhado de 2010 a 2015, e em 2017, 9 anos após o diagnóstico, ele se encontrava bem. Após passar por tratamentos convencionais e não obter resultados positivos, foi ofertado ao paciente um programa integrativo que incluiu tratamentos com ácido αlipóico intravenoso, vitamina C intravenosa, naltrexona em baixas doses (LDN), hidroxicitrato e mudanças no estilo de vida. Já após a primeira semana de tratamento, o paciente começou a se sentir melhor, relatando mais energia e uma maior sensação de bem-estar. Ao longo dos nove anos, ele apresentou uma melhora significativa em seus sintomas, recuperou o peso inicial, melhorou sua energia e perspectiva e conseguiu retornar ao trabalho em tempo integral. Os resultados sugerem que esse programa integrativo pode ser eficaz no tratamento do câncer de células renais em estágio IV, oferecendo uma abordagem alternativa à terapia convencional.
LIMITAÇÕES
Nos estudos realizados por Miskoff et al (2018), não foram relatados a frequência das doses, bem como, via de administração, associação, e seus efeitos adversos. No que diz respeito aos achados após administração, o estudo limitou-se aos resultados de exames de imagem, nos quais não foram evidenciados progressão da doença.
Em suas colocações, Berkson et al, também relata que não foram encontrados efeitos colaterais e adversos.
CONCLUSÃO
Nos relatos incluídos nessa revisão de escopo, a terapia integrativa com uso de naltrexona e baixas doses demonstrou ser promissora para o tratamento de pacientes oncológicos, uma vez que nenhum efeito adverso ou tóxico foi reportado, a sua pronta disponibilidade e o efeito positivo no aumento de sobrevida em pacientes com câncer em estado terminal.
Sua eficácia, no entanto, merece investigação mais aprofundada em ensaios clínicos controlados, com avaliação multidisciplinar, para que futuramente possa haver a possibilidade de uma utilização mais ampla e segura da terapia.
ANEXOS
Anexo 1 – Mapa de doses utilizadas para cada tipo de câncer.
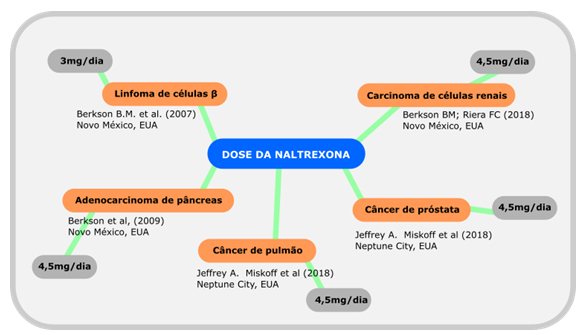
REFERÊNCIAS
Berkson BM, Rubin DM, Berkson AJ. Reversal of Signs and Symptoms of a B-Cell Lymphoma in a Patient Using Only Low-Dose Naltrexone. Integrative Cancer Therapies. 2007;6(3):293-296. doi:10.1177/1534735407306358
Berkson BM, Rubin DM, Berkson AJ. Revisiting the ALA/N (alpha-lipoic acid/low-dose naltrexone) protocol for people with metastatic and nonmetastatic pancreatic cancer: a report of 3 new cases. Integr Cancer Ther. 2009 Dec;8(4):416-22. doi: 10.1177/1534735409352082. Erratum in: Integr Cancer Ther. 2010 Jun;9(2):247. PMID: 20042414. DOI: 10.1177/1534735409352082
Berkson BM, Rubin DM, Berkson AJ. The long-term survival of a patient with pancreatic cancer with metastases to the liver after treatment with the intravenous alpha-lipoic acid/low-dose naltrexone protocol. Integr Cancer Ther. 2006 Mar;5(1):83-9. doi: 10.1177/1534735405285901. PMID: 16484716.
Berkson BM, Calvo Riera F. The Long-Term Survival of a Patient With Stage IV Renal Cell Carcinoma Following an Integrative Treatment Approach Including the Intravenous α-Lipoic Acid/Low-Dose Naltrexone Protocol. Integr Cancer Ther. 2018 Sep;17(3):986993. doi: 10.1177/1534735417747984. Epub 2017 Dec 19. PMID: 29258346; PMCID: PMC6142095.
Dalgleish, A. G., Liu, W. M.”The role of immune modulation and anti-inflammatory agents in the management of prostate cancer: A case report of six patients”. Oncology Letters 24, no. 2 (2022): 247. https://doi.org/10.3892/ol.2022.13367
GUIMARÃES, André Eduardo Xavier et al., “O uso off-label da naltrexona em baixa doses,” REPOSITÓRIO INSTITUCIONAL DA FAMP, acesso em 16 de outubro de 2023, http://repositorio.fampfaculdade.com.br/items/show/546.
Miskoff JA, Chaudhri M. Low Dose Naltrexone and Lung Cancer: A Case Report and Discussion. Cureus. 2018 Jul 5;10(7):e2924. doi: 10.7759/cureus.2924. PMID: 30197847; PMCID: PMC6126779. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6126779/. Acesso em: 6 nov. 2023.
Ouzzani M, Hammady H, Fedorowicz Z, Elmagarmid A. Rayyan – a web and mobile app for systematic reviews. Syst Rev. 2016;5(1):210. doi: https://doi. org/10.1186/s13643016-0384-4
Qichao Wu, Xiangyuan Chen, Jiaqiang Wang, Pengfei Sun, Meilin Weng, Wankun Chen, Zhirong Sun, Minmin Zhu, Changhong Miao, Nalmefene attenuates malignant potential in colorectal cancer cell via inhibition of opioid receptor, Acta Biochimica et Biophysica
Sinica, Volume 50, Issue 2, February 2018, Pages 156–163, https://doi.org/10.1093/abbs/gmx131 Disponível em: https://pubmed.ncbi.nlm.nih.gov/29267844/. Acesso em: 15 out. 2023.
Rocha, B. Imunoterapia para o câncer – Programa de Aprimoramento Profissional Secretaria de Estado da Saúde Coordenadoria de Recursos Humanos Fundação do Desenvolvimento Administrativo – Fundap. [s.l: s.n.]. Disponível em:<https://docs.bvsalud.org/biblioref/ses-sp/2014/ses-31786/ses-31786-5840.pdf>.
Santos M de O, Lima FC da S de, Martins LFL, Oliveira JFP, Almeida LM de, Cancela M de C. Estimativa de Incidência de Câncer no Brasil, 2023-2025. Rev. Bras. Cancerol. [Internet]. 6º de fevereiro de 2023 [citado 16º de outubro de 2023];69(1):e-213700. Disponível em: https://rbc.inca.gov.br/index.php/revista/article/view/3700. DOI: https://doi.org/10.32635/2176-9745.RBC.2023v69n1.3700
Sung, H., Ferlay, J., Siegel, R. L., Laversanne, M., Soerjomataram, I., Jemal, A., & Bray, F. (2021). Global Cancer Statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: A Cancer Journal for Clinicians, 71(3), 209–249. DOI: https://doi.org/10.3322/caac.21660
The Joanna Briggs Institute. Joanna Briggs Institute reviewers’ manual: 2014 edition. https://nursing.lsuhsc.edu/JBI/docs/ReviewersManuals/Economic.pdf. Acesso em 09/Out/2023. » https://nursing.lsuhsc.edu/JBI/docs/ReviewersManuals/Economic.pdf
Tricco, Andrea C. et al. PRISMA extension for scoping reviews (PRISMA-ScR): checklist and explanation. Annals of internal medicine, v. 169, n. 7, p. 467-473, 2018.
1Acadêmicos do curso de Medicina da Faculdade Estácio de Juazeiro-BA
2Profa. Orientadora
