REGISTRO DOI: 10.5281/zenodo.10214367
Aline Moraes Damaceno1
Ruan Damaceno2
Araceli Scalcon3
Resumo
Os polímeros naturais são materiais versáteis e com inúmeras aplicações em diversas áreas, inclusive na farmacêutica. Podem atuar como moduladores e direcionadores na liberação de fármacos em sítios específicos no organismo, bem como bioadesivos, biomiméticos e hidrogéis responsivos, podendo ser amplamente incluídos em formulações farmacêuticas. A pectina é um exemplo desses polímeros e pode ser extraída de diversos vegetais. A partir do exposto, o objetivo do trabalho é obter a pectina a partir da secagem e extração da casca da laranja (Citrus sinensis L. Osbeck) para aplicação farmacêutica. Para tanto, a metodologia contempla testes de extração da pectina. Uma melhor extração, foi obtida com adição da enzima em pH 4 e 70 Cº, após ser realizado oito testes, sendo cinco por meio ácido e 3 enzimáticas.
Palavras-chave: Heteropolissacarídeo. Qualidade. Metodologia. Secagem.
Abstract
Natural polymers are versatile materials with countless applications in different areas, including pharmaceuticals. They can act as modulators and drivers in the release of drugs at specific sites in the body, as well as bioadhesives, biomimetics and responsive hydrogels, and can be widely included in pharmaceutical formulations. Pectin is an example of these polymers and can be extracted from various vegetables. Based on the above, the objective of the work is to obtain pectin from the drying and extraction of orange peel (Citrus sinensis L. Osbeck) for pharmaceutical application. To this end, the methodology includes pectin extraction tests. It is expected that the product obtained, after characterizing its properties, will result in a potential pharmaceutical application.
Keywords: Heteropolysaccharide. Quality. Methodology. Drying.
1 Introdução
A pectina é uma substância natural presente em diversas frutas e vegetais, sendo especialmente abundante nas cascas e sementes de frutas cítricas. Algumas das principais fontes de pectina incluem a laranja, o limão, a maçã, a beterraba e a cenoura. É amplamente utilizada na indústria alimentícia como espessante, agente de gelificação e estabilizante em diversas aplicações, como a produção de geleias, iogurtes, sucos e sobremesas (REICHEMBACH, L. H; DE OLIVEIRA PETKOWICZ, C. L, 2021; ANDERSON, 2016; CANTERI, et al. 2012).
A extração de pectina é um processo de grande importância também para a indústria farmacêutica, e varia de acordo com a matéria-prima. Quando feita a partir de fontes naturais é um processo complexo que envolve a utilização de enzimas e soluções ácidas para separar a pectina das outras substâncias presentes no material de origem (MUNHOZ, 2008).
A laranja é um fruto cítrico, dotado por diferentes benefícios, sendo o mais conhecido a ação antioxidante e aumento da imunidade, provenientes da vitamina C, além de contribuir na ação contra pedras nos rins, pois trata-se de uma fruta cítrica composta por vários ácidos determinantes para evitar tal complicação (ALVES, 2019).
De acordo com a Companhia Nacional de Abastecimento – CONAB, estudos realizados em conjunto com a Secretaria de Agricultura e Abastecimento de Pessoas, a maior produção de laranja consiste no interior de São Paulo, responsável por 85% da produção do Brasil (ALVES, 2019).
Consequentemente, o Brasil também é o maior produtor de suco natural e campeão em exportação do mesmo. A perspectiva é de produção cada vez maior
em decorrência da demanda dos consumidores que buscam por uma alimentação mais saudável e com menor teor de aditivos químicos (MUNHOZ, 2008).
Junto a essa demanda, surge o aumento da geração de elevados volumes de resíduos como consequência das atividades industriais de produção de alimentos, cuja destinação pode se tornar um problema devido à necessidade de espaço e possíveis riscos ambientais quando mal gerenciados. Segundo a Lei nº 12.305/10 regida pela Política Nacional de Resíduos Sólidos – PNRS, um resíduo só é considerado rejeito quando se esgotam todas as possibilidades de reaproveitamento do mesmo (KINAS E TORRES, 2014).
Sendo assim, a extração da pectina da casca da laranja pode ser vista como uma oportunidade de reaproveitamento do resíduo gerado durante o processo de algumas indústrias alimentícias (BENELLI, 2010), resultando em um produto com potencial farmacêutico. Diante disso, o objetivo do trabalho foi obter a pectina a partir da secagem e extração da casca da laranja (Citrus sinensis L. Osbeck) para possível aplicação farmacêutica.
3 Materiais e Métodos
As amostras de casca de laranja (Citrus sinensis L. Osbeck) foram adquiridas por meio de doação do restaurante da Indústria Farmacêutica localizado na cidade de Toledo-PR. Os experimentos ocorreram nos laboratórios do Biopark Educação. O procedimento experimental contemplou etapas de preparação, extração e caracterização, conforme mostra o fluxograma da Figura 1. Na preparação, os resíduos foram lavados, cortados e posteriormente, foram levados para a secagem. Para a etapa de extração realizou-se dois métodos de extração, enzimático e ácido, seguindo como base a metodologia de extração executada por McCready e McComb (1952) e Kratchanova, Panchev et al. (1994)
Figura 3: Fluxograma, etapas da extração da pectina da casca da laranja.
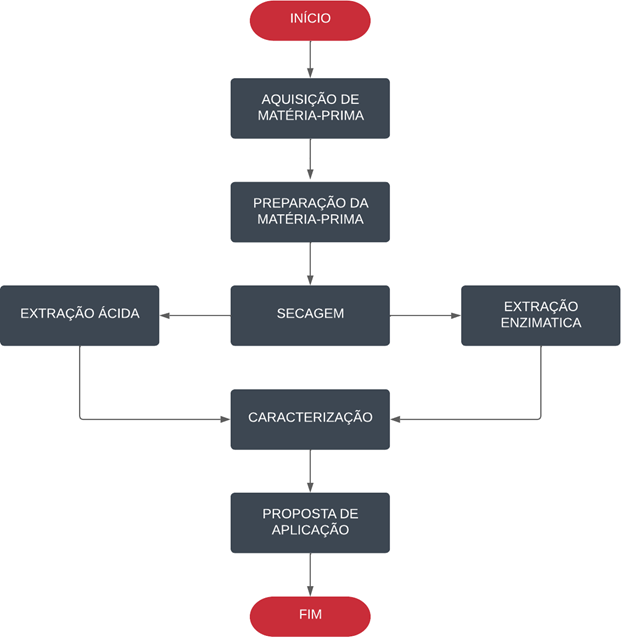
Fonte: Autoria própria
3.1 Extração ácida
A metodologia de extração foi adaptada de McCready e McComb (1952) e Kratchanova, Panchev et al. (1994). Neste tipo de extração, a amostra provinda da secagem foi diluída em água e acidificada com solução de ácido cítrico 1 M.
A mistura acidificada foi colocada sob agitação em 650 rpm e aquecida a 80 ºC por 120 minutos. Após esta etapa, as amostras seguiram para processo de purificação do extrato por meio de centrifugação durante 15 minutos a 3.500 rpm.
Colocou-se o extrato clarificado sobrenadante sob agitação no agitador magnético e adicionou-se etanol 95% por gotejamento, na razão de 1:2 v/v, conforme sugerido por Elnawawi e Shehata (1987). Após uma hora de agitação, mantivemos a amostra em repouso para assegurar a separação da pectina e do etanol. Separou-se a pectina por filtração a vácuo e encaminhou para a estufa de circulação forçada a 50 °C até o peso constante. O processo foi finalizado com lavagens subsequentes com etanol 70 % e 95 %, respectivamente.
3.2 Extração enzimática
Para a extração enzimática foi utilizada a pectinase líquida de amplo espectro obtida comercialmente. As informações fornecidas pelo fabricante indicam que a sua faixa de trabalho ideal é de 60 a 70 ºC e pH de 4 a 6. Para determinar qual a melhor faixa de temperatura e pH decorreu-se três extrações.
Colocou-se aproximadamente 2,0 gramas de amostra (albedo e flavedo desidratados provindos da secagem) acrescentando em Erlenmeyer água destilada na proporção de 1:70 (m/v). Ajustando o pH em uma faixa de 4 a 6 através da adição de ácido cítrico (1 Molar, Nuclear) e adicionado a pectinase na proporção 3/100 (v/v) agitou-se a mistura em 650 rpm e aquecimento de 60 a 70 ºC de 60 a 120 minutos. Após esta etapa, as amostras seguiram para o processo de purificação do extrato por meio de centrifugação durante 15 minutos a 3.500 rpm.
O extrato clarificado sobrenadante foi colocado sob agitação no agitador magnético e adicionado etanol 95% por gotejamento, na razão de 1:2 v/v. Após uma hora de agitação, a mistura precisou ficar em repouso, para assegurar a separação da pectina e do etanol. Separou-se a pectina por filtração a vácuo e levou-se à estufa de circulação forçada a 50 °C até o peso constante. Resultados semelhantes foram observados por Yang et al. (2018)
3.3 Caracterização
Calculou-se o rendimento da extração de pectina da matéria seca através do cálculo:
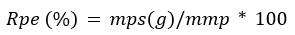

3 Resultados e Discussões
A extração da pectina foi realizada de acordo com a metodologia descrita no item 3.1 e 3.2. As imagens 1 e 2 apresentam respectivamente a pectina após adição de etanol, resultando em precipitação e filtração.
Imagem 1 Precipitação da pectina em etanol.

Fonte: autoria própria
Imagem 2 Filtragem da pectina.

Fonte: autoria própria
4.1 Extrações ácidas:
O quadro 4.1.1 apresenta o rendimento médio da pectina extraída da casca da laranja utilizando pH de 2,39 à 2,61 em aquecimento de 80 graus e durante 120 minutos. Nestas condições foi obtido uma média de 18,88%.
Quadro 4.1.1 – Rendimento médio da pectina extraída a 80ºC por 120 min:
Amostra pH Rendimento 1 2,43 19,2% 2 2,52 18,6% 3 2,61 18,1% 4 2,39 19,7% 5 2,54 18,8%
O rendimento obtido na extração foi de 18,9 %, menor do que o rendimento obtido por McCready e McComb (1952) e Kratchanova, Panchev et al. (1994), de 21% e 32 %, respectivamente. Acreditamos que esse baixo rendimento está interligado a capacidade máxima de centrifugação do equipamento, limitada a 3500rpm, sendo o proposto pelo método uma rotação de 10000rpm. A alternativa explorada foi a aplicação de maior tempo de equipamento, onde o proposto era de 10 minutos e substituímos 15 minutos. Mesmo com as adaptações testadas, não foi possível obter os mesmos rendimentos.
4.2 Extrações enzimáticas:
O quadro 4.2.1 demonstra o rendimento da extração da pectina sob a ação da enzima pectinase.
Quadro 4.2.1 – Rendimento médio da pectina extraída:
Amostra pH Enzima Temperatura Tempo Rendimento 1 4,00 4,5 ml 70 120 32,4% 2 5,02 4,5 ml 65 90 30,6% 3 6,00 4,5 ml 60 60 29,7 %
Para determinar a melhor faixa de pH e temperatura foram realizados três testes, com pH de 4 a 6 e temperaturas de 60Cº a 70Cº, por um período de tempo de 60 a 120 minutos. Podemos observar de acordo com os resultados que a adição de pectinase, aumentou significativamente o rendimento obtido, mesmo com a variável da rotação a 3500rpm. Sendo o melhor rendimento o teste com menor pH e maior tempo de extração,resultado esse que vai ao encontro das pesquisas realizadas, quando comparado a outros estudos.
5 Considerações Finais
Levando em consideração o propósito inicial desta pesquisa, referente a extração da pectina da casca da laranja através de dois métodos em diferentes condições avaliando seu rendimento, findamos esta ideia inicial com uma média de 30.9%, resultado da extração com a enzima pectinase menor pH e maior temperatura, sendo esse o melhor rendimento obtido.
No entanto, dentre os testes realizados e resultados inferiores, concluímos que a influência das variáveis operacionais influenciam diretamente nos valores alcançados.
Portanto, diante dos resultados obtidos e das considerações expostas acima, verifica-se que este estudo contribui para o avanço de pesquisas em extração de pectina da casca da laranja, para uma possível aplicação em larga escala, visto que este estudo utilizou operações unitárias simples (secagem e extração por meio ácido e enzimático) e obteve resultados satisfatórios, indicando que os processos aplicados são viáveis para obtenção de pectina. Conclui-se que a adição da enzima é um fato crucial e de grande importância na obtenção de pectina.
Referências
ALVES, Mayk. Laranja é uma das frutas mais populares do Brasil e em todo mundo. Agro20, 2019. Disponível em: https://agro20.com.br/laranja/.
ANDERSON, C. T. We be jammin’: an update on pectin biosynthesis, trafficking and dynamics. Journal of experimental botany, v. 67, n. 2, p. 495-502, 2016.
ANTUNES,H,E. Uso de pectinas na texturização de alimentos. Instituto superior de agronomia. Universidade de Lisboa. Dissertação para a obtenção do Grau de Mestre em Ciências Gastronómicas. 2021.
ARAMI, M. et al. Removal of dyes from colored textile wastewater by orange peel adsorbent: Equilibrium and kinetic studies. Journal of Colloid and Interface Science, v. 288, n. 2, p. 371- 376, 2005.
BENELLI, P. Agregação de valor ao bagaço de laranja (Citrus sinensis L. Osbeck) mediante obtenção de extratos bioativos através de diferentes técnicas de extração.
Dissertação de mestrado, Programa de Pós-graduação em Engenharia de Alimentos, Universidade Federal de Santa Catarina. Florianópolis, Brasil.2010.
BRADDOCK, R.J. Handbook of Citrus By-Products and Processing Technology. Lake Alfred-USA: University of Florida, John Wiley & Sons, 1999. 247p.
CANTERI, Maria H. G.; MORENO, Lirian et al. Pectina: da matéria-prima ao produto final. Seção técnica polímeros, 2012. Disponível em:
CANTERI, Maria H. G.; MORENO, Lirian et al. Pectina: da matéria-prima ao produto final. Seção técnica polímeros, 2012. Disponível em:
https://doi.org/10.1590/S0104-14282012005000024.
DEITOS, A.; KIELING, A.G.; FERNANDES, I. J.; MORAES, C.A.M.; BREHM, F. A.;
Avaliação do resíduo casca da laranja na obtenção de pectina e óleo essencial. ResearchGate, p.3 a 8, março, 2015.
FANI, Marcia. Pectinas – origem, características e aplicação industrial. Revista Aditivos & Ingredientes, ‘’s.d’’. Disponível em:
https://aditivosingredientes.com/artigos/todos/pectinas-origem-caracteristicas-e-aplic acao-industrial.
KINAS, N.P; TORRES, E. Poluição e resíduos sólidos. Centro Universitário Leonardo da Vinci – UNIASSELVI.Indaial – SC, p. 214, 2014.
LIU, D. et al. A wide diversity exists in pectin structure from thirteen apple cultivars.
International Journal of Biological Macromolecules, p. 125410, 2023.
REICHEMBACH, L. H; DE OLIVEIRA PETKOWICZ, C. L.. Pectins from alternative sources and uses beyond sweets and jellies: An overview. Food Hydrocolloids, v. 118, p. 106824, 2021.
SARTORI, I.A.; KOLLER,O.C.; SCHWARZ,S.F.; BENDER,R.J.; SCHAFER,G.
Maturação de frutos de seus cultivares de laranjas doces no depressão central do Rio Grande do Sul. Rev. Bras. Frutic., Jaboticabal – SP, v. 24, n. 2, p. 364-369, agosto. 2002.
SILVA Team. (2011b). What is pectin? Obtido de https://www.silvateam.com/en/products-andservices/food-ingredients/pectin/what-pec tin.html.
ZIMKE, D. Bala de pectina: Elaboração e avaliação sensorial. CENTRO UNIVERSITÁRIO UNIVATES CURSO TÉCNICO EM QUÍMICA. Lajeado, novembro de 2014.
Aline Moraes Damaceno – Aluna do Curso de Fármacia, Faculdade Biopark Educação, 85900-000, Toledo, PR, Brasil1
Ruan Damaceno – Aluno do Curso de Fármacia, Faculdade Biopark Educação, 85900-000, Toledo, PR, Brasil2
Araceli Scalcon – Curso de Fármacia, Faculdade Biopark Educação, 85900-000, Toledo, PR, Brasil3
