PREPARATION AND EVALUATION OF THE STABILITY OF O/W CREAMS BASED ON ANIONIC OR NONIONIC EMULGENT
REGISTRO DOI: 10.5281/zenodo.10076617
Acquila Freire Queiroz Sato1
Ágda Freire Queiroz Braz2
Ismael Holanda do Vale3
Larissa Bruno Gomes4
Amâncio Henrique Damasceno5
Gabriela do Nascimento Vieira6
Luana Marques Rodrigues7
Marigilson Pontes de Siqueira Moura8
RESUMO
Os danos à pele como queimaduras e fotoenvelhecimento, bem como o número de casos de câncer de pele no Brasil aumenta progressivamente com o passar dos anos, isto ocorre por causa dos altos índices de radiações ultravioletas emitidos pelo sol no Brasil durante todo o ano, até mesmo no inverno. Assim, medida de proteção contra a luz solar é de vital importância, o que inclui o uso principalmente de filtros solares de amplo espectro. Com a grande demanda e apelo por cosméticos ecológicos, ou seja, que utilizem de recursos naturais em sua composição, é de fundamental relevância a pesquisa e o desenvolvimento de novos protetores solares que utilizem de matérias-primas vegetais, visto que estas são abundantes na natureza, renováveis, rentáveis e estão associadas a poucos números de casos relacionados às alergias e irritações. A uva é amplamente estudada e conhecida por apresentar compostos bioativos tais como os flavonoides e taninos, que apresentam efeitos antioxidantes e fotoprotetores, pode ser utilizada para incorporação em bases galênicas de caráter aniônica e não iônica para estudo da estabilidade. O bagaço da uva, um subproduto da vinificação, conserva fitocompostos em quantidades elevadas e rotineiramente é descartado por não ter uma utilidade, por isso o seu uso na pesquisa e desenvolvimento de um novo fitocosmético torna-se essencial. A proposta do estudo visou a incorporação do extrato etanólico bruto em cremes O/A com emulgentes diferentes, para avaliar a sua estabilidade, através de teste de pH, viscosidade, características organolépticas, teste de estabilidade acelerada e centrífuga, bem como o estudo do FPS adquirido por essas formulações. As bases galênicas se adaptaram bem com o extrato, uma vez que não houve floculação e/ou separação de fases em nenhum momento da pesquisa, porém reações de oxidação foram observadas a olho nú que podendo ter influenciado na diferença dos valores de pH, bem como do FPS, que deram valores significativos utilizando apenas 5% do extrato. Estudos relacionados a um aumento dessa porcentagem e na aplicação de outros cosméticos multiuso são uma boa alternativa.
Palavras-chave: Uva. Bagaço da uva. Fotoproteção. Radiação ultravioleta. Emulsão.
1. INTRODUÇÃO
A pele é o maior e um dos mais importantes órgãos do corpo humano, dentre suas funções, ela é a nossa primeira linha de defesa. A realização de atividades ao ar livre, com consequente exposição aos raios solares, resulta em bem-estar físico e psicológico, e por isso, para minimizar os efeitos deletérios dos raios UV emitidos pelo sol na pele, a prática de fotoproteção é imprescindível, o que inclui principalmente o uso de filtros solares, a busca por sombra, vestimentas fotoprotetivas, chapéus, óculos, e outras ferramentas a nossa disposição, visto que o número de casos de cânceres de pele vem aumentando progressivamente (CARDOSO et al., 2017; NDIAYE et al., 2011).
Pelo fato de a pele estar continuamente exposta à luz solar, tal exposição pode resultar em efeitos positivos e negativos, essas implicações estão diretamente relacionadas com tempo de exposição, bem como do tipo de pele em questão. Dentre os efeitos benéficos, podem-se destacar como principais, a síntese de vitamina D e a prevenção de doenças como osteoporose e diabetes tipo I (CORRÊA, 2015).
Entretanto, quando o assunto são os efeitos deletérios da exposição prolongados a luz do sol, os principais são a formação de eritemas, fotoenvelhecimento, imunossupressão e, em casos mais sérios, o câncer de pele, que conta com duas classificações: os não melanomas (os mais comuns) e o do tipo melanoma (considerados os mais graves) (LIM; ARELLANO-MENDOZA; STENGEL, 2017; SCHALKA; REIS, 2011).
De acordo com o Instituto Nacional de Câncer (INCA), a estimativa de novos casos de canceres de pele do tipo não melanoma, o mais frequente no Brasil, para o ano de 2018 é de 85.170 para os homens e 80.410 para as mulheres. O número de mortes provocadas por esse tipo de câncer chega a 1.958 pessoas (1137 homens e 821 mulheres) de 2015 aos dias atuais (INCA 2019).
A demanda pelo desenvolvimento e pesquisa de novos produtos cosméticos que contribuam nessa proteção aos raios solares vem aumentando consideravelmente ao longo do tempo, principalmente os produtos que fazem o uso de componentes de origem vegetal, sendo estes recursos: naturais, renováveis, abundantes e prontamente disponíveis, e por conta do apelo ecológico implícito na utilização desse material (BADEA et al., 2015; BERES et al., 2017).
Os extratos naturais podem proporcionar proteção contra os raios ultravioleta (UV), pois são ricos em compostos fenólicos com atividade sequestradora de radicais livres, e conta com a presença de outras propriedades bioativas, tais como a hidratação da pele, restauração da função de barreira e promoção da síntese de colágeno. Uma vez que a absorção ultravioleta tem sido vista ao incorporarem-se esses extratos em veículos farmacêuticos, tais como as emulsões. (BADEA et al., 2015; MERCURIO et al., 2015; VIOLANTE et al, 2009).
A região Submédia do Vale do são Francisco é uma das regiões brasileiras com a economia voltada à produção de vinhos, e, por conseguinte, gera grandes quantidades de resíduos orgânicos, como o bagaço da uva, riquíssima em moléculas bioativas, porém é comumente descartado, o que torna o uso desse recurso de grande vantagem comercial e maximiza a relevância do seu aproveitamento no desenvolvimento de outros produtos (BADEA et al., 2015; BERES et al., 2017).
Com base no exposto, o presente trabalho tem como objetivo avaliar o emprego do extrato etanólico bruto de bagaço da uva (Vitis Vinifera) da variedade Syrah em emulsões com emulsificantes diferentes: não iônicas e aniônicas. Para avaliação do comportamento desses sistemas foi utilizado o teste de estabilidade acelerada, com ciclos de gelo e degelo, bem como a avaliação da atividade fotoprotetora dessas formulações obtidas com a incorporação do extrato bruto.
2. FUNDAMENTAÇÃO TEÓRICA OU REVISÃO DA LITERATURA
2.1. RADIAÇÃO ULTRAVIOLETA E SEUS EFEITOS SOBRE A PELE
A latitude é um parâmetro determinante na incidência de radiação solar emitida na atmosfera terrestre, a emissão dos raios solares em locais próximos à linha do equador é maior se comparado aos polos, isto ocorre por conta da maior inclinação dos raios solares nesta área (ROMBALDI, 2017). Devido sua localização geográfica, observa-se que no Brasil os níveis de radiação solar permanecem alto praticamente durante todo o ano, até mesmo no inverno, resultando em altos índices de danos a pele observado (CORRÊA, 2015).
O sol emite radiação ultravioleta (R-UV), que faz parte do espectro eletromagnético, e corresponde ao comprimento de onda de 100 a 400nm, a radiação ultravioleta (R-UV) representa somente 10% do total de radiação emitida pelo sol que incide na atmosfera, e ela ainda é subdividida em 3 tipos: radiação UVC que vai de 100 a 280 nm, a UVB de 280 a 315 nm, e por último, a radiação UVA que está entre 315 e 400 nm. Os outros 90% da radiação solar é caracterizado como o espectro visível e de infravermelho (CORRÊA, 2015; LORIGO; MARIANA; CAIRRAO, 2018).
A luz do sol é necessária à saúde e bem-estar, esses efeitos fotoquímicos e fotobiológicos, na quantidade de tempo essencial para cada indivíduo, vêm com ganhos psicológicos e físicos, como o estímulo da síntese de vitamina D, que está relacionada à saúde dos ossos, facilitando a absorção do cálcio, e consequentemente à prevenção de osteoporose. A exposição ao sol também previne doenças como artrite, diabetes tipo I, alguns tipos de cânceres e doenças autoimunes (CORRÊA, 2015; MUNHOZ et al., 2012; PURIM; LEITE, 2010; ROMBALDI, 2017).
A exposição à luz do sol também pode causar danos agudos e crônicos à pele humana, quando levado em consideração a intensidade da radiação baseada na latitude do local de exposição e da sensibilidade da pele que é um fato determinante já que depende diretamente da tonalidade da pele em questão (ROMBALDI, 2017).
O número de estudos epidemiológicos aponta a exposição excessiva aos raios solares, principalmente quando esta exposição ocorre durante a infância e adolescência, como o principal agente etiológico do câncer cutâneo. O aumento progressivo desses casos vem tornando-se um problema de saúde pública e interfere na qualidade de vida da população (MUNHOZ et al., 2012).
O estresse oxidativo gerado pela exposição à RUV é um dos fatores mais importantes e responsáveis pelos distúrbios e doenças documentadas, essas espécies reativas de oxigênio (ERO) podem sobrecarregar as células normais, levando-as a uma mudança de comportamento, carcinogênese e outros distúrbios cutâneos (NDIAYE et al., 2011).
A radiação UVA (R-UVA) é 20 vezes mais abundante, e tem uma importante contribuição na geração de ERO, levando a problemas como o fotoenvelhecimento precoce. Isso se deve ao fato de a R-UVA possuir um maior comprimento de onda, porém com menor energia, isso possibilita a penetração mais significativa da R-UVA na pele (BADEA et al., 2015). A R-UVA também está relacionada com a diminuição na quantidade de células de Langerhans e aumento na quantidade de células inflamatórias na derme (BALOGH; PEDRIALI; KANEKO, 2011; NDIAYE et al., 2011).
A radiação UVB (R-UVB) está ligada aos danos causados ao DNA, inflamação e carcinogênese, por apresentar um comprimento de onda menor que a R-UVA, com maior quantidade de energia, a R-UVB interage diretamente com o DNA das células, levando a mutação nos dímeros de pirimidina, associados ao câncer de pele não melanoma, e é responsável também por alguma fotodermatoses como a urticária solar (BALOGH; PEDRIALI; KANEKO, 2011; NDIAYE et al., 2011).
A radiação UVC (R-UVC) é a que apresenta a maior energia e por isso é letal para os seres vivos. Pode ser utilizada através de fontes artificiais para, por exemplo, purificar água por exemplo. A R-UVC não chega à superfície terrestre, isso uma vez que é absorvida pelo oxigênio presente na alta estratosfera (CORRÊA, 2015).
Segundo o INCA, para o Brasil, foi estimado que o risco de adquirir o câncer de pele não melanoma foi de 82,53 casos a cada 100 mil homens e 75,84 para cada 100 mil mulheres, para os anos de 2018 e 2019, sendo esse o câncer mais incidente em ambos os sexos no país. O câncer de pele do tipo não melanoma é caracterizado como basocelular e espinocelular, sendo estes, os tipos mais frequentes, dentre os acometidos, principalmente em pessoas de pele clara. Apresentando um bom prognóstico e altas taxas de cura quando tratados precocemente. (CEZAR-VAZ et al., 2015; INCA 2019).
Por esta razão, como a incidência de raios UV no norte e nordeste brasileiro é muito mais alta que o recomendado, inclusive no inverno, a prática de fotoproteção se torna essencial (ROMBALDI, 2017). O uso de roupas fotoprotetivas, chapéu de abas largas, óculos de sol, busca por sombra e principalmente a aplicação de filtros solares de amplo-espectro são de extrema importância no combate a essas doenças relacionadas à exposição aos raios UV (BALOGH; PEDRIALI; KANEKO, 2011).
2.2. FILTROS SOLARES
De acordo com a ANVISA, os protetores solares são definidos como qualquer preparação cosmética destinada a entrar em contato com a pele com finalidade exclusiva ou principal de protegê-la contra a radiação UVA e UVB, absorvendo, refletindo ou dispersando essa radiação. (BRASIL, 2012)
Os filtros solares são formulações cosméticas, para uso profilático e terapêutico, que impede os efeitos danosos da R-UV na pele. Eles são compostos por substâncias denominadas filtros orgânicos e inorgânicos, que agem dispersando, absorvendo ou refletindo a R-UV (BALOGH; PEDRIALI; KANEKO, 2011; REIS MANSUR et al., 2016).
Os filtros inorgânicos têm como exemplos o óxido de zinco e dióxido de titânio que são capazes de refletir e dispersar a R-UV por meio de uma barreira “física” opaca. Eles são considerados mais seguros clinicamente falando, mas possuem inconveniências como o esbranquiçado deixado na pele após a aplicação do produto (BALOGH; PEDRIALI; KANEKO, 2011; SCHALKA; REIS, 2011).
Os filtros orgânicos são moléculas capazes de absorver a radiação UV e transformá-la em energia na forma de calor, inócua para o ser humano. Essas moléculas são essencialmente aromáticas, elas podem fornecer proteções contra a R-UVA e R-UVB, funcionando como uma barreira química contra penetração da radiação UV na derme, porém os números de casos envolvendo alergias e irritação por parte dessas substâncias são vastas (BALOGH; PEDRIALI; KANEKO, 2011).
Combinações contendo filtros UV e extratos naturais para o uso em formulações cosméticas que podem atuar sinergicamente ou até sozinhas num fotoprotetor inovador e de origem natural vem sendo muito questionado recentemente (BERES et al., 2017; MERCURIO et al., 2015; VIOLANTE et al, 2009).
Devido aos seus benefícios para com a pele, por não causarem tantos efeitos indesejáveis quanto os filtros sintéticos, a demanda por filtros solares de origem natural vem sendo bastante expressa pelos consumidores. Destacando os extratos naturais como o da uva, que está presente em várias pesquisas por conta de sua ampla gama de moléculas bioativas que podem agir como fotoprotetoras (GLAMPEDAKI; DUTSCHK, 2014; LIM; ARELLANO-MENDOZA; STENGEL, 2017).
Na confecção de um filtro solar, a eficácia deste produto está relacionada ao tipo de veículo farmacêutico utilizado. A variedade de veículos disponíveis no mercado permite adequar-se aos requisitos exigidos pelos consumidores como as características sensoriais e boa permeação cutânea, alguns exemplos dessas formas farmacêuticas de uso tópicos são os cremes (emulsões), géis, loções, pomadas etc. (CHORILLI et al.,2009; SOUZA; FERREIRA, 2010).
No entanto para que o produto tenha a eficácia esperada é necessária a escolha criteriosa dos componentes que irão fazer parte deste, pois as características da formulação como espalhabilidade, emoliência, e resistência a água são delas decorrentes. Esses cuidados em torno da formulação não garantiram um produto de elevado FPS, esta condição está relacionada com a escolha do componente capaz de fornecer esta fotoproteção. (BERES et al., 2017; CHORILLI et al., 2009; MERCURIO et al., 2015; SOUZA; FERREIRA, 2010).
Segundo Johncoch (2000 apud CHORILLI et al., 2009, p.384) A fotoestabilidade é um tópico de grande discussão, visto que se o filtro não for foto estável poderá afetar o desempenho da formulação na liberação do fator de proteção.
Quando se diz respeito às formulações tópicas, as emulsões nos últimos anos vêm sendo muito utilizadas, seja para incorporação de fármacos (hidrossolúveis e lipossolúveis), ativos cosméticos. São consideradas sistemas termodinamicamente instáveis ou polifásico, por conter a presença de dois líquidos imiscíveis onde um representa a fase dispersa e a outra a fase dispersante, acrescido do tensoativo que une essas duas fases (CASTELI et al., 2008; FRANZOL; REZENDE, 2015; LANGE; HEBERLÉ; MILÃO, 2009).
Como dito anteriormente, a estabilidade de uma emulsão está diretamente relacionada com a escolha dos excipientes escolhidos, pertencentes à fase oleosa e aquosa, bem como do agente emulsificante escolhido para unir essas fases. O tamanho das gotículas que caracterizam a fase dispersa também tem grande influência no resultado do produto, pois pode acelerar uma separação de fases, efeito este não esperado ao se formular uma emulsão (FRANZOL; REZENDE, 2015; ZANIN et al.,2001)
As bases para cremes mais indicadas são as bases autoemulsionantes, a exemplo do creme Lanette que é aniônica. O álcool cetoestearílico 20OE é um exemplo de emulsificante não iônico, que vem substituindo cada vez mais os emulsificantes aniônicos, uma vez que o Lanette tem componentes que não são totalmente ácidos estáveis quando o pH é menor que 2,5 e são incompatíveis com tensoativos catiônicos como os sais de metais polivalentes (sais de zinco, chumbo, estanho, alumínio) e por causar problemas dermatológicos, porém as bases aniônicas quando não houver as incompatibilidades citadas acima ainda são de primeira escolha por promoverem melhor penetração cutânea (ZANIN et al., 2001).
Essa noção de estabilidade é dada com base no tempo necessário que uma emulsão leva para a separação de fases, ocorrido esse que pode levar minutos, ou seja, logo após a sua formulação, ou anos. Através do teste de estabilidade acelerada é possível verificar se a emulsão se apresenta estável para atingir o sucesso terapêutico esperado. Esse teste é feito em condições específicas e controladas, conseguindo-se respostas em tempo útil sobre o comportamento da emulsão estudada (FRANZOL; REZENDE, 2015; LANGE; HEBERLÉ; MILÃO, 2009)
Enfim, quando falamos da confecção de filtros solares, os veículos mais empregados são as emulsões por apresentarem vantagens como a formação de película epicutâneo espessa sobre a pele, garantindo a maior fixação do produto, a resistência a água, a compatibilidade com diferentes faixas de pH e a possibilidade da incorporação de filtros hidrossolúveis e lipossolúveis que podem atuar sinergicamente num cosmético, e se adaptando bem a incorporação de um extrato que conta com um conjunto de moléculas diferentes entre si (SOUZA; CAMPOS; PACKER, 2013).
2.3. O BAGAÇO DA UVA E SUA APLICABILIDADE NOS FILTROS SOLARES
O apelo por cosméticos naturais, também conhecidos pelo termo “new care”, por conta de sua melhor adaptação a pele é crescente. Por isso, o uso de extratos e óleos oriundos de vegetais vem sendo utilizados para estudos na aplicação de cosméticos, como os filtros solares principalmente por conta das pesquisas envolvendo analogias estruturais entre moléculas fotoprotetivas sintéticas e os princípios ativos de origem vegetal apresentando efeito antissolar (BADEA et al., 2015; MERCURIO et al., 2015; VIOLANTE et al., 2009)
A presença de uma vasta gama de moléculas bioativas nos vegetais, como a uva, é conhecida e aplicada na geração de novas tecnologias de produção cosmética e farmacêutica, por seus efeitos antioxidantes, cardioprotetoras, anti-inflamatórias, antimicrobianas, antienvelhecimento anticancerígenas (MARIÉLI KARLING, NATHALIE MERLIN; OLDONI, 2017; MUNHOZ et al., 2012; PINTAĆ et al., 2018).
Estudos comprovaram que a uva é uma fonte rica em numerosos compostos benéficos para a saúde humana, tais como vitaminas, ácidos orgânicos, minerais e os mais importantes, os polifenóis como os flavonoides, antocianinas, estilbenos e compostos aromáticos como terpenos e ésteres amplamente distribuídos na pele, sementes, hastes e folhas de uva (GLAMPEDAKI; DUTSCHK, 2014; PINTAĆ et al., 2018).
Um exemplo expressivo entre as moléculas presentes na uva é o resveratrol, um composto fenólico do grupo dos flavonoides. O resveratrol está presente em cerca de setenta espécies vegetais e é especialmente encontrado na uva em abundância, nas suas duas formas isoméricas, principalmente na casca da fruta, tem efeitos antioxidantes expressivos e por isso é estudado largamente (LANGE; HEBERLÉ; MILÃO, 2009)
O efeito antioxidante dessas moléculas tem a capacidade de reduzir a produção de ERO e atividade sequestradora de radicais livres, produzidas principalmente pela R-UVA, evitando assim danos às células e consequentemente os efeitos ocasionados por esses danos (BALOGH; PEDRIALI; KANEKO, 2011; MUNHOZ et al., 2012).
Essas moléculas possuem cromóforos, o que é de fundamental importância para a ação fotoprotetora, capazes de absorver a R-UV e liberar essa energia na forma de calor, que não é capaz de causar danos às células. Dessa maneira, protege a pele dos efeitos fotoquímicos causados pela R-UV (BADEA et al., 2015; BALOGH; PEDRIALI; KANEKO, 2011; COSTA et al., 2015; DUARTE; BUENSE; KOBATA, 2006; MUNHOZ et al., 2012). A possibilidade de uso desses extratos no desenvolvimento de filtros solares inovadores é bastante vantajosa, visto os benefícios descritos por essas moléculas bioativas, além do interesse por parte dos consumidores no uso desse material de origem natural e por trazer vantagens econômicas para a cadeia de produção das empresas vinícolas (BADEA et al., 2015; BERES et al., 2017; COSTA et al., 2015).
2.4. O REAPROVEITAMENTO DE RESÍDUOS NA CADEIA DE PRODUÇÃO INDUSTRIAL DE EMPRESAS VINÍCOLAS
A uva (Vitis spp.) é umas das frutas mais valorizadas no mundo, podendo ser consumida crua ou na confecção de outros produtos. Ela conta com um alto teor de fitonutrientes benéficos para a saúde, o que corrobora como fato dela estar listada como uma das frutas mais extensamente cultivadas, contando com uma vasta gama de produtos derivados dela, tais como sumos frescos, passas, geleias, vinagre e vinho (MENEZES et al., 2018; PINTAĆ et al., 2018)
A grande porcentagem de uva destinada a produção de vinho (cerca de 71%) leva a uma produção de cerca 12 milhões de toneladas de resíduos por ano, 75% desses resíduos correspondentes as semente e pele das uvas, essa grande quantidade de resíduo é considerada um problema ambiental, visto que grande parte não é reutilizada para outros fins (BERES et al., 2017; MENEZES et al., 2018).
Durante o processo de vinificação, grande parte das moléculas bioativas presentes na uva in natura ficam retidas no bagaço (pele, semente e haste). Sendo de grande interesse a aplicação desse material na fabricação de produtos inovadores farmacêuticos, cosméticos e alimentícios (BERES et al., 2017).
Segundo Dwyer, hosseinian e rod, (2014) “O potencial de mercado do bagaço de uva no Canadá mostra que, se cada grama de pele de bagaço vermelho for vendido, há um lucro de aproximadamente 448 milhões de euros […]” Demonstrando, desta forma, o quanto pode ser rentável a reutilização desses resíduos na aplicação de outras atividades.
Diante do que foi estudado em relação à composição química da uva, a ampla presença de moléculas aromáticas e com ação antioxidante presentes principalmente no bagaço de uva, e por ser uma fonte renovável e rentável como matéria-prima, se torna de grande interesse o uso desse material na confecção de um novo filtro solar (BERES et al., 2017; MENEZES et al., 2018).
3. METODOLOGIA
3.1. TIPO DE ESTUDO E LOCAL DE PESQUISA
Esta é uma pesquisa experimental, quantitativa, com objetivo exploratório e descritivo. O ambiente de coleta foi no laboratório de farmacotécnica (LABTEC) para a maceração do bagaço seco da uva e manipulação dos cosméticos, laboratório de química orgânica para a secagem do material e o laboratório de farmacognosia da Universidade Federal do Vale do São Francisco – UNIVASF campus sede Petrolina, este estudo foi realizado através de análises in vitro.
TABELA 1 – Equipamentos utilizados no desenvolvimento da pesquisa.
EQUIPAMENTOS UTILIZADOS PHmetro Analítica – Marca MS Tecnopon® Instrumentação Chapa aquecedora – Marca: Fisatom® Viscosímetro – Marca Quimis® Refrigerador – Marca: Consul® / Modelo CRM45 Centrífuga semiautomática – Marca Centribio® Estufa – Marca: Americanlab® / Modelo AL 100/100 Espectrofotômetro U2M – Marca Quimis ® Ultra purificador de água Heal Force® modelo Smart-P Balança analítica digital Bioscale® modelo FA2204B; Evaporador rotativo – Ethik Technor®/ modelo 420 TD
Fonte: Próprio autor, 2023.
3.2. OBTENÇÃO DO MATERIAL VEGETAL
Os resíduos da vinificação (bagaços) da uva (Vitis vinífera) foram disponibilizados pela Embrapa Semiárido de Petrolina-PE por meio da pesquisadora Dra. Aline Camarão Telles Biasoto. A variedade do bagaço de uva recebido é a Syrah, a determinação da variedade foi determinada de acordo com a época do ano e das condições climáticas que favoreceram a cultivo dessa variedade.
3.2.1. Secagem do bagaço da uva
O material recebido foi secado em estufa de circulação de ar a uma temperatura de 40°C por 72 h. O resíduo seco obtido foi acondicionado em recipientes apropriados e armazenados em refrigerador a 4°C até o momento de sua utilização.
3.2.2. Obtenção do extrato
Com auxílio de um béquer de plástico transferiu-se o bagaço para o percolador, após atingir a quantidade necessária de bagaço a mesma foi imersa em solução etanólica 70% (v/v) e o percolador foi fechado. Foi utilizado um Erlenmeyer em volta de papel alumínio para a coleta do extrato fluido, a solução extrativa fluída obtida foi concentrada com o auxílio de um evaporador rotativo sob pressão reduzida a 45° C a 6 rpm resultando no extrato etanólico bruto (EEB).
Foram utilizados 443,16 g de extrato seco no percolador e para essa quantidade 1,3 L de etanol 70% foi utilizado para realizar a extração pelo método de percolação durante 72 h. Logo em seguida, foi feita a secagem em evaporador rotativo do extrato fluído obtido, resultando em 45,0 g de EEB utilizado para a incorporação nas bases galênicas e para aferição de absorbância em espectrofotômetro.
3.2.3. Manipulação das emulsões
As duas bases galênicas (emulsões O/A) propostas, uma com emulsificante não-iônico, álcool cetoestearílico 20 OE, e outra base autoemulsionante aniônica Lanette, foram preparadas seguindo a mesma metodologia de emulsificação a quente. Em recipientes separados, uma contendo a fase oleosa e outra a fase aquosa, foram ambas aquecidas a 75 °C (5 °C). Posteriormente, a fase aquosa foi adicionada lentamente sobre a oleosa com agitação constante, após homogeneização as preparações foram resfriadas em constante agitação até temperatura ambiente e acondicionadas em frascos plásticos. Todas as formulações foram preparadas em triplicata.
3.2.4. Incorporação do extrato na base
O EEB foi incorporado às bases galênicas 72 h após as suas manipulações, tempo este suficiente para elas estabilizarem (maturar) segundo estudos prévios realizados pelo grupo de pesquisa de iniciação científica (2017 – 1018). O EEB foi incorporado numa quantidade correspondente a 5% (m/m) em ambas as bases galênicas. As manipulações das emulsões foram feitas em triplicata, com formulações controle, ou seja, que não receberam o EEB, enquanto as formulações com EEB foram denominadas de amostras.
3.3. AVALIAÇÃO DAS EMULSÕES OBTIDAS
No tempo inicial (Ti) foram feitas as análises das características organolépticas das emulsões, avaliação da viscosidade, determinação de pH e FPS, assim que concluídos esses testes deu-se início ao estudo de estabilidade com ciclo de gelo e degelo durante 15 dias e considerado como tempo final (Tf), onde novamente foram realizadas essas análises mencionadas anteriormente no Ti e incluído o teste de centrífuga.
3.3.1. Características organolépticas das formulações
Para a avaliação das características organolépticas no Ti e Tf, foram observados e analisados quesitos como; odor, cor e observação de como as emulsões se comportava macroscopicamente, como; sinais de instabilidade características de sistemas emulsionados grosseiros, os quais são cremagem, floculação, separação de fases ou inversão de fases. As amostras consideradas estáveis macroscopicamente passaram para a próxima fase de testes preliminares.
3.3.2. Comportamento reológico
Com o auxílio do viscosímetro rotativo observou-se a viscosidade das formulações obtidas, tanto controle quanto amostra, no Ti e Tf para comparação dos resultados, utilizando o spindle de número 4, entre 10 e 60 rotações por minuto (RPM) com intervalos de 10 RPM. Assim foi obtido o valor de viscosidade relativa que corresponde à velocidade/força de cisalhamento das emulsões frente ao fluxo sendo possível constatar o comportamento dos sistemas quanto aos modos newtonianos e não newtonianos. Os resultados foram expressos como média desvio padrão das análises em triplicata.
3.3.3. Determinação do fator de proteção solar (FPS)
Foram realizadas análises espectrofotométricas para determinação de FPS segundo metodologia descrita por Mansur e colaboradores (1986) com algumas modificações. As amostras foram analisadas em comprimento de onda entre 290 a 320 nm com intervalos de 5 nm em espectrofotômetro UV/VIS, usando cubeta de quartzo de 1,0 cm de caminho óptico. As absorbâncias foram adicionadas a equação de MANSUR para obtermos o valor do FPS in vitro. Foram também analisadas espectrofotometricamente as bases sem o EEB, bem como o do próprio EEB puro. O etanol foi usado como solvente (branco) e para diluir as amostras. Os testes foram realizados em triplicata, resultados expressos em média desvio padrão.
3.3.4. Potencial hidrogeniônico (pH)
A determinação do pH foi realizada em uma dispersão aquosa de 10% (m/m) da amostra em água destilada, usando pHmetro digital previamente calibrado com soluções tampão 4,0 e 6,86 de acordo com a Farmacopeia Brasileira (2010). Esse teste foi realizado para as formulações controle e amostra, em Ti e Tf. Os resultados foram expressos como média desvio padrão das análises em triplicata.
3.3.5. Estabilidade acelerada
Foi realizado ciclo de gelo e degelo alternantes para todas as formulações desenvolvidas. A cada 24 h, as formulações alternavam pela estufa a temperatura de 40 a 20°C, e pela geladeira na temperatura de 4 a 20°C. Ao final de 15 dias (Tf) nessas condições de temperatura, para observação do comportamento das bases galênicas ao passarem por estresses de temperatura (calor e frio) que simulam estresses de deslocamento, estocagem e vida na prateleira.
3.3.6. Teste de centrífuga
O teste de centrífuga foi realizado em tubos de ensaio cônicos, para todas as formulações obtidas, 5,0 g das amostras foram pesadas e então submetidas a ciclo de 3.000 RPM por 30 min em centrifuga a temperatura ambiente. Esse teste foi realizado somente no Tf, pois de acordo com estudos prévios de comportamento dessas bases galênicas não foi necessária à realização desse teste no Ti (BRASIL, 2004).
4. RESULTADOS E DISCUSSÕES
4.1. ESTUDO DA ESTABILIDADE DAS FORMULAÇÕES
O estudo da estabilidade das formulações foi realizado em Ti e Tf, que corresponde ao teste de estabilidade acelerada que durou 15 dias. Para análise das mudanças dos critérios avaliados e comparação dos resultados obtidos com ciclo de gelo e degelo.
4.1.1. Análise das formulações no Ti
Observou-se, como esperado, que antes da adição do EEB nas bases, os cremes apresentavam coloração branca opaca, tanto para a emulsão aniônica quanto para não iônica, e após a incorporação do EEB, ambas as formulações adquiriram coloração roxa, característica do EEB, como mostrado na Figura 1.
Figura 1. Aspecto colorativo das formulações com emulsionantes ânionico (esquerda) e o não iônico (direita). NO Ti, antes do teste de estabilidade acelerada.
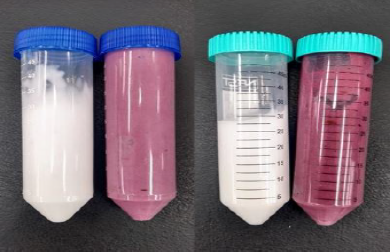
Fonte: Próprio autor, 2023.
Em relação ao odor das formulações, a base que continha o emulsionante não iônico não apresentava cheiro característico, ao contrário da base aniônica que se apresentava com um cheiro mais acentuado, característico de ácido graxo. Para os dois tipos de formulações ao se adicionar o EEB elas passaram a ter o odor característico do extrato, ou seja, de uva.
Com relação ao pH, foi constatado que com a adiação do EEB, o pH diminui consideravelmente, mesmo levando-se em consideração que o pH das bases sem o EEB já é considerado baixo, Tabela 2.
TABELA 2 –Valores de pH das formulações aniônica e não iônica em Ti e Tf.
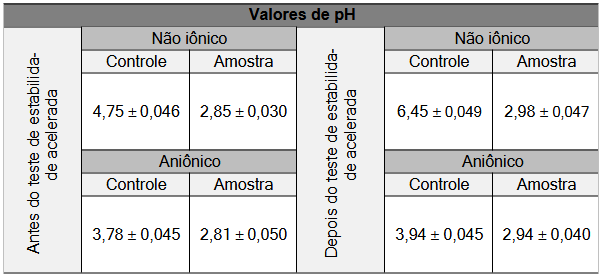
Fonte: Próprio autor, 2023.
Na análise da viscosidade em Ti, uma característica observada foi que as formulações não iônicas apresentavam um valor de viscosidade significativamente mais elevado do que a das formulações aniônicas como pode ser visto na Tabela 3, isso demonstra que a velocidade de sedimentação da formulação é menor e isso é um fato interessante, pois quanto menor a velocidade de sedimentação melhor será a estabilidade física do produto, uma vez que a velocidade de sedimentação aumentada pode acelerar também um possível processo de instabilidade da formulação resultando em forte coalescência e separação de fases (FRIEDRICH et al, 2007).
De acordo com a análise dos Gráficos 1 a 4, os dois tipos de formulações demonstraram comportamento não newtoniano, ou seja, há diminuição nos valores de viscosidade com o aumento da força de cisalhamento sobre a preparação, mostrando características pseudoplásticas, pois elas não precisam atingir um limiar para que haja mudança no valor de viscosidade. Pôde ser observado também que os valores de viscosidade para a formulação aniônica mudam levemente do controle para a amostra, demonstrando que a adição do extrato teve influência sobre a viscosidade da base aniônica, não houve mudança significativa para a formulação não iônica (FRIEDRICH, 2007; PRESTES et al., 2009).
TABELA 3 – Valores de viscosidade das formulações aniônica e não iônica em 50 RPM, em Ti e Tf.
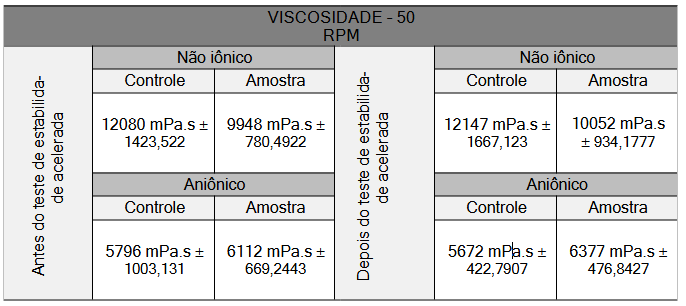
Fonte: Próprio autor, 2023.
Gráfico 1: Comportamento reológico da formulação não iônica, CONTROLE, em Ti.
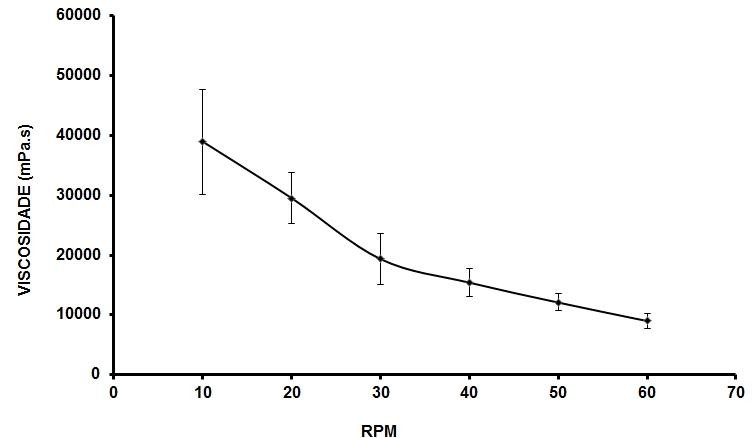
Fonte: Próprio autor, 2023.
Gráfico 2: Comportamento reológico da formulação não iônica, AMOSTRA, em Ti.
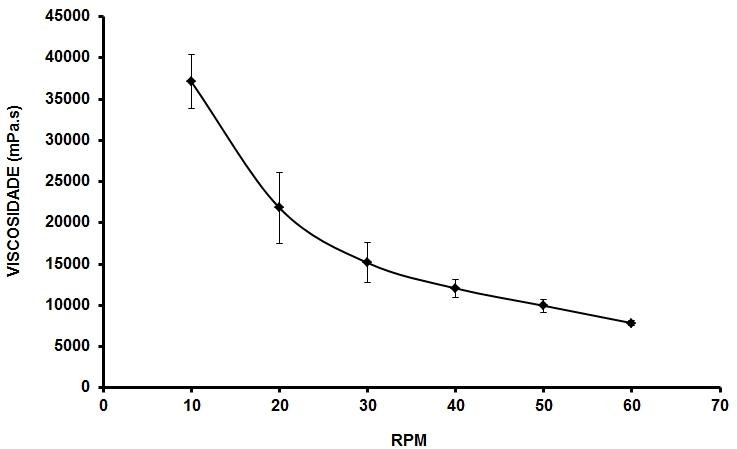
Fonte: Próprio autor, 2023.
Gráfico3: Comportamento reológico da formulação aniônica, CONTROLE, em Ti.
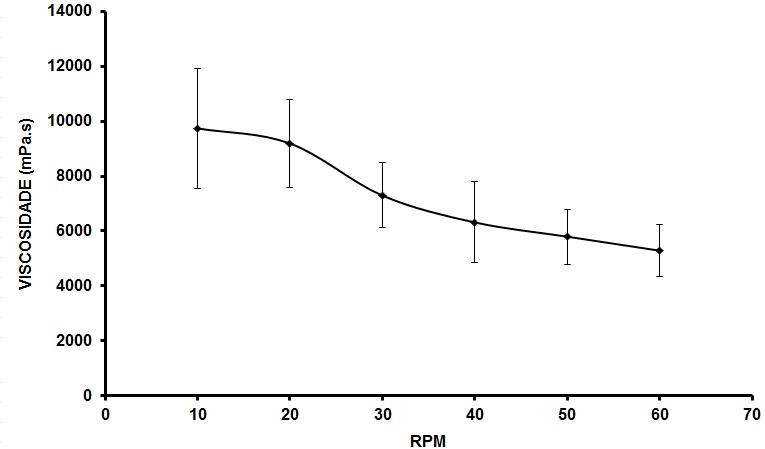
Fonte: Próprio autor, 2023.
Gráfico4: Comportamento reológico da formulação aniônica, AMOSTRA, em Ti.
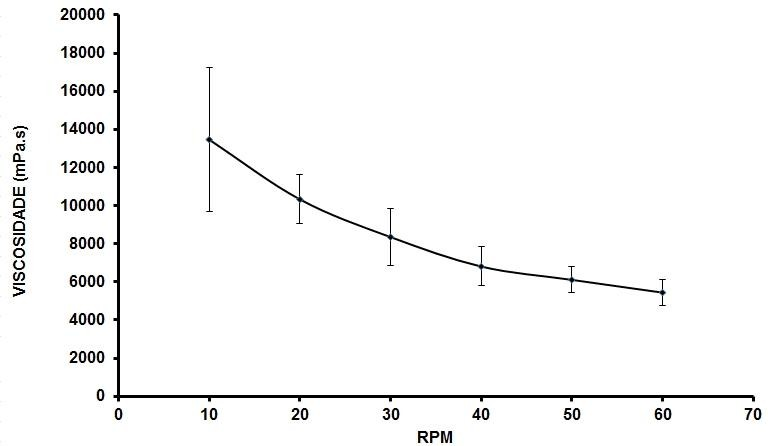
Fonte: Próprio autor, 2023.
Na análise dos resultados de FPS, foi observado que para as formulações amostra, devido ao extrato vegetal, houve resultados significativos de FPS com a adição do EEB, o que poderia ser relacionado a uma possível atividade fotoprotetora como pode ser visto na Tabela 4, ao contrário das bases sem o EEB que, como esperado, não demonstraram resultados de FPS relevantes.
Tabela 4: Valores de FPS das formulações aniônica e não iônica, em Ti e Tf.
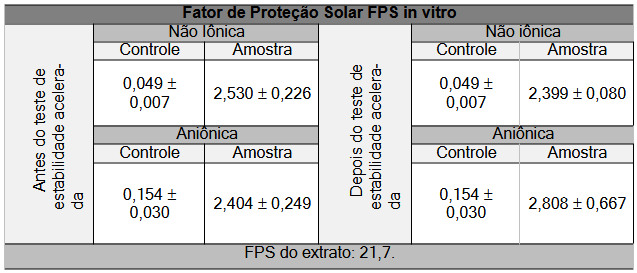
Fonte: Próprio autor, 2023.
4.1.2. Análise das formulações em Tf
Com relação às características organolépticas em Tf, foi observado que as formulações amostra (com EEB) perderam a coloração roxa que tinham em tempo inicial, tornando-se amarronzadas (Figura 2), o que foi visto principalmente na formulação aniônica, sendo, possivelmente resultado da presença de cargas negativas livres que levam a reações de oxidação mais facilmente, sendo também uma reação comum aos ácidos graxos, ou dos produtos deles formulados, a peroxidação lipídica pode levar a alterações de cor e odor, bem como a gostos característicos quando se trata de alimento que contem essas substâncias, assim alguns pontos são levados em consideração ao se estudar a estabilidade de produtos, como por exemplo, o processo de fabricação, tempo, temperatura, umidade, possíveis microrganismos, luz e principalmente a presença de oxigênio no meio podem estar diretamente relacionados à oxidação do produto. Uma solução é possível corrigir tais problemas modificando as concentrações de antioxidantes como o BHT comumente utilizado em formulações cosméticas, mesmo que a própria uva contenha antioxidantes em sua composição como o resveratrol, uma correção seria necessária (CHORILLI; LEONARDI; SALGADO, 2007; LANGE; HEBERLÉ; MILÃO, 2009; SALVADOR; JUNIOR; CHIARI-ANDRÉO, 2016).
Figura 2. Aspecto colorativo das formulações com emulsionantes ânionico (esquerda) e o não iônico (direita). NO Tf, depois do teste de estabilidade acelerada.
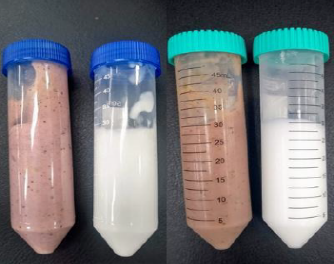
Fonte: Próprio autor, 2023.
De acordo com o guia de estabilidade dos produtos cosméticos da ANVISA (2004), uma das incompatibilidades químicas que podem ser visualizadas são as reações de óxido-redução, responsáveis por alterações nas atividades das substâncias ativas e das características organolépticas e físicas da formulação.
Em relação ao odor, no Tf foi observado que após o teste de estabilidade acelerada o cheiro característico do EEB ficou um pouco mais acentuado juntamente com o cheiro rançoso proveniente dos ácidos graxos presentes na base aniônica.
Na análise do pH foi observado aumento no valor do pH, tanto para a emulsão aniônica, quanto para a não iônica, sugerindo que com o ciclo de gelo e degelo, além das reações de oxidação que pôde ser constatada a olho nu, componentes responsáveis pela acidez foram degradados ou passaram por reações tornando mais alcalina as formulações. Reações como a hidrolise, visto que os cremes são O/A, ou seja, a sua maior composição é a água, oxidação como citada anteriormente ou até mesmo contaminação bacteriana podem influenciar o pH. Outros fatores que podem influenciar no valor do pH das formulações é a polaridade da fase oleosa e o pH do meio versus o pH do extrato, visto que o pH diminui consideravelmente com a adição do extrato nas bases galênicas, como mostra a Tabela 2, característica essa vista em outros trabalhos que também incorporavam extratos em emulsões (LANGE; HEBERLÉ; MILÃO, 2009; MUNHOZ et al., 2012; SOUZA; CAMPOS; PACKER, 2013).
No guia de estabilidade dos produtos cosméticos (ANVISA, 2004) é dito que em relação a valores alterados de pH, três fatores devem ser levados em consideração: a estabilidade dos ingredientes da formulação, a eficácia e a segurança do produto cosmético quando se leva em conta o pH da pele.
Mesmo com o pH da formulação tendo aumento depois do ciclo de gelo e degelo, para os dois tipos de formulações, ainda seriam necessárias interferências para correção desse pH, pois ambas as formulações se mantêm aquém dos limites de pH do manto da pele que é de 4,6 a 5,8, e nesse caso, substâncias como a trietanolamina são recomendadas para aumentar o pH de formulações e torná-la suscetível ao uso do consumidor (MUNHOZ et al., 2012).
Com relação à viscosidade, no Tf as formulações não demonstraram alterações significativas, mas houve um leve aumento nos valores quando comparados ao Ti, continuaram com comportamento não newtoniano e pseudoplásticas, Gráficos 5 a 8. O estudo da viscosidade é fundamental, pois o comportamento das formulações está diretamente relacionado aos critérios de aceitação do consumidor, influenciando nas características sensoriais de tato e espalhabilidade sobre a pele, e se a sensação não for agradável para quem estar fazendo uso do produto dificilmente ele será usado regularmente, influenciando na liberação dos princípios ativos presentes no produto e assim, consequentemente, não alcançando o resultado esperado para o consumidor. (PRESTES, et al).
Gráfico 5: Comportamento reológico da formulação não iônica, CONTROLE, no Tf.
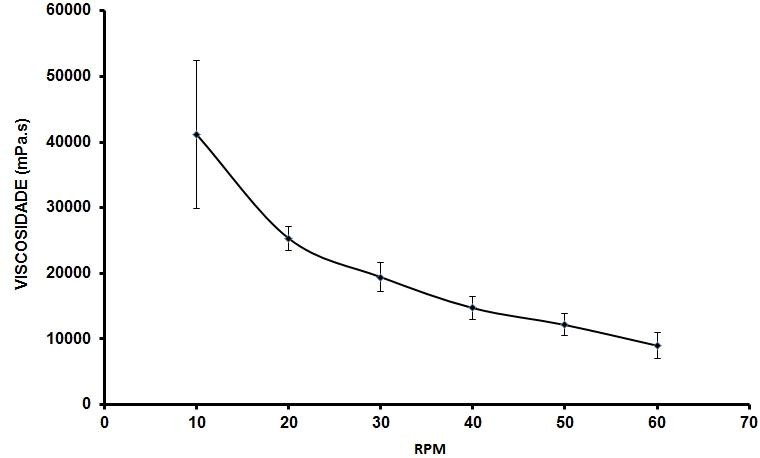
Fonte: Próprio autor, 2023.
Gráfico 6: Comportamento reológico da formulação não iônica, AMOSTRA, no Tf.
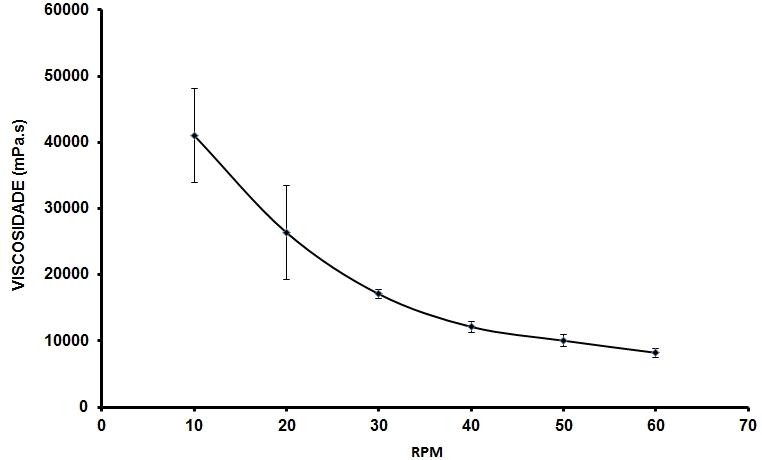
Fonte: Próprio autor, 2023.
Gráfico 7: Comportamento reológico da formulação aniônica, CONTROLE, no Tf.
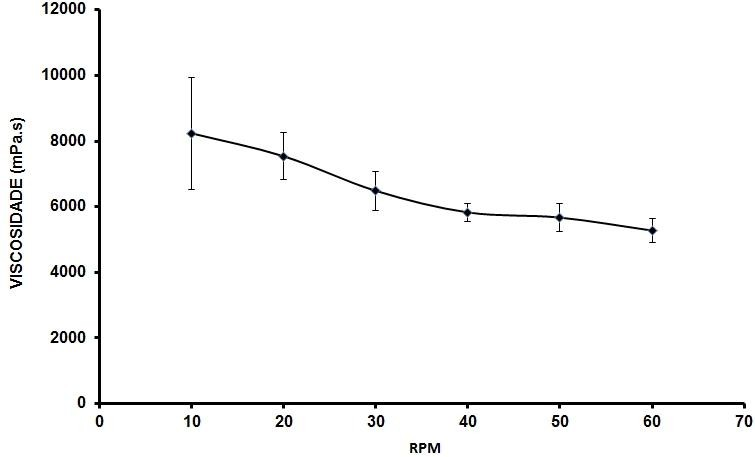
Fonte: Próprio autor, 2023.
Gráfico 8: Comportamento reológico da formulação aniônica, AMOSTRA, no Tf.
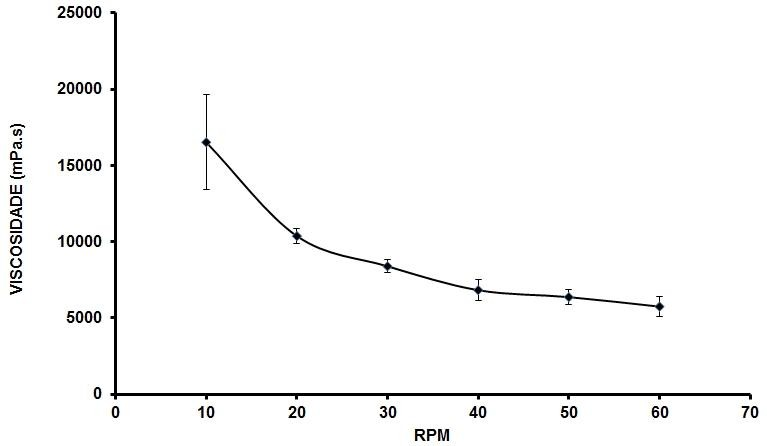
Fonte: Próprio autor, 2023.
Analisando o resultado de FPS das formulações (Tabela 4) pôde-se chegar à conclusão de que com o ciclo de gelo e degelo houve leve alteração nos valores das formulações não iônica com o EEB, o valor diminuiu de 2,53 para 2,39, essa pequena diferença é explicada primeiro por conta da alteração do pH das formulações que pode levar a deslocamentos batocrômicos ou hipsocrômicos que pode causar deslocamentos na banda de absorção para um comprimento de onda. Outra explicação a essa mudança de FPS é uma possível incompatibilidade da base creme não iônica com o extrato levando a uma degradação dos compostos responsáveis pela atividade fotoprotetora do extrato que resultou na diminuição do FPS da amostra, visto que o valor de absorbância do controle continuou sem alterações (MUNHOZ, et al., 2012).
Isso não foi observado na base creme aniônica que por sua vez teve um discreto aumento de FPS para amostra depois do ciclo, provavelmente não havendo degradação dos compostos responsáveis pela atividade fotoprotetora, mas essa mudança no valor mais uma vez pode ser explicada pelo efeito de deslocamento das curvas de absorção em relação a ondas de comprimento provocados pela alteração do pH (MUNHOZ, et al., 2012).
A ANVISA (BRASIL, 2012) estabelece que os valores de FPS de fotoprotetores comercializados só podem ser atestados por meio de métodos in vivo e para que um produto seja comercializado como filtro solar, segundo a RDC 30/2012, esta precisa ter o FPS de no mínimo 6.
O teste de centrifuga, feito somente no Tf, pois segundo estudos prévios realizados pelo grupo com as bases galênicas em estudo nesse trabalho juntamente com o EEB demonstraram que não havia alteração no Ti, já que as bases incorporaram bem ao extrato. Esse teste tem por finalidade aumentar a força de gravidade, com o aumento da movimentação das partículas do sistema fornecendo informações sobre a sua estabilidade de forma antecipada e assim antecipando também processos de floculações que podem gerar uma possível coalescência, sendo indicativa da necessidade de reformulação. No caso das formulações desse trabalho, elas não mostraram separação de fase a olho nu, para nenhum dos dois tipos de formulações, tanto controle quanto amostra, demonstrando que mesmo sob condições de estresse mecânico as bases galênicas permaneceram estáveis, como pode ser visto na Figura 3 (BRASIL, 2004; CASTELI, V. C. et al., 2008; FRIEDRICH, et al.; 2007; SOUZA; FERREIRA, 2010).
Figura 3. Formulações controle e amostra, em Tf, antes e depois de passar pela centrífuga, respectivamente, a esquerda corresponde a base aniônica e a da direita a base não iônica.
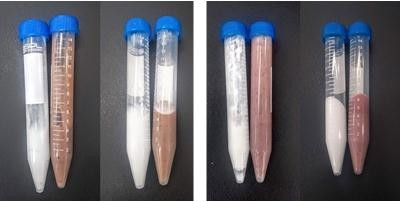
Fonte: Próprio autor, 2023.
Com os resultados obtidos observamos que o extrato se adaptou bem aos dois tipos de bases galênicas, quando avaliamos a sua resposta ao teste de centrifuga e a viscosidade, visto que não houve separação de fases e que elas mantiveram sua viscosidade mesmo após o teste de estabilidade acelerada, demonstrando que permaneceram estáveis mesmo após o estresse do frio e calor. Porém é importante mencionar que houve incompatibilidades químicas entre os componentes das bases e do extrato visto que ocorreram reações de oxidação, observado principalmente na base aniônica onde a susceptibilidade de ocorrência dessas reações são maiores por conta da presença de cargas livres. Essas reações químicas que ocorreram nas bases com o teste de estabilidade acelerada também provocaram alterações nos valores de pH e consequentemente do FPS, que como mencionado anteriormente é responsável pelos deslocamentos batocrômicos e hipsocrômicos.
5. CONCLUSÃO
Em relação ao FPS, o método utilizado neste estudo para medir o FPS, só media para a banda UVB, ou seja, não sabemos como seria o comportamento das moléculas do extrato em relação absorção na banda UVA e mesmo com os valores baixos de FPS, deve-se levar em consideração que no extrato há uma mistura variada de moléculas com inúmeros efeitos e por isso não tem como saber qual a concentração das moléculas com ação fotoprotetiva, porém sabe-se, de acordo com os resultados desse trabalho, que há sim viabilidade no uso do extrato em produtos cosméticos, mesmo com os valores abaixo de 6, que é o mínimo exigido pela ANVISA para os filtros solares, produtos multiuso que prometam uma proteção solar como os bronzeadores e protetores labiais, devem ter no mínimo um valor de FPS de 2, assim estudos na utilização desse extrato na confecção de algum desses cosméticos ou agindo sinergicamente com outros filtros químicos sintéticos são necessários. Outra questão que deve ser pontuada é a concentração do EEB nas bases, que correspondia a 5%, assim, estudar um aumento na concentração desse EEB nas bases também se torna uma boa alternativa.
REFERÊNCIAS
ANVISA. AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA. Farmacopeia Brasileira, volume 1. 5ª Ed. Brasília, 2010b.
BRASIL. Ministério da saúde. Agência Nacional de Vigilância Sanitária. Resolução da diretoria colegiada – RDC nº 30, de 1 de junho de 2012. Aprova o Regulamento Técnico Mercosul sobre Protetores Solares em Cosméticos e dá outras providencias. Diário Oficial da União 4 de junho de 2012.
Brasil. Agência Nacional de Vigilância Sanitária – ANVISA. Guia de estabilidade de produtos cosméticos. v.1. Brasília; 2004.
BADEA, G. et al. Use of various vegetable oils in designing photoprotective nanostructured formulations for UV protection and antioxidant activity. Industrial Crops and Products, v. 67, p. 18–24, 2015.
BALOGH, T. S.; PEDRIALI, C. A.; KANEKO, T. M. Proteção à radiação ultravioleta: recursos disponíveis na atualidade em fotoproteção. v. 1, p. 732–742, 2011.
BERES, C. et al. Towards integral utilization of grape pomace from winemaking process: A review. Waste Management, v. 68, p. 581–594, 2017.
CASTELI, V. C. et al. Desenvolvimento e estudos de estabilidade preliminares de emulsões O/A contendo Cetoconazol 2,0%. Acta Scientiarum. Health Sciences, v. 30, n. 2, p. 121-128, 2008.
CARDOSO, F. A. DE M. E S. et al. Prevalence of photoprotection and its associated factors in risk group for skin cancer in Teresina, Piaui. Anais Brasileiros de Dermatologia, v. 92, p. 206–210, 2017.
CEZAR-VAZ, M. R. et al. Skin cancer in rural workers: Nursing knowledge and intervention. Revista da Escola de Enfermagem, v. 49, n. 4, p. 563–570, 2015.
CHORILLI, M. et al. Avaliação Sensorial de Formulações Fotoprotetoras Contendo Filtro Solar de Amplo Espectro. Latin American Journal of Pharmacy, v. 28, n. 3, p. 383-392, 2009.
CHORILLI, M.; LEONARDI, G. R.; SALGADO, H. R. N. Radicais livres e antioxidantes: conceitos fundamentais para a adição em formulações farmacêuticas e cosméticas. Rev Bras Farm, v. 88, n. 3, p. 113-118, 2007.
CORRÊA, M. DE P. Solar ultraviolet radiation: properties, characteristics and amounts observed in Brazil and South America. An Bras Dermatol, v. 90, n. 3, p. 297–313, 2015.
COSTA, S. C. C. et al. In vitro photoprotective effects of Marcetia taxifolia ethanolic extract and its potential for sunscreen formulations. Brazilian Journal of Pharmacognosy, v. 25, n. 4, p. 413–418, 2015.
DUARTE, I.; BUENSE, R.; KOBATA, C. Fototerapia. Anais Brasileiros de Dermatologia, v. 81, n. 1, p. 74–82, 2006.
DWYER, K.; HOSSEINIAN, F.; ROD, M. The Market Potential of Grape Waste Alternatives. Journal of Food Research, v. 3, n. 2, p. 91, 2014.
FRANZOL, A.; REZENDE, M. C. Estabilidade de emulsões: um estudo de caso envolvendo emulsionantes aniônico, catiônico e não-iônico. Revista Polímeros, v. 25, p. 1-9, 2015.
FRIEDRICH, M. et al. Avaliação da estabilidade físico-química de creme não iônico inscrito no formulário nacional. Latin American Journal of Pharmacy, v. 26, n. 4, p. 558-562, 2007.
GLAMPEDAKI, P.; DUTSCHK, V. Stability studies of cosmetic emulsions prepared from natural products such as wine, grape seed oil and mastic resin. Colloids and Surfaces A: Physicochemical and Engineering Aspects, v. 460, p. 306–311, 2014.
Inca.gov.br [Internet]. Instituto Nacional de Câncer José Alencar Gomes da Silva. Coordenação de Prevenção e Vigilância. Estatística 2018. Rio de Janeiro: INCA, 2019. 124p. [acesso 28 de janeiro de 2019]. Disponível em: [https://www.inca.gov.br/tipos-de-cancer/cancer-de-pele-nao-melanoma#main-content].
LANGE, M. K.; HEBERLÉ, G.; MILÃO, D. Avaliação da estabilidade e atividade antioxidante de uma emulsão base não-iônica contendo resveratrol. Brazilian Journal of Pharmaceutical Sciences, v. 45, n. 1, 2009.
LIM, H. W.; ARELLANO-MENDOZA, M. I.; STENGEL, F. Current challenges in photoprotection. Journal of the American Academy of Dermatology, v. 76, n. 3, p. S91–S99, 2017.
LORIGO, M.; MARIANA, M.; CAIRRAO, E. Photoprotection of ultraviolet-B filters: Updated review of endocrine disrupting properties. Steroids, n. September 2017, p. 46-58, 2018.
MANSUR, J.S.; BREDER, M.N.R.; MANSUR, M.C.d’A.; AZULAY, R.D. Determinação do fator de proteção solar por espectrofotometria. An. Bras. Dermatol., v. 61, n.3, p. 121-124, 1986.
MARIÉLI KARLING, NATHALIE MERLIN, D. C. S.; OLDONI, T. L. C. Estudo do potencial antioxidante do bagaço de uva utilizando técnica de fracionamento líquido-líquido. Synergismus scyentifica UTFPR, v. 12, p. 88–93, 2017.
MENEZES, M. L. DE et al. Phenomenological determination of mass transfer parameters of oil extraction from grape biomass waste. Journal of Cleaner Production, v. 176, p. 130–139, 2018.
MERCURIO, D. G. et al. In vivo photoprotective effects of cosmetic formulations containing UV filters, vitamins, Ginkgo biloba and red algae extracts. Journal of Photochemistry and Photobiology B: Biology, v. 153, p. 121–126, 2015.
MUNHOZ, V. M. et al. Avaliação do fator de proteção solar em fotoprotetores acrescidos com extratos da flora brasileira ricos em substâncias fenólicas. Revista de Ciencias Farmaceuticas Basica e Aplicada, v. 33, n. 2, p. 225–232, 2012.
NDIAYE, M. et al. The grape antioxidant resveratrol for skin disorders: Promise, prospects, and challenges. Archives of Biochemistry and Biophysics, v. 508, n. 2, p. 164–170, 2011
PINTAĆ, D. et al. Solvent selection for efficient extraction of bioactive compounds from grape pomace. Industrial Crops and Products, v. 111, n. November 2017, p. 379–390, 2018.
PRESTES, P. S. et al. Avaliação da estabilidade sísico-química de emulsão acrescida de uréia dispersada, ou não, em propilenoglicol. Revista de Ciências Farmacêuticas Básicas e Aplicadas, v. 30, n. 1, p. 47-53, 2009.
PURIM, K. S. M.; LEITE, N. Fotoproteção e Exercício Físico. Rev Bras Med, v. 16, n. 3, 2010.
REIS MANSUR, M. C. P. P. et al. In vitro and in vivo evaluation of efficacy and safety of photoprotective formulations containing antioxidant extracts. Brazilian Journal of Pharmacognosy, v. 26, n. 2, p. 251–258, 2016.
ROMBALDI, A. J. Prevalence and factors associated with exposure to sunlight and sunscreen among physical education teachers in Pelotas, Southern Brazil. v. 92, n. 6, p. 785–792, 2017.
SALVADOR, M. P.; JUNIOR, J. A. O.; CHIARI-ANDRÉO, B. G. Influência do material de embalagem na estabilidade de formulação cosmética contendo vitamina c. Revista Brasileira Multidisciplinar, v. 19, n. 2, 2016.
SCHALKA, S.; REIS, V. M. S. DOS. Fator de proteção solar: significado e controvérsias. Anais Brasileiros de Dermatologia, v. 86, p. 507–515, 2011.
SOUZA, F. P.; CAMPOS, G. R.; PACKER, J. F.Determinação da atividade fotoprotetora e antioxidante em emulsões contendo extrato de Malpighia glabra L. – Acerola. Revista de Ciências Farmacêuticas Básica e Aplicada, v. 34, n. 1, p. 69-77, 2013.
SOUZA, V. B.; FERREIRA, J. R. N. Desenvolvimento e estudos de estabilidade de cremes e géis contendo sementes e extratos do bagaço da uva Isabel (Vitis labrusca L.). Rev Ciênc Farm Básica Apl, v. 31, n. 3, p. 217-222, 2010.
VIOLANTE, I. M. P. et al. Avaliação in vitroda atividade fotoprotetora de extratos vegetais do cerrado de Mato Grosso. Revista Brasileira de Farmacognosia, v. 19, n. 2ª, p. 452-457, 2009.
ZANIN, S. M. W. et al. Parâmetros físicos no estudo da estabilidade das emulsões physicals parameters in the emulsion stability study. Revista Visão Acadêmica, v. 2, n. 2, p. 47-58, /2001
1 Discente do Curso Superior Bacharelado em Farmácia da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: acquila.freire@gmail.com
2 Discente do Curso Superior Licenciatura em Química do Instituto Federal de Educação, Ciência e Tecnologia do Sertão Pernambucano Campus Petrolina e-mail: nome@provedor.com.br
3 Discente da Pós-graduação em Ciências da Saúde e Biológicas da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: Ismael.holanda@discente.univasf.edu.br
4 Discente da Pós-graduação em Ciência dos Materiais da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: Larissa.bruno@discente.univasf.edu.br
5 Discente da Pós-graduação em Ciências da Saúde e Biológicas da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: nome@amanciohdr@gmail.com
6 Discente do Curso Superior Bacharelado em Farmácia da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: gabinv.farma@gmail.com
7 Discente do Curso Superior Bacharelado em Farmácia da Universidade Federal do Vale do São Francisco Campus Petrolina e-mail: luanamarques@gmail.com
8 Docente do Curso Superior Bacharelado em Farmácia da Universidade Federal do Vale do São Francisco Campus Petrolina. Doutor em Ciências (Ciências Farmacêuticas/FCFRP-USP). e-mail: nome@provedor.com.br
