EXPANDING THE COURSE OF INFLAMMATORY BOWEL DISEASES BY UPDATING THEIR THERAPEUTIC APPROACHES
REGISTRO DOI: 10.69849/revistaft/ra10202505141531
Luma de Alencar Bezerra1
Maysa Maria Portela Martins Brito Passos1
José Lopes Pereira Junior2
Vanessa Meneses de Brito Campelo3
Marina Lages Pires4
Resumo
As Doenças Inflamatórias Intestinais (DIIs) compreendem um grupo heterogêneo de enfermidades crônicas ou agudas que afetam o trato gastrointestinal, tendo como principais representantes a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU). No Brasil, as DIIs são consideradas emergentes, com escassez de dados que delimitem com precisão sua prevalência e impacto. Este estudo teve como objetivo descrever as principais atualizações nas diretrizes terapêuticas voltadas ao tratamento dessas doenças. Realizou-se uma revisão sistemática da literatura baseada em Guias de Prática Clínica (GPC), por meio de buscas nas bases BVS, PubMed, SciELO e LILACS, considerando publicações dos últimos dez anos. Foram incluídas revisões, ensaios clínicos e meta-análises que abordassem o tratamento das DIIs conforme diretrizes reconhecidas. A seleção dos estudos foi feita por dois revisores independentes, com desempate por um terceiro, e a avaliação metodológica utilizou as ferramentas Cochrane e AMSTAR. Os dados extraídos foram analisados qualitativamente. Os resultados destacaram o papel crescente das terapias biológicas, como imunomoduladores e anticorpos monoclonais, na remissão de casos moderados a graves. A medicina personalizada, baseada em perfis genéticos e moleculares, representa um avanço promissor, embora ainda limitada por altos custos e estrutura inadequada. Estratégias complementares, como nutrição enteral exclusiva, probióticos e transplante de microbiota fecal, mostraram benefícios em subgrupos específicos. Persistem desafios como acessibilidade às terapias inovadoras, padronização de diretrizes e adesão ao tratamento, que demanda suporte emocional e acompanhamento contínuo. Conclui-se que a individualização do cuidado e a atuação interdisciplinar são fundamentais, sendo imprescindíveis políticas públicas e investimentos em pesquisa para ampliar o acesso equitativo às melhores terapias, promovendo melhores desfechos clínicos e qualidade de vida.
Palavras-chave: Doença de Crohn. Colite Ulcerativa. Guia de Prática Clínica.
1 INTRODUÇÃO
As doenças que decorrem de desordens inflamatórias de caráter crônico ou agudo e afetam o trato gastrointestinal formam um grupo patológico heterogêneo denominado Doenças Inflamatórias Intestinais (DII), tendo como principais representantes são a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU). Geralmente, esse processo inflamatório pode acontecer mediante infecção viral, bacteriana ou por protozoários, bem como por isquemia, radiação e de forma idiopática (Khorshidi, et. al, 2020; Marques et al., 2023).
Em relação aos aspectos clínicos, a DC e a RCU têm em comum sintomas, tais quais hematoquezia, diarreia e dor abdominal. Já a localização, a profundidade da inflamação e a prevalência das complicações diferem notoriamente. A DC tem uma inflamação tipicamente descontínua e transmural, de forma que todas as camadas do intestino podem ser envolvidas, da mesma forma que qualquer parte do TGI pode ser afetado, da boca ao ânus. Em contrapartida, na RCU o processo inflamatório tem caráter contínuo e se limita apenas às camadas mucosa e submucosa superficial, bem como afeta tipicamente apenas o reto e o cólon. Em relação às complicações, os estudos comprovam que a afecção por DII leva a um risco maior de desenvolvimento de câncer colorretal (CCR), em que, após 30 anos de doença, a probabilidade de um paciente com RCU desenvolvê-lo se acumula em 18%, enquanto o paciente com DC possui uma probabilidade acumulada de 8% (Pochard et. al., 2018; De Oliveira et al., 2021).
Os principais diagnósticos diferenciais das DII são outras inflamações que também apresentam inflamação intestinal, são elas: infecções, diverticulite, apendicite, enterite por radiação, fármacos e vasculite intestinal. Hodiernamente, não há conhecimento específico acerca da exata etiologia e dos eventos fisiopatológicos que incorrem em DII. A genética se configura como o principal fator de risco para ambas as doenças, além da microbiota do hospedeiro, que se configuram, portanto, os pontos de maior implicação no estabelecimento e na manutenção da inflamação intestinal (Khorshidi, et. al, 2020; Silva Fars et al., 2020).
Epidemiologicamente, as DII se caracterizam como mais comuns em brancos, especialmente, Judeus, tendo picos de incidência entre 15 e 40 anos e 50 e 80 anos de idade. É sabido que o predomínio da RCU é em homens, enquanto a DC possui uma taxa superior em mulheres. A morbidade, no entanto, é baixa, mas as DII têm aumentado sua incidência nos últimos anos, sendo mais alta em países ocidentalizados, principalmente, na Europa, América do Norte, Reino Unido e Austrália – por volta de 0,5% das pessoas adultas em países ocidentais sofrem de DII (Ferreira et. al., 2021; Marques et al., 2023).
Fica evidente, portanto, a relevância social do tema escolhido, sobretudo pelo direcionamento à atualização das medidas terapêuticas, uma vez que atualmente, as DII não têm cura e seu tratamento é basicamente direcionado ao controle dos sintomas. Em termos gerais os pacientes precisam fazer mudanças no estilo de vida e na alimentação, bem como são submetidos a medicações em fases de maior intensidade que são muito desconfortáveis. Dessa forma, é necessário considerar as DIIs como um problema de saúde pública no Brasil e no mundo, devido à sua cronicidade, alta morbidade e custos terapêuticos elevados, que afetam tanto os sistemas de saúde quanto a produtividade econômica dos países (STEINWURZ et al., 2023).
Diante do exposto, ainda que com uma etiopatogenia obscura, é nítido que as Doenças Inflamatórias Intestinais apresentam uma morbidade e uma importância epidemiológica latente e que crescer cada vez mais nos últimos anos. Nesse sentido, configura-se como um grupo de doenças complexo e cheio de nuances que devem ser cada vez mais investigados e discutidos no contexto acadêmico, a fim de fornecer embasamento teórico para a prática plena da Medicina baseada em evidências.
Nesse sentido, o objetivo principal desta pesquisa é apontar e descrever as principais atualizações em relação às diretrizes terapêuticas das Doenças Inflamatórias Intestinais (DII). Com isso, espera-se, de forma mais específica, compilar, em um único trabalho, os principais aspectos relacionados ao tratamento das DII; observar e descrever as alterações mais relevantes nos protocolos terapêuticos das DII nos últimos 5 anos; e apontar eventuais divergências em relação às diretrizes terapêuticas das DII atualmente, discutindo seus aspectos mais importantes.
2 FUNDAMENTAÇÃO TEÓRICA OU REVISÃO DA LITERATURA
2.1 MORFOFISIOLOGIA INTESTINAL
A anatomia do trato gastrointestinal (TGI), na ordem cranial para caudal, é composta da seguinte forma: boca, faringe, esôfago, estômago, intestino delgado, intestino grosso, reto e ânus. Todos esses órgãos são interligados a glândulas, como as salivares, e a outros acessórios, como pâncreas, fígado e vesícula biliar. Essas estruturas são fundamentais para o bom funcionamento do processo digestório. Diante disso, faz-se necessário conhecer a fisiologia do TGI, a fim de reconhecer as anormalidades que ocorrem nesse trajeto e ajudar a identificar as diferentes doenças de acordo com esse trajeto. Tendo como exemplo, a Doença de Crohn que pode afetar qualquer parte do TGI e a RCU que afeta apenas o reto e o ânus (Tortora, 2023).
Nesse contexto, a função primária do sistema digestório é encaminhar água, macronutrientes e micronutrientes, eletrólitos para o ambiente interno do corpo. Para isso, existe alguns processos como digestão, absorção, secreção, motilidade que são interligados e regulados pelo sistema nervoso autônomo (SNA), sistema nervoso entérico (SNE), endócrinos e parácrinos (Guyton, 2017).
Nesse ínterim, podemos destacar a histologia do TGI, a qual segue um padrão e pode ser dividida em mucosa, submucosa, muscular e serosa/adventícia. A muscosa possui glândulas que produzem secreções indispensáveis para o processo de digestão. Já na camada submucosa, poder encontrado tecido linfoide que tem função de defesa e também possui glândulas. Quanto à camada muscular lisa, a sua disposição é importante para os movimentos realizados pelas diferentes porções do canal alimentar. Entre essas camadas está localizado o plexo mioentérico (Auerbach), composto por neurônios motores que realizam o controle da motilidade. Além disso, possui o plexo submucoso (Meissner), o qual é composto por neurônios motores que inervam as glândulas mucosas e por neurônios sensoriais que promovem informações para o plexo entérico e regiões superiores, com isso, consegue controlar o processo de secreção (Junqueira, 2013).
Portanto, o trato gastrointestinal é responsável por todo o processamento e absorção dos nutrientes provenientes dos alimentos ingeridos, permitindo o bom funcionamento do organismo e processa os alimentos para obter energia e livrar o corpo de resíduos sólidos (Guyton, 2017).
2.2 VISÃO GERAL SOBRE AS DOENÇAS INFLAMATÓRIAS INTESTINAIS
2.2.1 EPIDEMIOLOGIA
No panorama mundial, é lícito postular que as maiores taxas de prevalência e incidência das DIIs se apresentam nos países de maior desenvolvimento econômico em regiões que se estendem desde o norte da Europa até a América – o Canadá, os Estados Unidos –, bem como a Oceania – Austrália e Nova Zelândia (Lophaven; Lynge; Burisch, 2017). Em áreas desenvolvidas, a incidência tem se mantido estável, ao passo que em regiões recém-industrializadas – Ásia, África e Europa oriental – os estudos epidemiológicos mais recentes indicam um aumento significativo, por conta de aspectos tangentes à maior taxa de urbanização que se deu numa mudança comportamental de estilo de vida, níveis mais altos de tabagismo, ocupações de caráter sedentárias e taxas menores de amamentação (Kaplan et. al., 2019.
Em terras sul-americanas, já é possível afirmar que a DC e a RCU são problemas que vêm se expandindo. Uma revisão sistemática envolvendo seis estudos, feita por Selvaratan et. al. (2019), mapearam a incidência das DIIs na América do Sul. Entre os achados, de forma unânime foi demonstrado que a RCU em comparação com a DC possui uma frequência relativamente maior, sendo a DC de cólon e a RCU pancolônca de maior predominância., seja associado por diferenças em polimorfismos genéticos ou exposições ambientais.
No Brasil, as DIIs são consideradas doenças emergentes, com poucos dados e informações que possam delimitar factualmente o cenário que se coloca. Isso se deve, sobretudo, pelo fato delas não serem doenças de notificação obrigatória, faltando registros de pacientes do serviço privado, além dos dados de prevalência e incidência serem escassos (Quaresma; Kaplan; Kotze, 2019). Parente et. al. (2015) conduziu um estudo retrospectivo de 21 anos (1988 a 2012) no Piauí, que incluiu 252 pacientes – 152 DC e 100 RCU – que são encaminhados para o centro de referência de DIIs, provenientes da rede pública de todo o estado. Suas conclusões indicaram um aumento na incidência e na prevalência de DIIs: passando de 1,0 para 8,0 por 100000 habitantes e de 1,2 para 21 por 100000 habitantes, respectivamente, no período analisado. Entre as regiões de maior afecção, a DC de cólon não estenosante e não fistulizante foi mais predominante, enquanto na RCU, a colite distal foi a localização mais repetida.
2.2.2 ETIOPATOGÊNESE
Hodiernamente, a etiogênese precisa das DIIs não é conhecida. Entretanto, existem fatores determinantes que já estão claros para a comunidade científica, como por exemplo a susceptibilidade genética, uma vez que o histórico de DII em parentes de primeiro grau aumenta o risco de desenvolver a doença de 8 a 10 vezes mais que os controles, bem como em casos de gêmeos, o riso passa a ser de 26 vezes para DC e 9 vezes para RCU, evidenciando, claramente a influência genética (Kim & Cheon, 2017). Além do mais, verificou-se também que imigrantes quando se mudam para países com alta prevalência de DII, indicando a influência nítida de fatores ambientais, como a microbiota, bem como a dieta ocidental, acreditando, portanto, que ela provoque direta ou indiretamente a DII (Rodrigues-Palacios et. al., 2018). Em 2021, Ferreira; De Deus & Junior (2021), reuniram numa revisão sistemática de literatura, os principais aspectos fisiológicos e etiológicos das DII.
Entre eles destaca-se a atividade da mieloperixosidade, uma enzima gerada por células do sistema imunológico que é crucial na defesa contra patógenos, contudo, sua atividade também pode danificar proteínas e a matriz extracelular, intensificando a inflamação em doenças inflamatórias intestinais (DII).
Outro achado fundamental é a Disbiose de microbiota, em que pacientes com DII possuem uma alteração nas espécies predominantes na microbiota, onde bactérias presentes em indivíduos saudáveis, que exercem atividade anti-inflamatória, são substituídas por bactérias com potencial patogênico, deflagrando um processo inflamatório crônico na mucosa intestinal.
Soma-se ao supracitado a autofagia, ou seja, a digestão e indução da morte de organelas no citoplasma, sendo um dos primeiros eventos a ocorrer no processo fisiopatológico das DII. Além disso, observa-se a presença das Células Gliais Entéricas (CGE), que possuem função na motilidade gastrointestinal e imunológica, acreditando-se que elas podem colaborar na fisopatologia da DII ao perder suas propriedades anti-inflamatórias.
A obesidade e a massa corporal também foram visualizadas, em que pacientes com DII possuem um declínio progressivo da massa magra paralelo à progressão da doença, devido ao estado inflamatório sistêmico. O tecido adiposo branco mesentérico possui mudanças patológicas importantes, tais quais a grande infiltração de células imunológicas e um tamanho anormalmente grande. Esse tecido – também chamado de gordura rastejante – que tipicamente se encontra em áreas de lesão intestinal é a gênese de vários mediadores inflamatórios que agem na mucosa intestinal próxima, decorrendo todo o processo inflamatório citado anteriormente.
Da mesma forma, a sarcopenia – diminuição da massa e da função muscular – é uma marca importante da DII. Não se sabe ainda, todavia, a precisa ordem cronológica de ocorrência desses eventos, ou mesmo se há a necessidade de que todos ocorram para que a doença se estabeleça no indivíduo.
2.2.3 QUADRO CLÍNICO
Entre os principais sintomas apresentados em ambas as doenças, a hematoquezia, a diarreia, a dor abdominal e a distensão abdominal são aos mais comuns. Em relação às manifestações extraintestinais, as queixas reumatológicas – artrites/artralgia e espondilite anquilosante – são as de maior frequência, sendo seguidas por queixas dermatológicas e oftalmológicas. Como complicações, têm-se como as mais comuns são fissuras perineais e a formação de subestenose ileal (Rogler et. al., 2019).
2.2.4 DIAGNÓSTICO
Para a RCU, o diagnóstico deve ser feito considerando uma anmnese minuciosa dos sintomas, exame físico e histórico familiar. Para complementação, são utilizadas ferramentas laboratoriais, tais quais hemograma, VHS, PCR, albumina, ferro sérico, ferritina, coproscopia e coprocultura, sendo eles indispensáveis para a exclusão de diagnósticos diferenciais de causas virais, bacterianas ou parasitárias, bem como comorbidades que podem estar presentes, a exemplo da anemia.
O exame íleo-conoscópico e a biópsia são os exames padrão-ouro para chegar ao diagnóstico e definir o grau de severidade e de extensão da enfermidade. Nota-se inflamação superficial do reto de forma contínua e confluente se estendendo proximalmente. Histologicamente, os achados são a perda da estrutura das criptas e a presença de células inflamatórias na lâmina própria (Bernstein et. al., 2015).
Na DC, há uma semelhança baseada na análise da anamnese bem coletada e na caracterização da doença através do exame endoscópico, a depender do grau de severidade terá achados específicos: na sua forma leve, serão encontradas ulcerações de pequeno tamanho e pouca inflamação, dificultando o diagnóstico. Nos estágios moderado e severo, encontra-se lesões segmentais, úlceras longitudinais e aftosas com aspecto de pavimento, associado a uma histologia compatível, obtido, no caso, pela borda das úlceras com presença de granuloma não caseoso (patognomônico da enfermidade). Como dito anteriormente, a patologia tem a possibilidade de acometer qualquer parte da extensão do TGI (da boca ao ânus) (Torres; Mehandru & Peyrin-Biroulet, 2017).
A classificação de Montreal é uma ferramenta fundamental para entender e categorizar as DIIs, abordando três principais aspectos das doenças: 1) Localização – descrevendo onde a inflamação está presente no TGI – , 2) Comportamento – descrevendo como a doença se manifesta ao longo do tempo, na DC, por exemplo, se a inflamação é estenosante, não estenosante ou penetrante – , e 2) Gravidade – avaliando a gravidade da doença e seu impacto na saúde geral do paciente, variando de leve a moderada a grave, dependendo dos sintomas clínicos, achados endoscópicos, exames de imagem e necessidade de intervenções médicas ou cirúrgicas. Todos esses parâmetros são essenciais para determinar a abordagem terapêutica mais apropriada e para monitorar a resposta ao tratamento ao longo do tempo (Durante et. al., 2022).
2.3 PRINCIPAIS ASPECTOS TERAPÊUTICOS
Segundo De Souza (2021), as principais doenças inflamatórias intestinais são a Doença de Crohn e a Retocolite Ulcerativa. Ambas são enfermidades crescentes em todo o mundo e possuem característica de exacerbação e remissão. Dito isso, por serem doenças crônicas, o seu tratamento é prolongado e, muitas vezes, por tempo indeterminado; por isso, precisa de uma boa adesão do paciente, para obter eficácia no tratamento. Já que o baixo grau de adesão está associado ao aumento da atividade da doença, às recaídas, à maior morbimortalidade, ao aumento do gasto em saúde, à má qualidade de vida e à maior incapacitação.
A abordagem farmacológica para o tratamento dessas doenças é bem complexa, devido ao desconhecimento da natureza dos agentes que provocam o processo inflamatório e pelas particularidades de cada paciente, além do intuito de prevenir recidiva, induzir a remissão e aliviar os sintomas (Cambui, 2015).
Diante disso, o tratamento convencional consiste no uso de ácido5-aminossalicílico (sulfassalazina), corticosteroides, antibióticos e imunossupressores capazes de resolver episódios agudos, mas não evitam recidivas (Cambui, 2015).
A sulfassalazina é uma combinação de sulfonamida (sulfapiridina) com um salicilato, cujos efeitos colaterais comuns consistem em distúrbios gastrintestinais como mal-estar e cefaleia, reações cutâneas e leucopenia, má absorção de ácido fólico, reversíveis com a interrupção do fármaco (Cambui, 2015).
A ciclosporina é o mais potente imunossupressor empregado no tratamento das doenças inflamatórias intestinais, com ação imediata após o início do uso. A utilização desse fármaco provoca disfunção renal, neurotoxicidade e infecções oportunistas. Ademais, o imunossupressor metotrexato apresenta baixa eficácia em casos de RCU (Cambui, 2015). Além disso, destaca-se o tratamento mediado por agentes biológicos. Como exemplo clássico, cita-se o infliximabe, um anticorpo monoclonal (imunoglobulina G) que age como antagonista do Fator de necrose tumor alfa (TNF-α), produto das células imunológicas do hospedeiro (Cambui, 2015).
Corticosteróides têm sido empregados quando o 5-ASA (molécula de atividade terapêutica da mesalazina) se mostra ineficiente. A prednisona ou prednisolona são as formas mais utilizadas. Contudo, há necessidade do controle desse tipo de fármaco devido à forte exposição do doente ao risco de desenvolver hipertensão arterial, diabetes, osteoporose e outras patologias associadas (Cambui, 2015). A via endovenosa é restrita à inflamação intestinal intensa, a ponto de inviabilizar. A via oral e diante sintomatologia de inflamação sistêmica exuberante. As drogas usuais são a hidrocortisona e a metilprednisolona (Do Carmo Carvalho, 2022).
Os imunomoduladores principais são as tiopurinas: azatioprina e mercaptopurina. São úteis em quadros moderados a graves associados a um agente anti-TNF ou em acometidos inaptos em reduzir a dose de glicocorticoide sem exacerbação. Tais drogas são potentes imunossupressores, inibindo a ação linfocitária e as células natural killer (Do Carmo Carvalho, 2022).
Portanto, as DII, sendo autoimunes, não têm cura. Mas existem tratamentos para que a doença seja controlada e a pessoa não tenha perda da sua qualidade de vida. Existe a associação da manifestação clínica com a genética e fatores externos, os quais influenciam no desencadeamento das principais DII, as quais cursam com sintomatologias semelhantes, mas que são condições impostas e precisam ser diagnosticadas e tratadas de modo precoce (Do Carmo Carvalho, 2022).
3 METODOLOGIA
Este estudo foi conduzido como uma revisão sistemática da literatura. A metodologia será estruturada para garantir a identificação, seleção e análise crítica de estudos relevantes que abordem as terapias para DC e CU conforme os Guias de Prática Clínica. Foram incluídos os estudos que abordam o tratamento das DII e que utilizam diretrizes reconhecidas, publicadas nos últimos 10 anos, sejam em inglês, português ou espanhol. Foram excluídos os artigos que não estavam disponíveis na íntegra, ou que se tratou de estudos de casos isolados, bem como as publicações que não eram revisões de literatura, ensaios clínicos ou metaanálises.
Para tanto, as bases de dados eletrônicas consultadas foram a BVS (BVS Biblioteca Virtual em Saúde), PubMed, SciELO (Scientifc Electronic Library Online) e LILACS (Literatura Latino-Americana e do Caribe em Ciências da Saúde). Foram utilizados, assim, os seguintes descritores nos idiomas supracitados: “Doença de Cronh” (Crohn’s Disease), “Colite Ulcerativa” (Ulcerative Colitis) e “Guia de Prática Clínica” (Clinical Practice Guideline), combinados entre si com uso dos operadores booleanos “OR” e “AND”.
Dessa forma, dois revisores independentes realizaram a triagem inicial dos títulos e resumos. Em seguida, os artigos selecionados foram avaliados na íntegra para confirmação dos critérios de inclusão. Qualquer discordância foi resolvida por um terceiro revisor. Logo após, utilizou-se uma tabela padronizada para extrair os seguintes dados dos estudos incluídos: Dados dos autores (nome, ano de publicação, país); Tipo de estudo (revisão de literatura, ensaio clínico, meta-análise); Intervenções terapêuticas descritas; Recomendações dos Guias de Prática Clínica; Resultados e conclusões principais.
A qualidade dos estudos foi avaliada utilizando a ferramenta Cochrane para risco de viés para ensaios clínicos e a ferramenta AMSTAR (A Measurement Tool to Assess Systematic Reviews) para revisões sistemáticas e meta-análises. Os dados serão sintetizados de forma qualitativa, com uma descrição detalhada das abordagens terapêuticas e recomendações dos Guias de Prática Clínica para DC e CU. Por se tratar de uma revisão sistemática da literatura, este estudo não envolveu diretamente seres humanos ou animais, dispensando a necessidade de aprovação por um comitê de ética em pesquisa. As referências utilizadas são citadas conforme as normas da ABNT ou do periódico ao qual o artigo está submetido.
4 RESULTADOS E DISCUSSÕES OU ANÁLISE DOS DADOS
Os resultados deste estudo ressaltam a importância da atualização das abordagens terapêuticas para as doenças inflamatórias intestinais (DIIs), de acordo com as evidências científicas mais recentes. Foi observado que os avanços terapêuticos, especialmente no campo da biotecnologia e da medicina personalizada, têm transformado significativamente o manejo clínico dessas condições.
A seguir, apresenta-se uma tabela com as principais informações dos estudos incluídos nesta revisão. Nela estão descritos os autores, o ano de publicação, o país de origem e o tipo de estudo de cada referência selecionada. Esses estudos abrangem uma variedade de abordagens, incluindo ensaios clínicos, revisões de literatura, consensos e investigações específicas sobre o manejo de doenças inflamatórias intestinais, com foco em tratamentos inovadores e avanços terapêuticos. A tabela fornece uma visão geral dos dados essenciais para a compreensão do contexto e da diversidade das abordagens utilizadas nas pesquisas analisadas.
TABELA 01 – Estudos incluídos nessa revisão de literatura
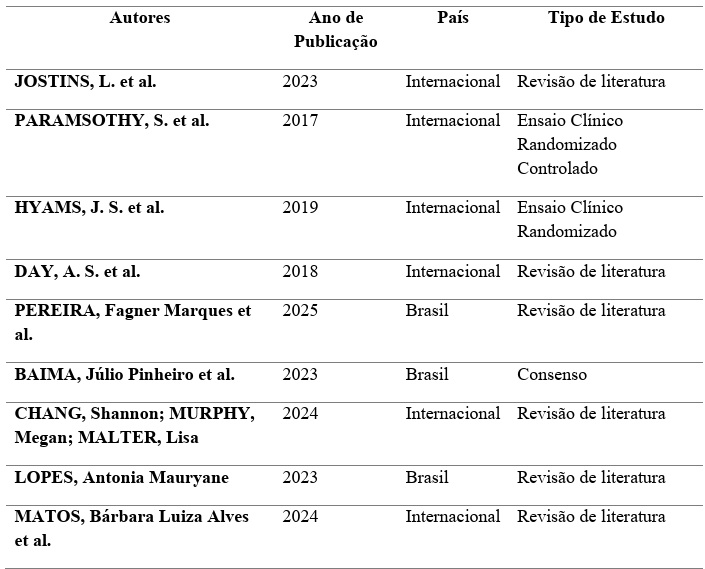
Fonte: Elaboração própria (2024). Essas informações são baseadas nos dados fornecidos para cada referência. As categorias de “Tipo de Estudo” foram inferidas a partir da descrição de cada artigo, como revisões, ensaios clínicos, consensos ou artigos de revisão médica.
Nos últimos cinco anos, houve significativas alterações nos protocolos terapêuticos das Doenças Inflamatórias Intestinais (DII), refletindo avanços substanciais tanto no entendimento da fisiopatologia quanto na introdução de novas abordagens terapêuticas. Essas mudanças possuem o intuito de otimizar o manejo clínico, melhorar a qualidade de vida dos pacientes e reduzir a incidência de complicações a longo prazo. A evolução dos tratamentos envolve principalmente inovações em medicamentos imunomoduladores e biológicos, além de novas estratégias para o manejo de casos refratários e a personalização da terapêutica (Lopes, 2023).
Entre os principais achados, destacam-se: a evolução das terapias biológicas, a relevância da medicina personalizada, o impacto do microbioma intestinal e a importância do manejo multidisciplinar.
O emprego de terapias biológicas, como imunoglobulinas monoclonais que bloqueiam o fator de necrose tumoral (TNF), demonstrou grande eficácia no controle da resposta inflamatória e na indução da remissão em pacientes com DIIs. Além disso, terapias inovadoras, como os inibidores de interleucinas específicas e moduladores de integrinas, surgem como opções promissoras para pacientes que não respondem aos tratamentos tradicionais (Chang, Murphy e Malter, 2024).
A adaptação da terapêutica com base em perfis genéticos tem sido considerada uma abordagem inovadora e com impacto para personalizar as intervenções terapêuticas. Investigações recentes identificaram marcadores genéticos, como variações nos genes NOD2, IL23R e ATG16L1, que estão associados ao risco de desenvolvimento de DIIs e à resposta a tratamentos específicos (Baima et al., 2023; Jostins et al., 2023). Esses progressos possibilitam ajustar as terapias conforme as características genéticas de cada paciente, potencializando a efetividade dos tratamentos e minimizando os efeitos adversos. Entretanto, a implementação dessa estratégia na prática clínica ainda enfrenta desafios, como o custo elevado dos exames genéticos e a necessidade de uma infraestrutura adequada para a análise e interpretação dos dados (Pereira et al., 2025).
A avaliação genética e molecular dos pacientes tem permitido a personalização do tratamento, possibilitando a escolha de intervenções mais adequadas ao perfil individual. Esse avanço diminui a incidência de efeitos adversos e melhora a eficácia terapêutica, representando um marco de suma importância no cuidado de pacientes com DIIs (Pereira et al., 2025).
Outra condição fundamental é a modulação da flora intestinal. Pesquisadores sugerem que o desequilíbrio da microbiota, denominado disbiose, exerce um papel essencial no desencadeamento das doenças inflamatórias intestinais (DIIs). Abordagens como o uso de probióticos, prebióticos e o Transplante de Microbiota Fecal (TMF) têm sido investigadas para restaurar o equilíbrio microbiano e reduzir a inflamação no intestino (Baima et al., 2023; Pereira et al., 2025). Particularmente, o TMF tem se mostrado eficaz em casos resistentes, induzindo remissão tanto clínica quanto endoscópica (Paramsothy et al., 2017). Entretanto, ainda é necessário realizar estudos mais detalhados para estabelecer protocolos consistentes e identificar as cepas bacterianas mais eficientes e garantir a segurança do procedimento.
As terapias biológicas continuam sendo a base principal no tratamento das (DIIs), especialmente nos casos moderados a graves que não respondem à terapêutica tradicional. Medicamentos como infliximabe, adalimumabe e vedolizumabe são amplamente empregados, com pesquisas indicando progressos na otimização das dosagens e na diminuição da imunogenicidade (Hyams et al., 2019). A introdução de anticorpos monoclonais mais direcionados tem auxiliado na indução e manutenção da remissão, além de diminuir a necessidade de corticosteroides, que possuem efeitos adversos consideráveis (Baima et al., 2023). A combinação de imunomoduladores com terapias biológicas tem se mostrado eficaz na prevenção da formação de anticorpos contra os biológicos, o que aumenta sua durabilidade e eficácia. Contudo, essa combinação demanda monitoramento constante devido ao risco aumentado de infecções e complicações hematológicas (Pereira et al., 2025).
As condutas nutricionais têm se destacado como alternativas eficazes e seguras no tratamento das (DIIs) principalmente em crianças. A Nutrição Enteral Exclusiva (NEE) é indicada como tratamento de primeira linha para indução da remissão na Doença de Crohn, mostrando-se comparável ou até mais eficaz que o uso de corticosteroides, sem os efeitos colaterais associados a esses medicamentos (Day et al., 2018). A NEE favorece não apenas a regeneração da mucosa intestinal, mas também auxilia no crescimento e no desenvolvimento saudável das crianças. No entanto, seguir dietas restritivas pode ser desafiador, especialmente entre os adolescentes. Por isso, é fundamental a elaboração de protocolos uniformizados e métodos de apoio para melhorar a aceitação e adesão ao tratamento nutricional (Pereira et al., 2025). Além da NEE, planos alimentares específicos, como a Dieta de Exclusão para Doença de Crohn (CDED), também têm mostrado resultados positivos.
No campo da discussão, é evidente que os avanços terapêuticos têm contribuído para a melhoria dos desfechos clínicos, mas desafios importantes permanecem. A acessibilidade às terapias inovadoras, principalmente em sistemas de saúde pública, ainda é uma barreira significativa. O custo elevado de medicamentos biológicos e terapias personalizadas limita sua ampla utilização, reforçando a necessidade de políticas públicas que promovam sua inclusão nos protocolos de saúde.
Apesar do avanço nas opções terapêuticas, existem algumas divergências nas diretrizes adotadas por diferentes sociedades médicas, o que reflete a complexidade das DII e a necessidade de uma abordagem personalizada. As diretrizes de sociedades como a American Gastroenterological Association (AGA), European Crohn’s and Colitis Organisation (ECCO) e a Brazilian Society of Gastroenterology (SBG) apresentam recomendações que, embora em grande parte convergentes, variam em pontos cruciais, como o momento ideal para o início de tratamentos biológicos e a escolha de terapias de manutenção (Matos et al., 2024).
Ademais, a adesão ao tratamento por parte dos pacientes depende de estratégias de educação continuada e suporte emocional. A participação ativa do paciente no manejo da sua condição, aliada a programas de acompanhamento, pode otimizar a eficácia do tratamento e minimizar complicações.
Outro ponto relevante é a necessidade de pesquisas sobre a heterogeneidade das DIIs. Embora os avanços terapêuticos sejam promissores, as respostas variáveis entre os pacientes reforçam a importância de compreender as nuances dessas condições. Estudos voltados à identificação de biomarcadores de prognóstico e resposta terapêutica são cruciais para o desenvolvimento de tratamentos ainda mais eficazes.
Por fim, os dados apresentados corroboram a importância da atualização constante nas abordagens terapêuticas e a integração de novos conhecimentos e tecnologias para aprimorar o cuidado com pacientes portadores de DIIs. Além disso, reforça-se a relevância de um modelo assistencial que priorize a interdisciplinaridade e a individualização do tratamento, garantindo um impacto positivo nos desfechos clínicos e na qualidade de vida dos pacientes. A tabela 2 a seguir sintetiza os principais tratamentos, medicamentos e seus mecanismos de ação, destacando desde as terapias biológicas e personalizadas até as estratégias nutricionais e a modulação da microbiota intestinal. Esses avanços, como o uso de anticorpos monoclonais direcionados e a personalização baseada em marcadores genéticos, não apenas otimizam os desfechos clínicos, mas também promovem uma abordagem integrada e interdisciplinar que melhora a qualidade de vida dos pacientes.
TABELA 02 – Principais tratamentos para Doenças Inflamatórias Intestinais (DIIs), medicamentos associados e os mecanismos de ação
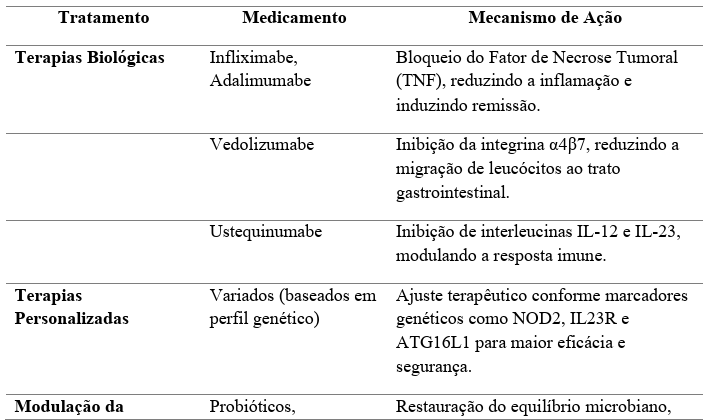
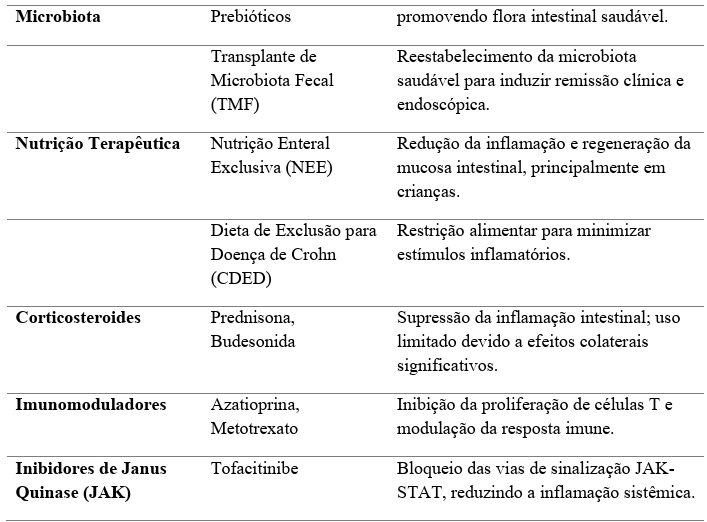
Fonte: Elaboração própria (2024). As informações apresentadas na tabela foram desenvolvidas com base nos dados fornecidos em diferentes referências mencionadas no texto.
5 CONCLUSÃO/CONSIDERAÇÕES FINAIS
Os resultados desta revisão evidenciam o impacto significativo dos avanços terapêuticos no manejo das Doenças Inflamatórias Intestinais (DIIs). O progresso em áreas como biotecnologia, medicina personalizada e modulação da microbiota intestinal tem contribuído para a melhoria dos desfechos clínicos e da qualidade de vida dos pacientes. As terapias biológicas, como os imunomoduladores e anticorpos monoclonais, continuam a ser a base do tratamento, demonstrando alta eficácia na indução e manutenção da remissão, especialmente em casos moderados a graves.
A personalização das intervenções terapêuticas, com base em perfis genéticos e moleculares, emerge como um marco no cuidado das DIIs. Apesar dos desafios, como o custo elevado e a necessidade de infraestrutura adequada, essa abordagem tem o potencial de otimizar os tratamentos e minimizar os efeitos adversos, representando um avanço significativo na prática clínica. Além disso, estratégias como a Nutrição Enteral Exclusiva (NEE) e o uso de probióticos e transplante de microbiota fecal (TMF) destacam-se como alternativas promissoras, especialmente em subgrupos específicos de pacientes.
No entanto, permanecem desafios importantes, como a acessibilidade às terapias inovadoras e a necessidade de uniformização das diretrizes clínicas. A adesão ao tratamento também depende de estratégias que combinem educação, suporte emocional e programas de acompanhamento. Nesse contexto, a interdisciplinaridade e a individualização do cuidado mostram-se essenciais para superar as barreiras existentes e aprimorar a abordagem terapêutica.
Por fim, o cenário atual reforça a necessidade de investimentos contínuos em pesquisa e desenvolvimento, além de políticas públicas que viabilizem o acesso às terapias mais avançadas. Com a integração de novos conhecimentos e tecnologias, é possível consolidar um modelo assistencial mais eficaz e humanizado, promovendo um impacto positivo nos desfechos clínicos e na qualidade de vida dos pacientes com DIIs.
REFERÊNCIAS
BAIMA, Júlio Pinheiro et al. Second Brazilian consensus on the management of ulcerative colitis in adults: a consensus of the Brazilian Organization for Crohn’s Disease and Colitis (GEDIIB). Arquivos de gastroenterologia, v. 59, p. 51-84, 2023.
CHANG, Shannon; MURPHY, Megan; MALTER, Lisa. A review of available medical therapies to treat moderate-to-severe inflammatory bowel disease. Official journal of the American College of Gastroenterology| ACG, v. 119, n. 1, p. 55-80, 2024.
DAY, A. S. et al. Exclusive enteral nutrition: An optimal therapy for Crohn’s disease in children. Nature Reviews Gastroenterology & Hepatology, v. 15, n. 9, p. 527-535, 2018. Disponível em: https://www.nature.com/articles/s41575-018-0036-6.
DE OLIVEIRA, Wynni Gabrielly Pereira et al. Doença inflamatória intestina9l: aspectos clínicos e diagnósticos. Facit Business and Technology Journal, v. 1, n. 27, 2021.
FERREIRA GS, et al. Fisiopatologia e etiologias das doenças inflamatórias intestinais: uma revisão sistemática de literatura. Brazilian Journal of Health Review, 2021; 4(4).
HYAMS, J. S. et al. Infliximab for induction and maintenance therapy for ulcerative colitis. New England Journal of Medicine, v. 381, n. 12, p. 1120-1129, 2019. Disponível em: https://www.nejm.org/doi/full/10.1056/NEJMoa1905724.
JOSTINS, L. et al. Host-microbe interactions have shaped the genetic architecture of inflammatory bowel disease. Nature, v. 491, n. 7422, p. 119-124, 2023. Disponível em: https://www.nature.com/art icles/nature11582.
KHORSHIDI, M. et al. A posteriori dietary patterns and risk of inflammatory bowel disease: a meta-analysis of observational studies. International Journal for Vitamin and Nutrition Research. Boston, v. 90, n. 3-4, p. 376-384, jun. 2020.
LOPES, Antonia Mauryane. FATORES SOCIODEMOGRÁFICOS E CLÍNICOS RELACIONADOS À QUALIDADE DE VIDA DE PACIENTES COM DOENÇA INFLAMATÓRIA INTESTINAL. 2023.
MARQUES, Iana Vitória Araújo et al. Análise epidemiológica da Doença Inflamatória Intestinal no Brasil nos últimos 10 anos. Revista Científica do Hospital e Maternidade José Martiniano Alencar, v. 4, n. 1, p. 13-17, 2023.
MATOS, Bárbara Luiza Alves et al. ESTRATÉGIAS INOVADORAS DE TRATAMENTO CLÍNICO PARA DOENÇA INFLAMATÓRIA INTESTINAL PEDIÁTRICA. Revista Ibero-Americana de Humanidades, Ciências e Educação, v. 10, n. 9, p. 245-258, 2024.
PARAMSOTHY, S. et al. Multidonor intensive faecal microbiota transplantation for active ulcerative colitis: a randomised placebo-controlled trial. The Lancet, v. 389, n. 10075, p. 1218-1228, 2017. Disponível em: https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(17)30182- 4/fulltext.
PEREIRA, Fagner Marques et al. AVANÇOS NO MANEJO DAS DOENÇAS INFLAMATÓRIAS INTESTINAIS (DII) EM CRIANÇAS: TERAPIAS BIOLÓGICAS, INTERVENÇÕES NA MICROBIOTA E PERSONALIZAÇÃO DO TRATAMENTO. LUMEN ET VIRTUS, v. 16, n. 44, p. 384-395, 2025.
POCHARD., C. et al. The multiple faces of inflammatory enteric glial cells: is Crohn’s disease a gliopathy? American Journal of Physiology Gastrointestinal and Liver Physiology. United States, v. 315, n. 1, p. G1-G11, jul. 2018.
SILVA FARS, et al. A análise transcricional completa identifica marcadores de B, T e vias de sinalização de células plasmáticas no tecido adiposo mesentérico associado à doença de Chron. Journal of Translational Medicine, 2020; 44(18).
STEINWURZ, Flavio et al. Latin America consensus statement on inflammatory bowel disease: importance of timely access to diagnosis and treatment. Therapeutic Advances in Gastroenterology, [S.l.], v. 16, p. 1–17, 2023. DOI: 10.1177/17562848231207312. Disponível em: https://journals.sagepub.com/doi/10.1177/17562848231207312. Acesso em: 12 maio 2025.
1 Discente do Curso Superior de Medicina do Instituto de Educação Superior do Vale do Parnaíba Campus sede – sabiazal. e-mail: lumabezerraalencar@gmail.com / maysamppassos@gmail.com
2 Docente do Curso Superior de Medicina do Instituto de Educação Superior do Vale do Parnaíba Campus sede – sabiazal. Doutor em Ciências Farmacêuticas (PPGCF/UFPI). e-mail: josejrfarmaceutico@gmail.com
3 Docente do Curso Superior de Medicina do Instituto de Educação Superior do Vale do Parnaíba Campus sede – sabiazal. Mestre em Biotecnologia (UFPI). e-mail: vanessa.campelo@iesvap.edu.br
4 Graduada em Medicina pelo Instituto de Educação Superior do Vale do Parnaíba Campus sede – sabiazal. Especialista em Clínica Médica (HEDA). R4 em gastroenterologia (HU-UFMA). e-mail: marinallagesp@gmail.com
